
【题目】下列几种导电性变化图像,把符合要求的图像序号填在相应的题目后面括号中。
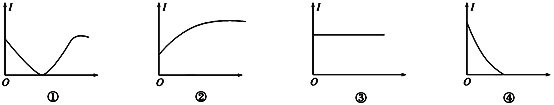
(1)向H2SO4溶液中加入等体积、等物质的量浓度的Ba(OH)2溶液(______)
(2)向H2SO4溶液中通入Cl2直至过量(______)
(3)向AgNO3溶液通入少量HCl(______)
(4)向氨水中通入HCl直至过量(______)
(5)向NaOH溶液中通入少量Cl2(______)
(6)向饱和石灰水中不断通入CO2(______)
【答案】④ ② ③ ② ③ ①
【解析】
溶液导电性和溶液中离子浓度和离子所带电荷数有关,相同条件下,离子浓度越大,导电性越强,离子所带电荷数越高,导电性越强,结合反应中离子的变化分析解答。
(1)向H2SO4溶液中加入等体积、等物质的量浓度的Ba(OH)2溶液二者反应生成硫酸钡和水,离子浓度减小导电性减弱,完全中和导电性接近于0,故选④;
(2)向H2SO4溶液中通入Cl2直至过量,氯气和水反应生成盐酸和次氯酸,离子浓度增大,溶液导电性增强,当溶液饱和时趋于最大后导电性不变,故选②;
(3)向AgNO3溶液通入少量HCl,发生反应生成氯化银沉淀和硝酸,减少的银离子由氢离子补充,溶液中离子浓度基本不变,导电性基本不变,故选③;
(4)向氨水中通入HCl直至过量,氯化氢和一水合氨反应生成氯化铵溶液,溶液中离子浓度增大,导电性增强,饱和后离子浓度基本不变,导电性不变,故选②;
(5)氢氧化钠溶液中通入少量氯气,发生反应生成氯化钠、次氯酸钠和水,氯化钠和次氯酸钠是强电解质完全电离,溶液中离子浓度变化不大,溶液导电性变化不大,故选③;
(6)向饱和石灰水中不断通入CO2,发生反应生成碳酸钙沉淀和水,离子浓度减小,随后继续不断通入二氧化碳,碳酸钙溶解,溶液中离子浓度又增大,导电性先减小后增大,故选①。


科目:高中化学 来源: 题型:
【题目】锂-铜空气燃料电池容量高、成本低,具有广阔的发展前景。该电池工作时发生复杂的铜腐蚀现象,电池总反应为:2Li+Cu2O+H2O=2Cu+2Li++2OH-,其工作原理如图所示,下列说法不正确的是( )
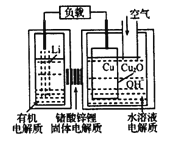
A. 电池放电时,正极附近溶液pH增大
B. 工作时,Li′透过固体电解质向Cu极移动
C. 电池放电过程中,空气中的O2并不参加反应
D. 两极的有机电解质和水溶液电解质不可对换
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学—选修3:物质结构与性质](15分)A、B、C、D为原子序数依次增大的四种元索,A2-和B+具有相同的电子构型;C、 D为同周期元索,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。回答下列问题:
(1)四种元素中电负性最大的是 (填元素符号),其中C原子的核外电子排布式为__________。
(2)单质A有两种同素异形体,其中沸点高的是 (填分子式),原因是 ;A和B的氢化物所属的晶体类型分别为 和 。
(3)C和D反应可生成组成比为1:3的化合物E, E的立体构型为 ,中心原子的杂化轨道类型为 。
(4)化合物D2A的立体构型为 ,中心原子的价层电子对数为 ,单质D与湿润的Na2CO3反应可制备D2A,其化学方程式为 。
(5)A和B能够形成化合物F,其晶胞结构如图所示,晶胞参数,a=0.566nm, F 的化学式为 :晶胞中A 原子的配位数为 ;列式计算晶体F的密度(g.cm-3) 。
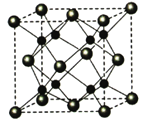
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)甲烷的电子式为_____,其空间结构为_____;乙烯的结构简式为_____,乙烯通入溴水中的化学方程式为_____,其反应类型为_____,C5H12的烃有_____种同分异构体
(2)一装有等体积氯气和甲烷的量筒倒扣在盛水的水槽中,放在室外一段时间后,可观察到的现象是量筒内气体颜色变浅、_____、_____、量筒内液面上升,写出该反应生成一氯甲烷的化学方程式_____,该反应类型为_____.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
①![]() 、
、![]() 、
、![]() 属于碱性氧化物,
属于碱性氧化物,![]() 、
、![]() 、
、![]() 都能和碱溶液发生反应属于酸性氧化物
都能和碱溶液发生反应属于酸性氧化物
②碳酸钠、氢氧化钡、氯化铵、过氧化钠都属于离子化合物
③混合物:漂白粉、水玻璃、![]() 胶体、冰水混合物
胶体、冰水混合物
④醋酸、烧碱、纯碱和生石灰分别属于酸、碱、盐和氧化物
⑤硅导电,铝在浓硫酸中钝化均属于物理变化
⑥盐酸属于混合物,而液氯、冰醋酸均属于纯净物
A.①③⑤B.④⑤⑥C.②④⑥D.②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于苯的叙述正确的是
A.苯的分子式为C6H6,它不能使酸性KMnO4溶液褪色,属于饱和烃
B.从苯的凯库勒式(![]() )看,苯分子中含有碳碳双键,应属于烯烃
)看,苯分子中含有碳碳双键,应属于烯烃
C.苯的同系物是分子中仅含有一个苯环的所有烃类物质
D.苯分子为平面正六边形结构,6个碳原子之间的价键完全相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】均三甲苯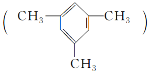 是一种易燃、不溶于水、比水密度小的有毒液体,是重要的有机化工原料,用于制备合成树脂、抗氧化剂等。
是一种易燃、不溶于水、比水密度小的有毒液体,是重要的有机化工原料,用于制备合成树脂、抗氧化剂等。
(1)均三甲苯属于苯的同系物,选用一种试剂区别苯和均三甲苯:________________。
(2)均三甲苯分子中的一个H原子被Cl原子取代,所得产物有________种。
(3)下列属于苯的同系物的是________(填字母)。
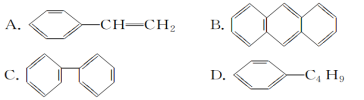
(4)下列物质中,能发生加成反应,也能发生取代反应,同时能使溴水因加成反应而褪色,还能使酸性高锰酸钾溶液褪色的是________(填字母)。
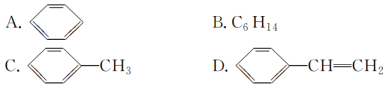
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化性:Br2 > Fe3+> I2,向含 a mol FeI2 和 a mol BaCl2 的混合溶液中缓慢通入 b mol Br2,并不断搅拌,溶液中离子的物质的量随 Br2加入的变化如图所示(不考虑盐类水解、水的电离及溶液体积变化)。则下列说法不正确的是( )
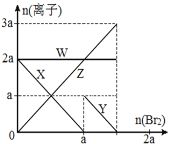
A.离子的还原性 I-> Fe2+> Br-
B.四条线与溶液中离子的对应关系是: X-Fe2+、Y-I-、Z-Br-、W-Cl-
C.当4a =3b时,反应后的离子浓度比:c(Fe2+):c(Fe3+):c(Br-) = 1:2:8
D.当3a≤2b时,发生的离子方程式:2Fe2++ 4I-+ 3Br2=2Fe3++ 2I2+6Br-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A.键角:BF3>CH4>NH3>H2O
B.P4和CH4都是正四面体形分子且键角都为109°28′
C.C22-与O22+互为等电子体,1 mol O22+中含有的π键数目为2NA
D.已知反应N2O4(l)+2N2H4(l)===3N2(g)+4H2O(l),若该反应中有4 mol N—H键断裂,则形成的π键数目为3NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com