
| 实验 编号 | H2C2O4溶液 | 酸性KMnO4溶液 | H2O/mL | 温度/℃ | KMnO4溶液完全褪色时间(s) | ||
| 浓度/mol•L-1 | 体积/mL | 浓度/mol•L-1 | 体积/mL | ||||
| ① | 0.20 | 2.0 | 0.010 | 4.0 | 2.0 | 25 | t1 |
| ② | 0.20 | 4.0 | 0.010 | 4.0 | 0 | 25 | t2 |
| ③ | 0.20 | 4.0 | 0.010 | 4.0 | 0 | 50 | t3 |
分析 (1)KMnO4与H2C2O4在酸性条件下,高锰酸根离子能和草酸发生氧化还原反应生成二价锰离子、二氧化碳和水,根据化合价升降总数相等配平离子方程式;
(2)由表中数据可知3次实验KMnO4溶液的浓度相等,反应时溶液的总体积都是8mL,通过改变H2C2O4溶液的体积来改变反应时H2C2O4溶液的浓度,①②两组温度相同,反应速率由H2C2O4溶液的浓度决定;
(3)根据实验②和实验③除温度不同外,其他条件都相同可知实验目的;
(4)考虑锰离子有催化作用;要想验证锰离子的催化作用,再加入硫酸锰即可.
解答 解:(1)在酸性条件下,高锰酸根离子能和草酸发生氧化还原反应生成二价锰离子、二氧化碳和水,Mn下降5价,C上升1价,1个草酸中有2个碳原子,共上升2价,根据化合价升降相等,配平离子方程2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O,
故答案为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O;
(2)实验①②中KMnO4溶液的浓度相等,反应时溶液的总体积都是8mL,实验①中H2C2O4溶液的用量比实验②少,则实验①中H2C2O4溶液浓度小于实验②,浓度越小,反应速率越慢,则实验①中KMnO4溶液完全褪色时间更长,
故答案为:>;①②两组温度相同,①中H2C2O4溶液浓度小于②;
(3)实验②和实验③反应物的浓度完全相同,只有温度不同,则实验目的是探究浓度不变时,温度对化学反应速率影响,
故答案为:探究浓度不变时,温度对化学反应速率影响;
(4)KMnO4与H2C2O4反应生成硫酸锰,锰离子有催化作用,所以猜想还可能是Mn2+对该化学反应起催化作用;要想验证锰离子的催化作用,在做对比实验时同时加入硫酸锰观察反应速率是否变化即可,不能加氯化锰,因为氯化锰会引入氯离子,不能确定锰离子和氯离子谁起作用,
故答案为:Mn2+对该化学反应起催化作用;B.
点评 本题考查了条件不同对反应速率影响的分析判断,主要是催化剂、温度、浓度对反应速率的影响探究,注意控制变量法的使用,题目难度中等.


 快捷英语周周练系列答案
快捷英语周周练系列答案科目:高中化学 来源: 题型:解答题
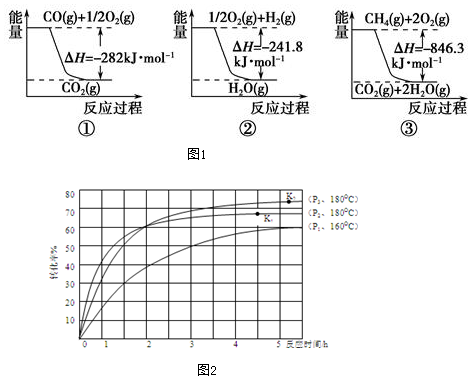
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
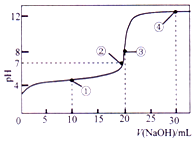 常温下,用 0.1000mol•L-1NaOH 溶液滴定 20.00mL 0.1000mol•L-1的 CH3COOH 溶液所得滴定曲线如图.下列说法正确的是( )
常温下,用 0.1000mol•L-1NaOH 溶液滴定 20.00mL 0.1000mol•L-1的 CH3COOH 溶液所得滴定曲线如图.下列说法正确的是( )| A. | 点①所示的溶液中:c(Na+)+c(H+)>c(CH3COOH)+c(OH-) | |
| B. | 点②所示溶液中:c(Na+)=c(CH3COO-)+c(CH3COOH) | |
| C. | 点③所示溶液中:c(H+)=c(CH3COOH)+c(OH-) | |
| D. | 点④所示溶液中:2c(OH-)-2c(H+)=c(CH3COO-)+3c(CH3COOH) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (或
(或
 ).
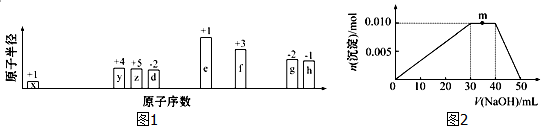
).
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 油脂和蛋白质是人体必需的营养物质,都属于高分子化合物 | |
| B. | 食品包装袋中常有硅胶、生石灰、还原铁粉等,其作用都是吸水防止食品变质 | |
| C. | 采用催化转化技术,可将汽车尾气中的一氧化碳和氮氧化物转化为无毒气体 | |
| D. | 中医古籍《肘后备急方》中“青蒿一握,以水二升渍,绞取汁,尽服之”启发了屠呦呦采用低温提取青蒿素,该提取过程属于化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑤ | B. | ②③⑥ | C. | ②③④⑤ | D. | ②⑤⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com