
| A£® | øĆĢõ¼žĻĀ·“Ó¦µÄĘ½ŗā³£ŹżĪŖ1.6”Į103 | |
| B£® | Ķس£ĒéæöĻĀ£¬øĆ·“Ó¦Ņ»¶ØÄÜ×Ō·¢½ųŠŠ | |
| C£® | ĢāøųĢõ¼žĻĀ£¬SO2µÄ×Ŗ»ÆĀŹŹĒ80% | |
| D£® | µ±ĢåĻµÖŠSO2ŗĶSO3µÄĖŁĀŹÖ®±ČŹĒ1£ŗ1Ź±£¬ŌņøĆ·“Ó¦“ļµ½»ÆŃ§Ę½ŗāדĢ¬ |
·ÖĪö ŅĄ¾Ż»ÆŃ§Ę½ŗāČż¶ĪŹ½ĮŠŹ½¼ĘĖćĘ½ŗāÅØ¶Č£»
A£®½įŗĻĘ½ŗāÅضČŗĶĘ½ŗā³£ŹżøÅÄī¼ĘĖć·“Ó¦µÄĘ½ŗā³£Źż·ÖĪöÅŠ¶Ļ£»
B£®ŅĄ¾Ż”÷H-T”÷S£¼0·“Ó¦×Ō·¢½ųŠŠ£¬½įŗĻ·“Ó¦ĢŲÕ÷·ÖĪöÅŠ¶Ļ£»
C£®ŅĄ¾ŻČż¶ĪŹ½¼ĘĖć½į¹ū£¬×Ŗ»ÆĀŹ=$\frac{ĻūŗÄĮæ}{ĘšŹ¼Įæ}$”Į100%¼ĘĖć£»
D£®µ±ĢåĻµÖŠSO2ŗĶSO3µÄĖŁĀŹÖ®±ČŹĒ1£ŗ1Ź±£¬Ć»ÓŠÖø³öÕżÄę·“Ó¦ĖŁĀŹ£¬ŌņĪŽ·ØÅŠ¶ĻŹĒ·ń“ļµ½Ę½ŗāדĢ¬£®
½ā“š ½ā£ŗŅĄ¾Ż»ÆŃ§Ę½ŗāČż¶ĪŹ½ĮŠŹ½¼ĘĖćĘ½ŗāÅØ¶Č£»
2SO2£Øg£©+O2£Øg£©?2SO3£Øg£©£¬
ĘšŹ¼Įæ£Ømol/L£© 0.025 0.015 0
±ä»ÆĮæ£Ømol/L£© 0.02 0.01 0.02
Ę½ŗāĮæ£Ømol/L£© 0.005 0.005 0.02
A£®Ę½ŗā³£Źż=$\frac{0.0{2}^{2}}{0.005”Į0.00{5}^{2}}$=3200=3.2”Į103£¬¹ŹA“ķĪó£»
B£®”÷H-T”÷S£¼0·“Ó¦×Ō·¢½ųŠŠ£¬2SO2£Øg£©+O2£Øg£©?2SO3£Øg£©£¬·“Ó¦ŹĒ”÷H£¼0£¬”÷S£¼0µÄ·“Ó¦£¬Ķس£ĒéæöĻĀæÉÄÜ“ęŌŚ”÷H-T”÷S£¾0£¬²»Ņ»¶ØÄܹ»×Ō·¢½ųŠŠ£¬¹ŹB“ķĪó£»
C£®ĢāøųĢõ¼žĻĀ£¬SO2µÄ×Ŗ»ÆĀŹ=$\frac{0.02mol/L}{0.025mol/L}$”Į100%=80%£¬¹ŹCÕżČ·£»
D£®Ć»ÓŠøęĖßÕżÄę·“Ó¦ĖŁĀŹ£¬Ōņµ±ĢåĻµÖŠSO2ŗĶSO3µÄĖŁĀŹÖ®±ČŹĒ1£ŗ1Ź±£¬ÕżÄę·“Ó¦ĖŁĀŹ²»Ņ»¶ØĻąµČ£¬øĆ·“Ó¦“ļ²»Ņ»¶Øµ½»ÆŃ§Ę½ŗāדĢ¬£¬¹ŹD“ķĪó£»
¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²éĮĖ»ÆŃ§Ę½ŗā¼ĘĖć£¬ĢāÄæÄѶČÖŠµČ£¬Éę¼°·“Ó¦ĖŁĀŹ”¢Ę½ŗā³£Źż¼ĘĖćµÄ·ÖĪöÅŠ¶Ļ£¬Ć÷Č·»ÆŃ§Ę½ŗā¼°ĘäÓ°ĻģĪŖ½ā“š¹Ų¼ü£¬ŹŌĢāÅąŃųĮĖѧɜµÄ·ÖĪöÄÜĮ¦¼°Įé»īÓ¦ÓĆÄÜĮ¦£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½«Ćŗ×Ŗ»Æ³ÉĘųĢåČ¼ĮĻæÉŅŌÓŠŠ§µŲ¼õÉŁ”°ĪĀŹŅŠ§Ó¦”±µÄĘųĢå²śÉś | |
| B£® | ¼ÓæģĢ«ŃōÄÜ”¢·ēÄÜ”¢ÉśĪļÖŹÄÜ”¢ŗ£ŃóÄܵČĒå½ąÄÜŌ“µÄæŖ·¢ĄūÓĆ | |
| C£® | ŃŠÖĘæŖ·¢ŅŌĖ®“śĢęÓŠ»śČܼĮµÄ»Æ¹¤ĶæĮĻ | |
| D£® | “óĮ¦·¢Õ¹Å©“åÕÓĘų£¬½«·ĻĘśµÄ½ÕøŃ×Ŗ»ÆĪŖĒå½ąøߊ§µÄÄÜŌ“ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ü¢Ż¢Ž | B£® | ¢Ü¢Ż¢Ž¢ß | C£® | ¢Ł¢Ś¢Ū¢Ü | D£® | Č«²æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | H+”¢Fe2+”¢Cr2O72-”¢SO42- | B£® | Na+”¢OH-”¢SO42-”¢HCO3- | ||
| C£® | K+”¢Mg2+”¢SO42-”¢OH- | D£® | H+”¢K+”¢CO32-”¢Cl- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 2Al+2NaOH+2H2OØT2NaAlO2+3H2”ü | B£® | 2Na+2H2OØT2NaOH+H2”ü | ||
| C£® | 2F2+2H2OØT4HF+O2 | D£® | Na2O+2H2OØT2NaOH |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
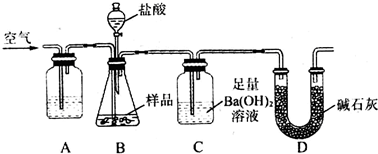
 ČēĶ¼ĖłŹ¾£¬øō°åI¹Ģ¶Ø²»¶Æ£¬»īČū¢ņæÉ×ŌÓÉŅĘ¶Æ£¬M”¢NĮ½øöČŻĘ÷ÖŠ¾ł·¢Éś·“Ó¦£ŗA£Øg£©+3B£Øg£©?2C£Øg£©”÷H=-192kJ•mol-1£®ĻņM”¢NÖŠ£¬¶¼ĶØČėx mol AŗĶy mol BµÄ»ģŗĻĘųĢ壬³õŹ¼M”¢NČŻ»żĻąĶ¬£¬±£³ÖĪĀ¶Č²»±ä£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
ČēĶ¼ĖłŹ¾£¬øō°åI¹Ģ¶Ø²»¶Æ£¬»īČū¢ņæÉ×ŌÓÉŅĘ¶Æ£¬M”¢NĮ½øöČŻĘ÷ÖŠ¾ł·¢Éś·“Ó¦£ŗA£Øg£©+3B£Øg£©?2C£Øg£©”÷H=-192kJ•mol-1£®ĻņM”¢NÖŠ£¬¶¼ĶØČėx mol AŗĶy mol BµÄ»ģŗĻĘųĢ壬³õŹ¼M”¢NČŻ»żĻąĶ¬£¬±£³ÖĪĀ¶Č²»±ä£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©| A£® | Ę½ŗāŹ±AĘųĢåŌŚĮ½ČŻĘ÷ÖŠĢå»ż·ÖŹżæÉÄÜĻąµČ | |
| B£® | Čōx£ŗy=1£ŗ2£¬ŌņĘ½ŗāŹ±£¬MÖŠµÄ×Ŗ»ÆĀŹ£ŗA£¾B | |
| C£® | Čōx£ŗy=1£ŗ3£¬µ±MÖŠ·Å³öČČĮæ172.8 kJŹ±£¬AµÄ×Ŗ»ÆĀŹĪŖ90% | |
| D£® | Čōx=1£¬y=3£¬Ōņ“ļµ½Ę½ŗāŹ±·“Ó¦ĪļµÄ×Ŗ»ÆĀŹN£¾M |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¾ßÓŠĻĀĮŠµē×ÓÅŲ¼Ź½µÄŌ×ÓÖŠ£¬¢Ł1s22s22p63s23p2 ¢Ś1s22s22p3 ¢Ū1s22s22p2 ¢Ü1s22s22p63s23p4£¬Ō×Ó°ė¾¶×ī“óµÄŹĒ¢Ł | |
| B£® | ĻĀĮŠŌ×ӵļŪµē×ÓÅŲ¼ÖŠ£¬¢Ł3s23p1 ¢Ś3s23p2 ¢Ū3s23p3¢Ü3s23p4£¬¶ŌÓ¦µÄµŚŅ»µēĄėÄÜ×ī“óµÄŹĒ¢Ū | |
| C£® | ¢ŁNa”¢K”¢Rb ¢ŚN”¢P”¢As ¢ŪO”¢S”¢Se ¢ÜNa”¢P”¢Cl£¬ŌŖĖŲµÄµēøŗŠŌĖęŌ×ÓŠņŹżµÄŌö¼Ó¶ųµŻŌöµÄŹĒ¢Ü | |
| D£® | ijŌŖĖŲµÄÖš¼¶µēĄėÄÜ£ØkJ•mol-1£©·Ö±šĪŖ738”¢1451”¢7733”¢10540”¢13630”¢17995”¢21703£¬µ±ĖüÓėĀČĘų·“Ó¦Ź±×īæÉÄÜÉś³ÉµÄŃōĄė×ÓŹĒX3+ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com