
| A. | 单质沸点:W>Y | |
| B. | X的最高价氧化物对应的水化物能与Y的氧化物反应 | |
| C. | W与X形成的化合物中含有共价键 | |
| D. | 简单离子的半径:X>Y>Z |
分析 W、X、Y、Z均为短周期元素,W、X同主族,且W最高正价与最低负价的代数和为0,则W位于ⅣA族或ⅠA族;X、Y、Z的M层电子数分别为1、3、7,则X位于ⅠA,所以W为H元素;X为Na元素、Y为Al、Z为Cl元素,据此进行解答.
解答 解:W、X、Y、Z均为短周期元素,W、X同主族,且W最高正价与最低负价的代数和为0,则W位于ⅣA族或ⅠA族;X、Y、Z的M层电子数分别为1、3、7,则X位于ⅠA,所以W为H元素;X为Na元素、Y为Al、Z为Cl元素,
A.W为H,单质为氢气,Y为铝,氢气的沸点小于铝,故A错误;
B.X为Na,其最高价氧化物对应水合物为氢氧化钠,Y为氧化物为氧化铝,氢氧化钠与氧化铝反应生成偏铝酸钠和水,故B正确;
C.W与X形成的化合物为NaH,该化合物中只含有离子键,故C错误;
D.离子的电子层越多,离子半径越大,电子层相同时,核电荷数越大,离子半径越小,则简单离子半径大小为:Z>X>Y,故D错误;
故选B.
点评 本题考查了原子结构与元素周期律的关系,题目难度中等,正确推断元素名称为解答关键,注意熟练掌握原子结构与元素周期律、元素周期表的关系,试题培养了学生的分析能力及灵活应用能力.


科目:高中化学 来源: 题型:选择题
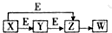 如图是某常见元素M的单质及其化合物间的转化关系图,其中X、Y、Z、W四种物质中均含有元素M,E是另一种单质,下列有关说法中不正确的是( )
如图是某常见元素M的单质及其化合物间的转化关系图,其中X、Y、Z、W四种物质中均含有元素M,E是另一种单质,下列有关说法中不正确的是( )| A. | W可能是硫酸 | B. | Y不可能是Mg | C. | X可能是钠 | D. | Z可能是CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
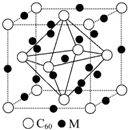 硼及其化合物的研究在无机化学的发展中占有独特的地位.
硼及其化合物的研究在无机化学的发展中占有独特的地位. H++B(OH)4-
H++B(OH)4-查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属的电化学腐蚀比化学腐蚀更普遍 | |
| B. | 航海船船底四周镶嵌锌块保护船体,利用的是牺牲阳极保护法 | |
| C. | 用铝制铆钉连接铁板,铝钉易被腐蚀 | |
| D. | 原电池中电子由正扱流入负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
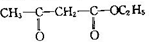 )和聚乙烯醇(PVA)都是重要的有机化工产品,其合成路线如图所示.
)和聚乙烯醇(PVA)都是重要的有机化工产品,其合成路线如图所示.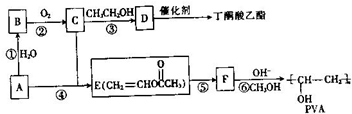
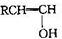 不稳定会自动转化为RCH2CHO.
不稳定会自动转化为RCH2CHO.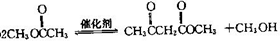
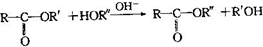
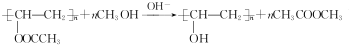 ,该反应的反应类型为取代反应.
,该反应的反应类型为取代反应.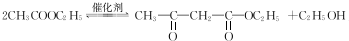 ,Na与生成的乙醇反应,平衡右移,提高D的转化率.(根据化学方程式和平衡移动原理回答)
,Na与生成的乙醇反应,平衡右移,提高D的转化率.(根据化学方程式和平衡移动原理回答) 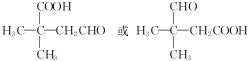 (填结构简式).
(填结构简式).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
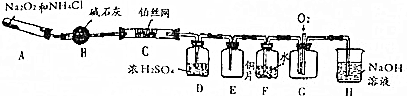
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 28g乙烯和环丁烷的混合气体中含有的碳原子数为2NA | |
| B. | 常温常压下,46gNO2和N2O4的混合气体中含有的原子数为3NA | |
| C. | 标准状况下,22.4L水中含有的质子数为10NA | |
| D. | 1molNa与足量的O2反应,生成Na2O和Na2O2的混合物,转移电子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 向上风口转移 | B. | 向下风口转移 | ||
| C. | 用湿毛巾捂住口鼻 | D. | 及时戴上用硫酸溶液湿润过的口罩 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com