
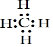 ; B与D组成的三原子分子的结构式为O=C=O.
; B与D组成的三原子分子的结构式为O=C=O.分析 A原子核内仅有1个质子,应为H元素;
D原子最外层电子数是其电子层数的3倍,则有两个电子层,最外层电子数为6,则D为O元素;
B原子的电子总数与D原子的最外层电子数相等,则B为C元素;
C的原子序数介于C、O之间,所以C是N元素,
E原子的L层电子数小于K、M层电子数之和,则最外层应为7个电子,为Cl元素,结合对应单质、化合物的性质以及元素周期律解答该题.
解答 解:(1)A与B组成的最简单化合物为CH4,电子式为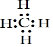 ,B与D组成的三原子分子为CO2,结构式为O=C=O,
,B与D组成的三原子分子为CO2,结构式为O=C=O,
故答案为: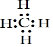 ;O=C=O;
;O=C=O;
(2)一般来说,离子核外电子层数越多,离子半径越大,具有相同核外电子排布的离子,核电荷数越大离子半径越小,应为Cl->N3->O2-,
故答案为:Cl->N3->O2-;
(3)E为Cl,对应的最高价氧化物的水化物为HClO4,为强酸,与氢氧化铝反应生成铝离子,离子方程式为3H++Al(OH)3=Al3++3H2O,
故答案为:HClO4;3H++Al(OH)3=Al3++3H2O;
(4)已知A、B、C、D可组成一种化合物,其原子个数比为8:1:2:3,应为(NH4)2CO3,为离子化合物,
故答案为:(NH4)2CO3;离子;
(5)C为N元素,有多种氧化物,其中甲的相对分子质量最小,则甲为NO,在一定条件下,2L的甲气体与0.5L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,设氧化产物中N元素化合价为a,根据电子转移守恒:2(a-2)=0.5×4,解得a=3,所生成的C的含氧酸盐的化学式是NaNO2,
故答案为:NaNO2.
点评 本题考查位置、结构与性质,为高频考点,把握元素的位置、元素化合物知识为解答的关键,侧重分析与应用能力的考查,注意化学用语及氧化还原反应的使用,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3溶液除去锅炉中水垢(CaSO4):Ca2++CO32-═CaCO3↓ | |
| B. | 用惰性电极电解饱和硫酸铜溶液:2Cu2++2H2O$\frac{\underline{\;通电\;}}{\;}$2Cu+O2↑+4H+ | |
| C. | 铝溶于氢氧化钠溶液:Al+2OH-+H2O=AlO2-+2H2↑ | |
| D. | 用H2O2从酸化的海带灰浸出液中提取碘:2I-+H2O2=I2+2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 现象或事实 | 解释 |
| A. | 肉制品中添加适量的亚硝酸钠 | 亚硝酸钠有防腐的作用 |
| B. | 液氨常用作制冷剂 | 液氨汽化时要吸收大量的热 |
| C. | 利用静电除尘装置除去粉尘 | 胶体粒子带电 |
| D. | Al(OH)3用作塑料的阻燃剂 | Al(OH)3受热熔化吸收大量的热 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 玛瑙、水晶、钻石、红宝石等装饰品的主要成分都是硅酸盐 | |
| B. | 使用含有氯化钙的融雪剂会加速桥梁的腐蚀 | |
| C. | “山东疫苗案”涉及疫苗未冷藏储运而失效,这与蛋白质变性有关 | |
| D. | 沼气是可再生资源,电能是二次能源 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 室温下,1LpH=13的NaOH溶液中,由水电离的OH-数目为0.1NA | |
| B. | 0.1mol${\;}_{38}^{90}$Sr原子中含中子数为3.8NA | |
| C. | 足量的O2与1molNa充分反应,转移的电子数为NA | |
| D. | 50mL12mol•L-1的盐酸与足量MnO2共热,转移电子数为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中子数为18的硫原子:${\;}_{16}^{34}$S | B. | S2-的结构示意图: | ||
| C. | 过氧化氢的电子式:H+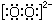 H+ H+ | D. | 葡萄糖的结构简式:C6H12O6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
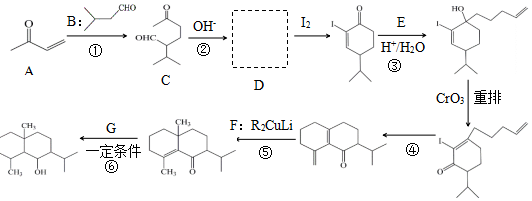
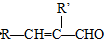 +H2O
+H2O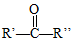 →
→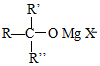 $\stackrel{H+/H_{2}O}{→}$
$\stackrel{H+/H_{2}O}{→}$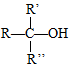

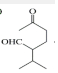 $\stackrel{O{H}^{-}}{→}$
$\stackrel{O{H}^{-}}{→}$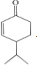 +H2O.
+H2O.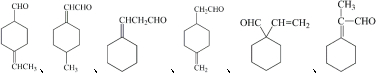
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增加c(CO),平衡向正向移动,反应的平衡常数增大 | |
| B. | 第一阶段,在30℃和50℃两者之间选择反应温度,选50℃ | |
| C. | 第二阶段,Ni(CO)4分解率较低 | |
| D. | 该反应达到平衡时,v生成[Ni(CO)4]=4v生成(CO) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com