
标准状态下,气态分子断开1mol化学键的焓变为键焓.已知 H﹣H, H﹣O 和O=O 键的键焓△H分别为 436kJ•mol﹣1、 463kJ•mol﹣1 和 495kJ•mol﹣1.下列热化学方程式正确的是( )
A.H2O(g) ═H2(g)+1/2O2(g) △H=﹣485kJ•mol﹣1
B.H2O(g)═H2(g)+1/2O2(g) △H=+485kJ•mol﹣1
C.2H2(g)+O2(g)═2H2O(g) △H=+485kJ•mol﹣1
D.2H2(g)+O2(g)═2H2O(g) △H=﹣485kJ•mol﹣1
 考前必练系列答案
考前必练系列答案科目:高中化学 来源:2016-2017年吉林长春白城一中两校高二上期中化学卷(解析版) 题型:填空题
(1)下列化合物的分子中,所有原子都处于同一平面的有
A .乙烷 B.甲苯 C.氯苯 D.四氯乙烯
.乙烷 B.甲苯 C.氯苯 D.四氯乙烯
(2)下列除去杂质的方法正确的是
①除去乙烷中少量的乙烯:光照条件下通入Cl2,气液分离
②除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤、分液、干燥、蒸馏
③除去CO2中少量的SO2:气体通过盛饱和碳酸钠溶液的洗气瓶
④除去乙醇中少量的乙酸:加足量生石灰,蒸馏
(3)有下列各组物质:
A.O2和O3
B.12C和13C
C.CH3 —CH2—CH2—CH3和
—CH2—CH2—CH3和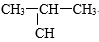
D.和
E.甲烷和庚烷
F.淀粉和纤维素
G.蔗糖和麦芽糖
H.聚乙烯和聚丙烯
① 组两物质互为同位素;
② 组两物质互为同素异形体;
③ 组两物质属于同系物;
④ 组两物质互为同分异构体;
⑤ 组中两物质是同一物质;
⑥ 组中两物质是混合物;
⑦ 聚丙烯的链节是 ;
⑧ 的名称是 。
的名称是 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西西安中学高二实验班上期中化学卷(解析版) 题型:选择题
反应 A(g)+3B(g)=2C(g)+2D(g)在四种不同情况下的反应速率分别为
①v(A)=0.45mol·L-1·min-1
②v(B)=0.6mol·L-1·s-1
③v(C)=0.4mol·L-1·s-1
④v(D)=0.45mol·L-1·s-1
下列有关反应速率的比较中正确的是
A. ④>③=②>① B. ④<③=②<① C. ①>②>③>④ D. ④>③>②>①
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西西安中学高二平行班上期中化学卷(解析版) 题型:选择题
下列事实,不能用勒夏特列原理解释的是( )
A.在合成氨的工业生产中要及时将生成的氨分离出去
B.对 2HI(g) ? H2(g)+I2(g)平衡体系,增大压强可使颜色变深
C.溴水中有下列平衡 Br2+H2O?HBr+HBrO,当加入 AgNO3 溶液后,溶液颜色变浅
D.合成氨反应,为提高氨的产率,理论上不宜采用高温
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西西安中学高二平行班上期中化学卷(解析版) 题型:选择题
把下列4 种Na2S2O3溶液和相应体积的水,分别加入4个盛有20mL 2mol•L﹣1 硫酸的烧杯中,此时, Na2S2O3和H2SO4缓慢地进行反应: Na2S2O3+H2SO4═Na2SO4+S↓+SO2↑+H2O 其中最早出现明显浑浊的是( )
A.25℃20mL 3mol•L﹣1 的Na2S2O3溶液,25mL 蒸馏水
B.0℃30mL 2mol•L﹣1 的Na2S2O3溶液,15mL 蒸馏水
C.25℃10mL 4mol•L﹣1 的Na2S2O3溶液,35mL 蒸馏水
D.0℃10mL 2mol•L﹣1 的Na2S2O3溶液,35mL 蒸馏水
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西省高二上期中化学试卷(解析版) 题型:填空题
向体积为2 L的固定密闭容器中通入3 mol X气体,在一定温度下发生如下反应:2X(g) Y(g)+3Z(g)
Y(g)+3Z(g)
(1)经5 min后反应达到平衡,此时测得容器内的压强为起始时的1.2倍,则用Y表示的速率为____________ mol·L-1·min-1。
(2)若上述反应在甲、乙、丙、丁四个同样的密闭容器中进行,在同一段时间内测得容器内的反应速率分别为甲:v(X)=3.5 mol·L-1·min-1;乙:v(Y)=2 mol·L-1·min-1;丙:v(Z)=4.5 mol·L-1·min-1;丁:v(X)=0.075 mol·L-1·s-1。若其他条件相同,温度不同,则温度由高到低的顺序是(填序号)______ ______。
(3)若向达到(1)的平衡体系中充入氦气,则平衡__________(填“向左”、“向右”或“不”)移动;若从达到(1)的平衡体系中移走部分Y气体,则平衡____________(填“向左”、“向右”或“不”)移动。
(4)若在相同条件下向达到(1)所述的平衡体系中再充入0.5 mol X气体,则平衡后X的转化率与(1)的平衡中X的转化率相比较( )
A.无法确定 B.前者一定大于后者
C.前者一定等于后者 D.前者一定小于后者
(5)若保持温度和压强不变,起始时加入X、Y、Z物质的量分别为a mol、b mol、c mol,达到平衡时仍与(1)的平衡等效,则:a、b、c应该满足的关系为___________________。
(6)若保持温度和体积不变,起始时加入X、Y、Z物质的量分别为a mol、b mol、c mol,达到平衡时仍与(1)的平衡等效,且起始时维持化学反应向逆反应方向进行,则c的取值范围是_________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西省高二上期中化学试卷(解析版) 题型:选择题
下列说法中有明显错误的是
A.对有气体参加的化学反应,减小体积增大压强,可使单位体积内活化分子数增加,因而反应速率增大
B.升高温度,一般可使活化分子的百分数增大,因而反应速率增大
C.活化分子之间发生的碰撞一定为有效碰撞
D.使用催化剂,可使活化分子的百分数大大增加,成千上万倍地增大化学反应的速率
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西省高二上期中化学试卷(解析版) 题型:选择题
“酸碱质子理论”认为凡是能够给出质子(H+)的分子或离子都是酸,凡是能够接受质子的分子或离子都是碱,物质酸性( 碱性)的强弱取决于分子或离子给出(接受)质子能力的大小。按照“酸碱质子理论”,下列说法正确的是
碱性)的强弱取决于分子或离子给出(接受)质子能力的大小。按照“酸碱质子理论”,下列说法正确的是
A.2Na+2H2O===2NaOH+H2↑是酸碱反应
B.ClO-+H2O===HClO+OH-是酸碱反应
C.碱性强弱顺序:ClO->OH->CH3COO-
D.HCO 既是酸又是碱,NH3既不是酸又不是碱
既是酸又是碱,NH3既不是酸又不是碱
查看答案和解析>>
科目:高中化学 来源:2016-2017学年宁夏高一上月考二化学卷(解析版) 题型:简答题
(1)250 mL密度为1.1 g·cm-3、质量分数为24.5%的硫酸跟铁屑充分反应。计算生成H2的体积( 标准状况)(给出必要的计算过程)
标准状况)(给出必要的计算过程)
(2)上述反应中转移电子数目为多少?
(3)亚硝酸钠(NaNO2)具有致癌作用,许多腌制食品中含NaNO2。酸性KMnO4溶液与亚硝酸钠反应的离子反应为 MnO4-+NO2-+H+→Mn2+ + NO3-+H2O(未配平),下列叙述错误的( )
A.生成1mol Mn2+,转移电子为5mol
B.该反应中氮元素被氧化
C.配平后,水的化学计量数为3
D.反应中氧化产物与还原产物的物质的量之比为2:5
(4)向NaOH溶液中逐渐滴入Mg(HCO3)2溶液至沉淀完全的离子方程______________
(5)现有铜片、锌片、导线、小灯泡 、电流表
、电流表 、硫酸铜溶液及烧杯
、硫酸铜溶液及烧杯 ,设计实验证明氧化还原反应中有电子转移。要求画图表示及必要的文字说明。
,设计实验证明氧化还原反应中有电子转移。要求画图表示及必要的文字说明。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com