
某研究性小组探究乙酸乙酯的反应机理,实验如下:
CH3COOH + C2H5OH  CH3COOC2H5 + H2O
CH3COOC2H5 + H2O
投料 1 : 1 CH3COOH转化率 65%
1 : 10 CH3COOH转化率 97%
(在120 ℃下测定)
|
已知:相关物理性质(常温常压)
| 密度g/mL | 熔点/℃ | 沸点/℃ | 水溶性 | |
| 乙醇 | 0.79 | -114 | 78 | 溶 |
| 乙酸 | 1.049 | 16.2 | 117 | 溶 |
| 乙酸乙酯 | 0.902 | −84 | 76.5 | 不溶 |
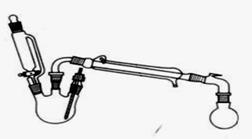
合成反应:
在三颈瓶中加入乙醇5 mL,硫酸5 mL,2小片碎瓷片。漏斗加入乙酸14.3 mL ,乙醇20 mL。冷凝管中通入冷却水后,开始缓慢加热,控制滴加速度等于蒸馏速度,反应温度不超过120 ℃。
分离提纯:
将反应粗产物倒入分液漏斗中,依次用少量饱和的Na2CO3溶液、饱和NaCl溶液、饱和CaCl2溶液洗涤,分离后加入无水碳酸钾,静置一段时间后弃去碳酸钾。最终通过蒸馏得到纯净的乙酸乙酯。
回答下列问题:
(1)酯化反应的机理
用乙醇羟基氧示踪
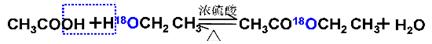

用醋酸羟基氧示踪
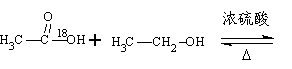
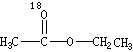
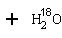
含氧18水占到总水量的一半,酯也一样。这个实验推翻了酯化反应为简单的取代反应。请你设想酯化反应的机理
。
(2)酯化反应是一个可逆的反应,120 ℃时,平衡常数K= 。
(3)如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是________(填正确答案标号)。
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(4)浓硫酸与乙醇如何混合? 。
(5)控制滴加乙酸和乙醇混和液的速度等于蒸馏速度目的是? 。
(6)蒸出的粗乙酸乙酯中主要有哪些杂质? 。
饱和的Na2CO3溶液洗涤除去乙酸。如何判断是否除净? 。
用饱和NaCl溶液洗涤除去残留的Na2CO3溶液,为什么不用水? 。
科目:高中化学 来源: 题型:
下列说法或表达正确的是
①次氯酸的结构式为 H—Cl—O
②含有离子键的化合物都是离子化合物
③蛋白质、漂白粉、苛性钾、液氨分别为纯净物、混合物、强电解质和非电解质
④丁达尔效应可用于区别溶液和胶体,云、雾均能产生丁达尔效应
⑤酸性氧化物不一定是非金属氧化物,但是碱性氧化物一定是金属氧化物
A.①②④ B.①③⑤ C.②④⑤ D.③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
已知1 mol红磷转化为1 mol白磷,吸收18.39 kJ热量。
①4Ps,红)+5O2g)===2P2O5s) ΔH1
②4Ps,白)+5O2g)===2P2O5s) ΔH2
则ΔH1与ΔH2的关系正确的是 )。
A.ΔH1=ΔH2 B.ΔH1>ΔH2
C.ΔH1<ΔH2 D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
如图是用铁铆钉固定两个铜质零件的示意图,若将该零件置于潮湿空气中,下列说法正确的是( )。
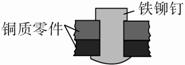
A.发生电化学腐蚀,铜为负极,铜极产生H2
B.铜易被腐蚀,铜极上发生还原反应,吸收O2
C.铁易被腐蚀,铁发生氧化反应:Fe-2e-===Fe2+
D.发生化学腐蚀:Fe+Cu2+===Cu+Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
分子式为C5H12O的饱和一元醇与和它相对分子质量相同的饱和一元羧酸进行酯化反应,生成的酯共有(不考虑立体异构)
A.13种 B.14种 C.15种 D.16种
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,下列各组离子在指定的溶液中可能大量共存的是( )
A.无色透明溶液中:Al3+、Ca2+、Cl-、HCO3-。
B.含大量Fe3+的溶液中:K+、I-、SO42-、NO3-。
C.与Al反应放出H2的溶液中:NH4+、Na+、NO3-、F- 。
D.由水电离出的c(H+) = 1.0×10-14mol/L的溶液中:Mg2+、K+、Cl-、SO42-。
查看答案和解析>>
科目:高中化学 来源: 题型:
Fe2+和I-是两种常见的还原性离子。
(1)向FeSO4溶液中滴加氯水,溶液由浅绿色变成黄色,反应的离子方程式为__________________(2分);
向KI溶液中滴加氯水,溶液由无色变成黄色,反应的离子方程式为______________________ (2分)。
(2)请以FeSO4溶液、KI溶液、氯水为试剂探究Fe2+和I-的还原性强弱。
①提出假设:假设1:Fe2+还原性强于I-;假设2:_____________________________(1分)
②设计实验方案,写出实验步骤、预期现象和结论。其他限选试剂:3 mol·L-1 H2SO4、0.01 mol·L-1 KMnO4、20% KSCN、3%H2O2、淀粉溶液、紫色石蕊溶液。
| 实验步骤(6分) | 预期现象与结论(2分) |
| 步骤1:取2mLFeSO4溶液和2mLKI溶液混合于试管中,再_________ __ | 现象:溶液变成黄色。结论:可能是生成了Fe3+、也可能是生成了I2。 |
| 步骤2:___________________________
|
|
(3)利用(2)②中提供的试剂证明碘与铁的化合物中铁显+2价,实验操作和现象是:
取少量样品溶于水,______________________________________________________。(3分)
查看答案和解析>>
科目:高中化学 来源: 题型:
在298 K时,下列反应的ΔH依次为:
C2H5OH(l)+3O2(g)===2CO2(g)+3H2O(l)
ΔH1=-1 366.8 kJ·mol-1
C(石墨)+O2(g)===CO2(g)
ΔH2=-393.5 kJ·mol-1
H2(g)+1/2O2(g)===H2O(l)
ΔH3=-285.8 kJ·mol-1
乙醇(C2H5OH)、氢气、石墨和氧气的熵值分别为:161.0 J·mol-1·K-1、130.6 J·mol-1·K-1、5.74 J·mol-1·K-1、205.3 J·mol-1·K-1,则298 K时,由单质生成1 mol 乙醇的ΔH、ΔS及ΔH-TΔS分别为多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,将2 mol A和2 mol B两种气体混合放入体积为2 L的 密闭刚性容器中,发生反应:3A(g)+B(g)
密闭刚性容器中,发生反应:3A(g)+B(g)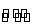 xC(g)+2D(g)
xC(g)+2D(g)
2 min末反应达到平衡,生成0.8 mol D,并测得C的浓度为0.4 mol·L-1,下列说法正确的是( )
D,并测得C的浓度为0.4 mol·L-1,下列说法正确的是( )
A.x的值为1
B.A的转化率为40%
C.此温度下该反应的平衡常数K等于0.5
D.A和B的平衡转化率相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com