
| 实验序号 | 操作及现象 |
| i | 取少量固体样品,加入过量稀盐酸,固体溶解,产生无色气体(经检验为H2),溶液呈浅黄色 |
| ii | 向i所得溶液中加入少量KSCN溶液,溶液呈浅红色,再加入H2O2溶液,产生无色气体(经检验为O2),溶液变为深红色 |
分析 (1)反应中吸热、放热与反应条件没有必然关系,需要根据反应物总能量与生成物总能量大小进行比较;铝热反应中由于铝的还原性较强,所以才能够将还原性弱的金属置换出来;
(2)铝与氧化铁在高温下发生反应生成氧化铝和铁,据此写出反应的化学方程式;
(3)取少量固体样品,加入过量稀盐酸,固体溶解,产生无色气体(经检验为H2),溶液呈浅黄色,说明溶液中含有铁离子;向i所得溶液中加入少量KSCN溶液,溶液呈浅红色,再加入H2O2溶液,产生无色气体(经检验为O2),溶液变为深红色,说明加入双氧水后,溶液中亚铁离子被氧化成铁离子,所以溶液由浅红色变为深红色,则溶液中铁元素存在形式为Fe2+、Fe3+;铁离子能够做催化剂,使双氧水分解生成氧气;可以用氢氧化钠溶液鉴别反应后的固体中是否含有金属铝,据此进行解答.
解答 解:(1)a.该反应需在高温下发生,所以是吸热反应:反应吸热、放热与反应条件没有必然关系,该反应中反应物总能量大于生成物总能量,所以该反应为放热反应,故a错误;
b.铝热反应中,由于铝的还原性较强,所以铝能将相对不活泼的金属从其化合物中置换出来,故b正确;
故答案为:b;
(2)铝与氧化铁发生的铝热反应方程式为:2Al+Fe2O3$\frac{\underline{\;\;△\;\;}}{\;}$2Fe+Al2O3,故答案为:2Al+Fe2O3$\frac{\underline{\;\;△\;\;}}{\;}$2Fe+Al2O3;
(3)取少量固体样品,加入过量稀盐酸,固体溶解,产生无色气体(经检验为H2),溶液呈浅黄色,说明溶液中含有铁离子;向i所得溶液中加入少量KSCN溶液,溶液呈浅红色,再加入H2O2溶液,产生无色气体(经检验为O2),溶液变为深红色,说明加入双氧水后,溶液中亚铁离子被氧化成铁离子,所以溶液由浅红色变为深红色,则溶液中铁元素存在形式为Fe2+、Fe3+,
①根据分析可知,铁元素在溶液中存在形式为:Fe2+、Fe3+,故答案为:Fe2+、Fe3+;
②铁、氧化铁都不与氢氧化钠溶液反应,而铝能够与氢氧化钠溶液反应,所以可用氢氧化钠溶液检验样品中是否含Al单质,故答案为:NaOH溶液;
③ii中双氧水在铁离子催化作用下分解生成氧气,反应的化学方程式为:2H2O2$\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑,故答案为:2H2O2$\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑.
点评 本题考查了铝热反应,题目难度中等,涉及铝热反应原理、化学方程式书写、物质检验与鉴别方法等知识,明确铝热反应原理为解答关键,试题侧重考查学生的分析、理解能力及化学实验能力.


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案科目:高中化学 来源: 题型:选择题
| A. | X的原子序数比Y大 | B. | X的原子半径比Y大 | ||
| C. | X原子的最外层电子数比Y小 | D. | X元素的最高正价比Y大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①>②>③ | B. | ②>①>③ | C. | ③>①>② | D. | ②>③>① |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加热 | B. | 保持容器体积不变,增加H2输入量 | ||
| C. | 充入N2,保持容器内压强不变 | D. | 充入N2,保持容器体积不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
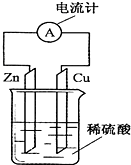
| A. | 锌片上有气泡产生 | B. | 烧杯中溶液逐渐呈蓝色 | ||
| C. | 电流由铜片通过导线流向锌片 | D. | 该装置能将电能转变为化学能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纯碱溶液去油污 | |
| B. | 铁在潮湿的环境下生锈 | |
| C. | 将饱和FeCl3溶液滴加到沸水中制得Fe(OH)3 胶体 | |
| D. | 铵态氮肥不能与草木灰混合施用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 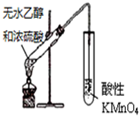 A装置用于检验乙醇发生消去反应的产物 | |
| B. | 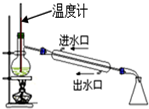 B装置可用于分离乙醇和丙三醇形成的混合物 | |
| C. | 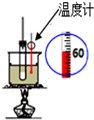 C装置用于实验室制硝基苯 | |
| D. | 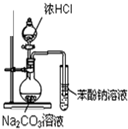 D装置可证明酸性:盐酸>碳酸>苯酚 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用溶解、过滤的方法提纯含有少量BaSO4的BaCO3 | |
| B. | 用过滤的方法除去NaCl溶液中含有的少量淀粉胶体 | |
| C. | 用渗析的方法精制Fe(OH)3胶体 | |
| D. | 用加热→蒸发的方法可以除去粗盐中的CaCl2、MgCl2等杂质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该溶液中溶剂与溶质的质量比为m(水):m(溶质)=( $\frac{18na}{M}$+b):(a-$\frac{18na}{M}$) | |
| B. | 该溶液的物质的量浓度为c=$\frac{1000a}{MV}$mol•L-1 | |
| C. | 该溶液中溶质的质量分数为ω=$\frac{100a(M-18n)}{a+b}$% | |
| D. | 该溶液的密度为ρ=$\frac{1000(a+b)}{V}$g•L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com