
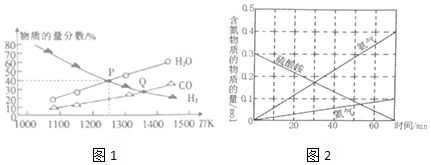
���� ��1����ͼ1���������¶����ߣ�����������С��˵������ƽ��������У�����ӦΪ���ȷ�Ӧ��
��Q���¶ȸ���P�㣬�¶�Խ��ƽ��������У��������ʵ�����������ѹǿ���������ʵ������������
��P���Ӧ�¶��£�������ˮ���������ʵ���������ͬΪ40%����ϻ�ѧ��Ӧ���м�����ʽ����õ�ת���ʺ�ƽ�ⳣ����
��2����2Cu2S��s��+3O2��g���T2Cu2O��s��+2SO2��g����H=-768.2kJ/mol
��2Cu2O+Cu2S��s���TCu��s��+SO2��g����H=+116kJ/mol��
��ϸ�˹���ɼ��㣨��+�ڣ���$\frac{1}{3}$���õ�Cu2S��O2��Ӧ����Cu��SO2���Ȼ�ѧ����ʽ��
��3����֪������ Kb��NH3•H2O��=1.5��l0-5 Ka1��H2SO3��=1.6��l0-2 Ka2��H2SO3��=1��10-7������̶�H2SO3��NH3•H2O��HSO3-���ð�ˮ����ת��ΪNH4HSO3��Һ��HSO3-����̶ȴ���Һ�����ԣ���Һ��c��SO32-����c��H2SO3����
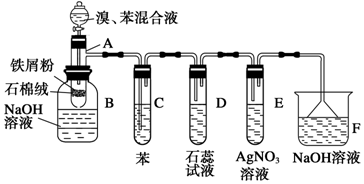
��4����500��������立ֽ�����еõ�4�ֲ���京��������ʱ��仯��ϵ��ͼ����ʾ������立ֽ����ɵ��������������������ˮ����ϵ����غ��ԭ���غ���ƽ��д��
��� �⣺��1����ͼ1���������¶����ߣ�����������С��˵������ƽ��������У�����ӦΪ���ȷ�Ӧ��a��0��
�ʴ�Ϊ������
��Q���¶ȸ���P�㣬�¶�Խ��ƽ��������У��������ʵ�������������ѹǿ�����������ڵ���ѹ��P�㣼Q�㣬
�ʴ�Ϊ������
�������Ϊ2L�ĺ����ܱ������м���0.1molMoS2��0.2molNa2CO3��������0.4molH2��P���Ӧ�¶��£�������ˮ���������ʵ���������ͬΪ40%���� ����CO���ʵ���Ũ��Ϊx��
������Ӧ��MoS2��s��+2Na2CO3��s��+4H2��g��?Mo��s��+2CO��g��+4H2O��g��+2Na2S��s��
��ʼ����mol/L�� 0.2 0 0
�仯����mol/L�� 2x x 2x
ƽ������mol/L�� 0.2-2x x 2x
$\frac{2x}{0.2-2x+x+2x}$��100%=40%
x=0.05��
H2��ƽ��ת����=$\frac{2��0.05}{0.2}$��100%=50%��
ƽ�ⳣ��K=$\frac{��2��0.05��^{4}��0.0{5}^{2}}{��0.2-0.05��2��^{4}}$=0.0025��
�ʴ�Ϊ��50%��0.0025��
��2����2Cu2S��s��+3O2��g���T2Cu2O��s��+2SO2��g����H=-768.2kJ/mol
��2Cu2O+Cu2S��s���TCu��s��+SO2��g����H=+116kJ/mol��
��ϸ�˹���ɼ��㣨��+�ڣ���$\frac{1}{3}$���õ�Cu2S��O2��Ӧ����Cu��SO2���Ȼ�ѧ����ʽ��Cu2S��s��+O2��g��=2Cu��s��+SO2��g����H=-217.4kJ/mol��
�ʴ�Ϊ��Cu2S��s��+O2��g��=2Cu��s��+SO2��g����H=-217.4kJ/mol��
��3����3����֪������ Kb��NH3•H2O��=1.5��l0-5 Ka1��H2SO3��=1.6��l0-2 Ka2��H2SO3��=1��10-7������̶�H2SO3��NH3•H2O��HSO3-���ð�ˮ����ת��ΪNH4HSO3��Һ��HSO3-����̶ȴ���Һ�����ԣ���ҺPH��7����Һ��c��SO32-����c��H2SO3����
�ʴ�Ϊ����������
��4����500��������立ֽ�����еõ�4�ֲ���京��������ʱ��仯��ϵ��ͼ����ʾ������立ֽ����ɵ��������������������ˮ����ϵ����غ��ԭ���غ���ƽ��д�õ���ѧ����ʽΪ3��NH4��2SO4$\frac{\underline{\;\;��\;\;}}{\;}$N2��+4NH3��+3SO2��+6H2O����
�ʴ�Ϊ��3��NH4��2SO4?N2��+4NH3��+3SO2��+6H2O����
���� ���⿼�����Ȼ�ѧ����ʽ��˹���ɼ���Ӧ�á�ͼ�����������ѡ��������ԭ��Ӧ�Ͳ�����жϡ������ܽ�Ȳ�ͬ�õ�����ķ���������ˮ���������ʵ���̶ȱȽϵ�֪ʶ�㣬���ջ����ǽ���ؼ�����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
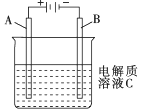 ��1���£�N2H4���ֳ���������һ�ֿ�ȼ��Һ�壬������ȼ�ϣ���-����ȼ�ϵ����һ�ּ���ȼ�ϵ�أ��������Һ��20%��30%��KOH��Һ����Ӧ����һ�ֿ��Բ������ѭ�������壮�õ�طŵ�ʱ�������ĵ缫��Ӧʽ�ǣ�N2H4+4OH--4e-=4H2O+N2����
��1���£�N2H4���ֳ���������һ�ֿ�ȼ��Һ�壬������ȼ�ϣ���-����ȼ�ϵ����һ�ּ���ȼ�ϵ�أ��������Һ��20%��30%��KOH��Һ����Ӧ����һ�ֿ��Բ������ѭ�������壮�õ�طŵ�ʱ�������ĵ缫��Ӧʽ�ǣ�N2H4+4OH--4e-=4H2O+N2�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����10%��ZnSO4��Һ����l0gZnSO4�ܽ���90gˮ�� | |
| B�� | �����Ȼ�̼��ȡ��ˮ�еĵ�ʱ����������Ȼ�̼��Һ�ӷ�Һ©���¿ڷų� | |
| C�� | NaCl��Һ�����ᾧʱ������Ѫ���о���������ʣ������Һ��ʱ��ֹͣ���� | |
| D�� | ��������ˮ�������л�ԭ��ʱ������������Һ�м��뼸��ϡ���ᣬˮԡ���ȼ����ӣ��������м������Ƶ�������Һ����ˮԡ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ǧ���������ɽ | B�� | ѩ��ɽ������Ȫ | C�� | ������ɳʼ���� | D�� | ����ɻ���ʼ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
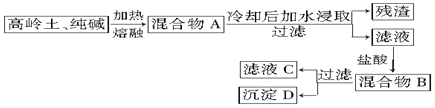
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����

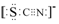 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
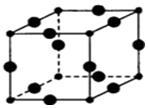 ��1��ijԪ��ԭ�ӵļ۵��ӹ���Ϊ4s24p1�������ڵ������ڢ�A�壬��p��Ԫ�أ�
��1��ijԪ��ԭ�ӵļ۵��ӹ���Ϊ4s24p1�������ڵ������ڢ�A�壬��p��Ԫ�أ�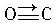 ��CO�ṹ�����Ƶķ�����N2�������ֽṹ���Ƶķ����У����ӵļ��Բ���ͬ�����ͬ������ͬ������
��CO�ṹ�����Ƶķ�����N2�������ֽṹ���Ƶķ����У����ӵļ��Բ���ͬ�����ͬ������ͬ������| ���� | NaCl | KCl | CaO |
| ������/kJ•mol-1 | 786 | 715 | 3 401 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������2-�����黥Ϊͬ���칹�� | |
| B�� | ����ϩ��ʹ������Ȼ�̼��Һ��ɫ�������ķ�Ӧ�Ǽӳɷ�Ӧ | |
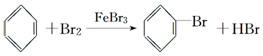
| C�� | ������ʹ���Ը��������Һ��ɫ������FeBr3����������Һ�巢��ȡ����Ӧ | |
| D�� | ��ȥ���������в��������ᣬ��Ч�Ĵ���������ˮϴ���Һ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com