
ÓĆĻĀĮŠŅĒĘ÷”¢Ņ©Ę·ŃéÖ¤ÓÉĶŗĶŹŹĮæÅØĻõĖį·“Ó¦²śÉśµÄĘųĢåÖŠŗ¬NO£ØŅĒĘ÷“ÓĶ¼Ź¾ĖłĮŠÖŠŃ”ÓĆ£¬N2ŗĶO2µÄÓĆĮææÉ×ŌÓÉæŲÖĘ£©”£ŅŃÖŖ£ŗ¢ŁNO+NO2+2OH£”ś2NO+H2O¢ŚĘųĢåŅŗ»ÆĪĀ¶Č£ŗNO2 21”ę£¬NO-152”ę
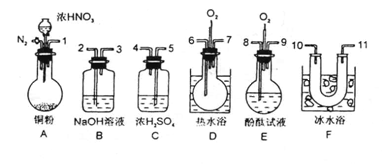 |
£Ø1£©ŅĒĘ÷µÄĮ¬½ÓĖ³Šņ£Ø°“×ó”śÓŅĮ¬½Ó£¬Ģīø÷½ÓæŚµÄ±ąŗÅ£©ĪŖ ”£
£Ø2£©·“Ó¦Ē°Ó¦ĶØČėN2£¬ÄæµÄŹĒ ”£
£Ø3£©×°ÖĆFµÄ×÷ÓĆŹĒ ”£
£Ø4£©Č·ČĻĘųĢåÖŠŗ¬NOµÄĻÖĻóŹĒ ”£
£Ø5£©ČōĶØČėO2¹żĮæŌņBÖŠ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ ”£
£Ø1£©1,5,4,10,11,6,7,2£Ø10ŗĶ11æÉŅŌµßµ¹£©
£Ø2£©ĒżøĻ×°ÖĆÖŠæÕĘų£¬·ĄÖ¹·“Ó¦²śÉśµÄNO±»Ńõ»Æ
£Ø3£©ĶØČėO2ŗó×°ÖĆDÖŠÓŠŗģ×ŲÉ«ĘųĢåÉś³É
£Ø4£©·ÖĄėNOŗĶNO2£Ø»ņŹ¹NO2Ņŗ»Æ£©
£Ø5£©4NO2+O2+4NaOH”ś4NaNO2+2H2O
ĢāÖŠŅŖĒó“Ó±»Ń”ŅĒĘ÷ŗĶ×°ÖĆÖŠŃ”³öŹŹµ±ŅĒĘ÷ŗĶ×°ÖĆĄ“ŃéÖ¤CuŗĶÅØHNO3·“Ó¦²śÉśµÄĘųĢåÖŠÓŠNO”£¼ģŃéNOµÄŅ»°ć·½·ØŹĒĄūÓĆĖüÄܱ»O2Ńõ»Æ¶ųÉś³É×ŲÉ«ĘųĢå£ØNO2£©µÄŌĄķ”£¶ųCuÓėÅØHNO3·“Ó¦Ņ²ÓŠNO2ĘųĢåÉś³É£¬ĖłŅŌŌŚ¼ģŃéNOÖ®Ē°±ŲŠė½«NO2³żČ„”£øł¾ŻĢāŹ¾ŠÅĻ¢£¬ NO2Ņ×Ņŗ»Æ£¬ĖłŅŌæÉĄūÓĆ“ĖŠŌÖŹ½«»ģŗĻĘųĢåĄäČ“ŅŌ“ļµ½·ÖĄėNO2ŗĶNOµÄÄæµÄ”£ÓÉӌװÖĆÖŠÓŠæÕĘų£¬Äܽ«Éś³ÉµÄNOŃõ»Æ¶ų“ļ²»µ½ŹµŃéÄæµÄ£¬ĖłŅŌ±ŲŠėĻČĻņ×°ÖĆÖŠĶØČėN2£¬ĒżøĻµōæÕĘų”£ÓÉÓŚŌŚ±łĖ®Ō”ÖŠNOĪĀ¶Č½µµĶ£¬ÓėŃõĘų·“Ó¦ŗóŅ×Éś³Éøü¶ąµÄN2O4£¬¼“2NO2![]() N2O4-Q£¬ĖłŅŌӦєŌńČČĖ®Ō”µÄ×°ÖĆD£¬ĪŖ·ĄÖ¹ĪŪČ¾£¬ŹµŃé×īŗóŠčÓŠĪ²Ęų“¦Ąķ×°ÖĆ”£ĮķĶā£¬ĪŖ·ĄÖ¹NO2ÓėH2O·“Ӧɜ³ÉNO£¬ŠčŅŖŌŚNO2Ņŗ»ÆĒ°½«H2O£ØĘų£©³żČ„”£±¾ĢāÖ»ÄÜĻČ³żČ„Ė®ŌŁ³żČ„NO2²ÅÄÜÖ¤Ć÷NOµÄ“ęŌŚ£¬ĆüĢāÕßĶعżŃĻĆܵĹ¹Ė¼£¬ÖŲŹÓŹµŃéÉč¼ĘµÄÄÜĮ¦ŃµĮ·£¬“ļµ½ĮĖ¶ŌŹµŃéÄÜĮ¦æ¼²éµÄÄæµÄ£¬Ņ²ĢåĻÖĮĖæĘѧĖ¼Ī¬ĖŲÖŹµÄÅąŃų”£½āĢāÕßÖ»ÓŠæĖ·žĖ¼Ī¬¶ØŹĘ”¢ŌĖÓĆæĘѧĖ¼Ī¬·½·Ø£¬·½ÄÜĻū³ż“ķĪóŅž»¼”£
N2O4-Q£¬ĖłŅŌӦєŌńČČĖ®Ō”µÄ×°ÖĆD£¬ĪŖ·ĄÖ¹ĪŪČ¾£¬ŹµŃé×īŗóŠčÓŠĪ²Ęų“¦Ąķ×°ÖĆ”£ĮķĶā£¬ĪŖ·ĄÖ¹NO2ÓėH2O·“Ӧɜ³ÉNO£¬ŠčŅŖŌŚNO2Ņŗ»ÆĒ°½«H2O£ØĘų£©³żČ„”£±¾ĢāÖ»ÄÜĻČ³żČ„Ė®ŌŁ³żČ„NO2²ÅÄÜÖ¤Ć÷NOµÄ“ęŌŚ£¬ĆüĢāÕßĶعżŃĻĆܵĹ¹Ė¼£¬ÖŲŹÓŹµŃéÉč¼ĘµÄÄÜĮ¦ŃµĮ·£¬“ļµ½ĮĖ¶ŌŹµŃéÄÜĮ¦æ¼²éµÄÄæµÄ£¬Ņ²ĢåĻÖĮĖæĘѧĖ¼Ī¬ĖŲÖŹµÄÅąŃų”£½āĢāÕßÖ»ÓŠæĖ·žĖ¼Ī¬¶ØŹĘ”¢ŌĖÓĆæĘѧĖ¼Ī¬·½·Ø£¬·½ÄÜĻū³ż“ķĪóŅž»¼”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā
 £Ø2011?»ĘɽģÄā£©ČēĶ¼ŹĒø÷ÖÖ²»Ķ¬ĆܶȵÄĻõĖįÓėĢś·“Ó¦£ØĻąĶ¬ĪĀ¶Č£©Ź±Ö÷ŅŖ»¹Ō²śĪļµÄ·Ö²¼Ķ¼£®ĒėČĻÕę¶ĮĶ¼·ÖĪö£¬»Ų“šÓŠ¹ŲĪŹĢā£®
£Ø2011?»ĘɽģÄā£©ČēĶ¼ŹĒø÷ÖÖ²»Ķ¬ĆܶȵÄĻõĖįÓėĢś·“Ó¦£ØĻąĶ¬ĪĀ¶Č£©Ź±Ö÷ŅŖ»¹Ō²śĪļµÄ·Ö²¼Ķ¼£®ĒėČĻÕę¶ĮĶ¼·ÖĪö£¬»Ų“šÓŠ¹ŲĪŹĢā£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| a |
| 4 |
| a |
| 2 |
| a |
| 4 |
| a |
| 2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2010Äźø£½ØŹ”ÕÄÖŻČżÖŠøßČżÉĻѧʌµŚ¶ž“ĪŌĀæ¼ŹŌ¾ķ»ÆѧŹŌĢā ĢāŠĶ£ŗŹµŃéĢā
ÓĆĻĀĮŠŅĒĘ÷”¢Ņ©Ę·ŃéÖ¤ÓÉĶŗĶŹŹĮæĻõĖį·“Ó¦²śÉśµÄĘųĢåÖŠŗ¬NO£ØŅĒĘ÷æÉŃ”ŌńŹ¹ÓĆ£¬N2ŗĶO2µÄÓĆĮææÉ×ŌÓÉæŲÖĘ£©”£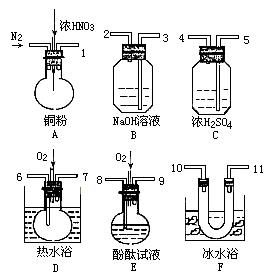
ŅŃÖŖ£ŗ¢Ł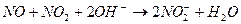 ¢Ś ĘųĢåŅŗ»ÆĪĀ¶Č£ŗNO2 21”ę£¬ NO -152”ę
¢Ś ĘųĢåŅŗ»ÆĪĀ¶Č£ŗNO2 21”ę£¬ NO -152”ę
ŹŌ»Ų“š£ŗ
£Ø1£©Š“³ö×°ÖĆAÖŠ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½_____ ”£
£Ø2£©ŅĒĘ÷µÄĮ¬½ÓĖ³Šņ£Ø°“×ó”śÓŅĮ¬½Ó£¬Ģīø÷½ÓæŚµÄ±ąŗÅ£©ĪŖ____
”£ŌŚĢī¼ÓŅ©
Ę·Ē°Ó¦ĻČ½ųŠŠµÄ²Ł×÷ŹĒ ”£
£Ø3£©·“Ó¦Ē°ĻČĶØČėN2£¬ÄæµÄŹĒ______ £»
£Ø4£©Č·ČĻĘųĢåÖŠŗ¬NOµÄĻÖĻóŹĒ________ ”£
£Ø5£©×°ÖĆ£Ā”¢FµÄ×÷ÓĆŹĒ _______ ”””””””””””””” ”””” ”£
£Ø6£©Čō“Ó£Į³öĄ“µÄ»ģŗĻĘųĢåÖŠNO2”¢NOµÄĢå»ż·Ö±šĪŖV1mL”¢V2mL£¬Čō×īÖÕµŖµÄŃõ»ÆĪļĶźČ«±»ČÜŅŗĪüŹÕ£¬×°ÖĆÖŠÖĮÉŁŠčŅŖ³äČėŃõĘųµÄĢå»żĪŖ£ŗ £ØĻąĶ¬×“Ģ¬ĻĀ£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2011-2012ѧğ½Ī÷Ź”øßČżÉĻѧʌµŚČż“ĪŌĀæ¼»ÆѧŹŌ¾ķ£ØĘÕ£© ĢāŠĶ£ŗŃ”ŌńĢā
£Ø12·Ö£©ĻĀĶ¼ŹĒø÷ÖÖ²»Ķ¬ĆܶȵÄĻõĖįÓėĢś·“Ó¦(ĻąĶ¬ĪĀ¶Č)Ź±Ö÷ŅŖ»¹Ō²śĪļµÄ·Ö²¼Ķ¼”£ĒėČĻÕę¶ĮĶ¼·ÖĪö£¬»Ų“šÓŠ¹ŲĪŹĢā”£

¢ÅĻĀĮŠŠšŹöÖŠÕżČ·µÄŹĒ(ĢīŠņŗÅ) ”£
A.Ķ¼ÖŠŗį×ų±źŹĒĻõĖįµÄĆÜ¶Č£¬ĻõĖįµÄĆܶČŌ½“ó£¬ĘäÅضČŌ½“ó
B.µ±»¹Ō¼ĮŗĶĪĀ¶ČĻąĶ¬Ź±£¬²»Ķ¬ÅØ¶ČµÄĻõĖį±»»¹ŌµÄ²śĪļ²»ŹĒµ„Ņ»µÄ£¬Ö»ŹĒŌŚÄ³ÅØ¶ČŹ±£¬ŅŌijÖÖ²śĪļĪŖÖ÷¶ųŅŃ
C.ĻõĖįµÄÅضČŌ½“󣬻¹Ō²śĪļÖŠNŌŖĖŲµĶ»ÆŗĻ¼Ū²śĪļŌ½¶ą
D.µ±ĻõĖįĆܶȓóÓŚ1.3 g”¤cm-3Ź±£¬»¹Ō²śĪļÖ÷ŅŖĪŖNO”¢NO2
¢Ęµ±ĻõĖįČÜŅŗµÄĆܶČĪŖ1.36 g”¤cm-3Ź±£¬ĻĀĮŠ»Æѧ·½³ĢŹ½ÖŠ£¬ÄܽĻ×¼Č·±ķ“ļFeÓė¹żĮæĻõĖį·“Ó¦µÄŹĒ(ĢīŠņŗÅ£© ”£
A.2Fe + 10HNO3 == 2Fe(NO3)3 + NO”ü£«3NO2”ü£«5H2O
B.4Fe + 18HNO3 == 4Fe(NO3)3 + 3NO”ü£«3NO2”ü£«9H2O
C.3Fe + 12HNO3 == 2Fe(NO3)3 + Fe(NO3)2 + 2NO”ü£«2NO2”ü£«3H2O
¢ĒĆܶČĪŖ1.26 g”¤cm-3£¬ÖŹĮæ·ÖŹżĪŖ50.0 %µÄĻõĖį£¬ĘäĪļÖŹµÄĮæÅØ¶ČŹĒ mol”¤L-1”£
¢ČĻŽÓĆĻĀĮŠŅĒĘ÷”¢Ņ©Ę·ŃéÖ¤ÓÉĢśŗĶ¹żĮæ1.36 g”¤cm-3ĻõĖį·“Ó¦²śÉśµÄĘųĢåÖŠŗ¬ÓŠNO(²»æ¼ĀĒN2O4)”£Éč¼ĘŅ»øöŗĻĄķ¶ų¼ņµ„µÄŹµŃé·½°ø£ØŅĒĘ÷æÉŃ”ŌńŹ¹ÓĆ£¬N2µÄÓĆĮææÉ×ŌÓÉæŲÖĘ£¬¼ÓČČ×°ÖĆŗĶ¹Ģ¶Ø×°ÖĆŹ”ĀŌ£©”£

µŚ1²½£ŗ·“Ó¦²¢ŹÕ¼ÆÉś³ÉµÄĘųĢå£ŗ
¢ŁŹµŃéÖŠĘųĢå·¢Éś×°ÖĆӦєŌńÄÄÖÖ×°ÖĆ¼°ĄķÓÉŹĒ ”£
¢Ś×°ÖƵÄĮ¬½ÓĖ³ŠņŹĒ(Ģīø÷×°ÖĆ½ÓæŚµÄŠņŗÅ)£ŗ[ ]”ś[ ] [ ]”ś[8] [9]”ś[ ]”£
¢Ū¼ģ²é×°ÖĆĘųĆÜŠŌŗó£¬æŖŹ¼·“Ó¦”£“żEÖŠ³äĀśŗģ×ŲÉ«ĘųĢ壬Ķ£Ö¹ŹµŃ锣
µŚ2²½£ŗŃéÖ¤EÖŠÓŠNO”£
¢Ü Č”ĻĀŹŌ¹ÜE£¬µ¹Į¢ŌŚFÖŠ£¬ĒįĒįŅ”¶ÆŹŌ¹Ü”£
Č·ČĻÉś³ÉµÄĘųĢåÖŠÓŠNOµÄĻÖĻóŹĒ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2011-2012ѧğ°²»ÕŹ”»ĘɽŹŠøßČżĘߊ£ĮŖæ¼»ÆѧŹŌ¾ķ ĢāŠĶ£ŗĢīæÕĢā
£Ø14·Ö£©ĻĀĶ¼ŹĒø÷ÖÖ²»Ķ¬ĆܶȵÄĻõĖįÓėĢś·“Ó¦(ĻąĶ¬ĪĀ¶Č)Ź±Ö÷ŅŖ»¹Ō²śĪļµÄ·Ö²¼Ķ¼”£ĒėČĻÕę¶ĮĶ¼·ÖĪö£¬»Ų“šÓŠ¹ŲĪŹĢā”£

¢ÅĻĀĮŠŠšŹöÖŠÕżČ·µÄŹĒ(ĢīŠņŗÅ) ”£
A£®Ķ¼ÖŠŗį×ų±źŹĒĻõĖįµÄĆÜ¶Č£¬ĻõĖįµÄĆܶČŌ½“ó£¬ĘäÅضČŌ½“ó”£
B£®µ±»¹Ō¼ĮŗĶĪĀ¶ČĻąĶ¬Ź±£¬²»Ķ¬ÅØ¶ČµÄĻõĖį±»»¹ŌµÄ²śĪļ²»ŹĒµ„Ņ»µÄ£¬Ö»ŹĒŌŚÄ³ÅØ¶ČŹ±£¬ŅŌijÖÖ²śĪļĪŖÖ÷¶ųŅŃ”£
C£®ĻõĖįµÄÅضČŌ½“󣬻¹Ō²śĪļÖŠNŌŖĖŲµĶ»ÆŗĻ¼Ū²śĪļŌ½¶ą”£
D£®µ±ĻõĖįĆܶȓóÓŚ1.3 g”¤cm-3Ź±£¬»¹Ō²śĪļÖ÷ŅŖĪŖNO”¢NO2
¢Ę µ±ĻõĖįČÜŅŗµÄĆܶČĪŖ1.36 g”¤cm-3Ź±£¬ĻĀĮŠ»Æѧ·½³ĢŹ½ÖŠ£¬ÄܽĻ×¼Č·±ķ“ļFeÓė¹żĮæĻõĖį·“Ó¦µÄŹĒ(ĢīŠņŗÅ£© ”£
A£®2Fe + 10HNO3 == 2Fe(NO3)3 + NO”ü£«3NO2”ü£«5H2O
B£®4Fe + 18HNO3 == 4Fe(NO3)3 + 3NO”ü£«3NO2”ü£«9H2O
C£®3Fe + 12HNO3 == 2Fe(NO3)3 + Fe(NO3)2 + 2NO”ü£«2NO2”ü£«3H2O
¢Ē ĆܶČĪŖ1.26 g”¤cm-3£¬ÖŹĮæ·ÖŹżĪŖ50.0 %µÄĻõĖį£¬ĘäĪļÖŹµÄĮæÅØ¶ČŹĒ mol”¤L-1”£
¢Č ĻŽÓĆĻĀĮŠŅĒĘ÷”¢Ņ©Ę·ŃéÖ¤ÓÉĢśŗĶ¹żĮæ1.36 g”¤cm-3ĻõĖį·“Ó¦²śÉśµÄĘųĢåÖŠŗ¬ÓŠNO(²»æ¼ĀĒN2O4)”£Éč¼ĘŅ»øöŗĻĄķ¶ų¼ņµ„µÄŹµŃé·½°ø£ØŅĒĘ÷æÉŃ”ŌńŹ¹ÓĆ£¬N2µÄÓĆĮææÉ×ŌÓÉæŲÖĘ£¬¼ÓČČ×°ÖĆŗĶ¹Ģ¶Ø×°ÖĆŹ”ĀŌ£©”£

µŚ1²½£ŗ·“Ó¦²¢ŹÕ¼ÆÉś³ÉµÄĘųĢå£ŗ
¢ŁŹµŃéÖŠĘųĢå·¢Éś×°ÖĆӦєŌń (Ģī×°ÖĆŠņŗÅ)£¬ĄķÓÉŹĒ ”£
¢Ś×°ÖƵÄĮ¬½ÓĖ³ŠņŹĒ(Ģīø÷×°ÖĆ½ÓæŚµÄŠņŗÅ)£ŗ[ ]”ś[ ] [ ]”ś[8] [9]”ś[ ]”£
¢Ū¼ģ²é×°ÖĆĘųĆÜŠŌŗó£¬æŖŹ¼·“Ó¦”£“żEÖŠ³äĀśŗģ×ŲÉ«ĘųĢ壬Ķ£Ö¹ŹµŃ锣
µŚ2²½£ŗŃéÖ¤EÖŠÓŠNO”£
¢Ü Č”ĻĀŹŌ¹ÜE£¬µ¹Į¢ŌŚFÖŠ£¬ĒįĒįŅ”¶ÆŹŌ¹Ü”£
Č·ČĻÉś³ÉµÄĘųĢåÖŠÓŠNOµÄĻÖĻóŹĒ ”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com