
在BaSO4饱和溶液中,加入Na2SO4(s),达到平衡时( )
A.[Ba2+]=[SO42-]
B.[Ba2+]=[SO42-]=[Ksp (BaSO4)]1/2
C.[Ba2+]≠[SO42-],[Ba2+]·[SO42-]=Ksp (BaSO4)
D.[Ba2+]≠[SO42-],[Ba2+]·[SO42-]≠Ksp (BaSO4)
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
如图是某同学鉴别NH4HCO3、NH4Cl、KCl三种化肥的过程,其中试剂甲和乙分别可能是( )
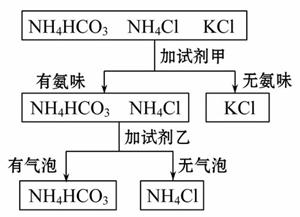
A.甲:熟石灰;乙:稀盐酸
B.甲:水;乙:氢氧化钠溶液
C.甲:氯化钠溶液;乙:稀硫酸
D.甲:稀盐酸;乙:氯化钠溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法错误的是( )。
A.油脂属于酯类物质,能发生水解反应
B.卤代烃在一定条件下能与NaOH水溶液发生反应
C.甲苯能使酸性KMnO4溶液褪色
D.棉花和蚕丝的主要成分都是纤维素
查看答案和解析>>
科目:高中化学 来源: 题型:
2013年10月,三位美国化学家因为给复杂化学体系设计了多尺度模型而荣获诺贝尔化学奖。下列模型由C、H、O中的两种或三种原子构成,有关说法错误的是( )
| 编号 | 1 | 2 | 3 | 4 |
| 模型示意图 |
|
|
|
|
A.模型1对应物质的二氯代物有2种
B.模型2对应物质的官能团是羧基
C.模型2对应物质可与模型3对应的物质发生酯化反应
D.模型4对应物质可以与氯气发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
已知常温下,AgCl的Ksp=1.8×10-10 mol2·L-2,AgBr的Ksp=4.9×
10-13 mol2·L-2。
(1)现向AgCl的悬浊液中:
①加入AgNO3固体,则Cl-的浓度________(填“变大”“变小”或“不变”,下同);
②若改加更多的AgCl固体,则[Ag+]__________;
③若改加更多的KBr固体,则[Ag+]_________,[Cl-]_________。
(2)有关难溶盐的溶度积及溶解度有以下叙述,其中正确的是_______。
A.将难溶电解质放入纯水中,溶解达到平衡时,升高温度,Ksp一定增大
B.两种难溶盐电解质,其中Ksp小的溶解度也一定小
C.难溶盐电解质的Ksp与温度有关
D.向AgCl的悬浊液中加入适量的水,使AgCl再次达到溶解平衡,AgCl的Ksp不变,其溶解度也不变
查看答案和解析>>
科目:高中化学 来源: 题型:
一种常用的泡沫灭火器构造如图。内筒a是玻璃瓶,外筒b是钢瓶,平时泡沫灭火器内筒外筒盛有液态试剂,当遇火警时,将灭火器取下倒置,内外筒液体试剂立即混合产生大量CO2泡沫灭火,从液态试剂在灭火器中长久放置和快速灭火两个角度分析,盛放药品正确的是( )

A.a中盛饱和Na2CO3溶液,b中盛Al2(SO4)3溶液
B.a中盛饱和NaHCO3溶液,b中盛Al2(SO4)3溶液
C.a中盛Al2(SO4)3溶液,b中盛饱和Na2C O3溶液
O3溶液
D.a中盛Al2(SO4)3溶液,b中盛饱和NaHCO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各项叙述中,正确的是( )
A.电子层序数越大,s原子轨道的半径越大,形状发生明显的变化
B.在同一电子层上运动的电子,其自旋方向肯定不同
C.电负性的大小可以作为判断金属性和非金属性强弱的尺度
D.原子最外层电子排布是5s1的元素,其氢氧化物不能使氢氧化铝溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
化合物Ⅳ为一种重要化工中间体,其合成方法如下:

(1)化合物Ⅰ的化学式为________;化合物Ⅳ除了含有—Br还有的官能团是________(填名称)。
(2)化合物Ⅱ具有卤代烃的性质,在一定条件下能生成烯,该反应条件是________。
(3)1 mol化合物Ⅲ与足量NaOH反应消耗NaOH的物质的量为________ mol。
(4)化合物Ⅳ能发生酯化反应生成六元环化合物Ⅴ,写出该反应的化学方程式:__________________________________________。
(5)根据题给化合物转化关系及相关条件,请你推出 (2-甲基-1,3-丁二烯)发生类似①的反应,得到有机物Ⅵ和Ⅶ,结构简式分别是________、________,它们物质的量之比是________。
(2-甲基-1,3-丁二烯)发生类似①的反应,得到有机物Ⅵ和Ⅶ,结构简式分别是________、________,它们物质的量之比是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com