
【题目】下列五种烃①2-甲基丁烷 ②2,2-二甲基丙烷 ③正戊烷 ④丙烷 ⑤丁烷,按沸点由高到低的顺序排列的是
A. ①>②>③>④>⑤ B. ②>③>⑤>④>①
C. ③>①>②>⑤>④ D. ④>⑤>②>①>③
 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案科目:高中化学 来源: 题型:
【题目】高分子材料PET聚酯树脂和PMMA的合成路线如下图:
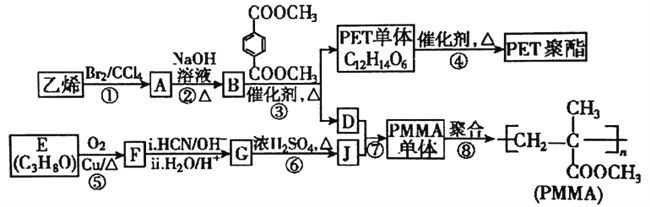
已知:
I.RCOOR+R "OH![]() RCOOR "+ROH (R.R'、R"代表烃基)
RCOOR "+ROH (R.R'、R"代表烃基)
II.  (R代表烃基)。
(R代表烃基)。
(1)PMMA单体的结构简式为_______,PET单体中的官能团名称为________。
(2)反应⑤的反应类型是________;反应②的化学方程式为_________。
(3)若反应④得到的某一条链状产物聚合度为n,则缩聚反应中脱去的小分子有(___)个。
(4)PMMA单体有多种同分异构体,某种异构体K具有如下性质:①不能发生银镜反应②不能使溴水褪色③分子内没有环状结构④核磁共振氢谱有面积比为3:1的两种峰,则K的结构简式为:__________;另一种异构体H含有醛基、羟基和碳碳双键,在铜催化下氧化,官能团种类会减少一种,则H合理的结构共有___种(不考虑立体异构和空间异构)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学方程式或离子方程式正确的是( )
A.用铜做电极电解CuSO4溶液:2Cu2++2H2O=2Cu↓+O2↑+4H+
B.惰性电极电解MgCl2溶液:2Cl﹣+2H2O ![]() 2OH﹣+Cl2↑+H2↑
2OH﹣+Cl2↑+H2↑
C.乙醛溶液中加入新制碱性Cu(OH)2悬浊液并加热CH3CHO+2 Cu(OH)2+OH﹣ ![]() CH3COO﹣+Cu2O↓+3H2O
CH3COO﹣+Cu2O↓+3H2O
D.硝酸银溶液中滴加过量氨水:Ag++NH3H2O═AgOH↓+NH4+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2015年2月美国研究人员将CO和O附着在一种钌催化剂表面,用激光脉冲将其加热到2000K,成功观察到CO与O形成化学键生成CO2的全过程.下列说法正确的是( ) 
A.CO、CO2均属于酸性氧化物
B.形成化学键时需吸收能量
C.钌催化剂可以改变该反应的焓变
D.CO与O形成化学键过程中有电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.向氨水通入足量SO2:SO2+2NH3H2O═2NH4++SO32﹣+H2O
B.将Ba(OH)2溶液滴入NaHSO4溶液中至SO42﹣恰好完全沉淀:Ba2++SO42﹣+2OH﹣+2H+═BaSO4↓+2H20
C.向醋酸溶液中滴加过量NaOH溶液:H++OH﹣═H2O
D.向新制Cu(OH)2悬浊液中加入乙醛溶液并加热:CH3CHO+2Cu(OH)2+OH﹣ ![]() CH3COO﹣+Cu2O↓+3H2O
CH3COO﹣+Cu2O↓+3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语的书写,正确的是( )
A. 硫原子的结构示意图: ![]() B. 二氧化碳的结构式:
B. 二氧化碳的结构式:![]()
C. 乙烯的结构简式:CH2CH2 D. 丙烷分子的球棍模型:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】芳香酯I的合成路线如下:
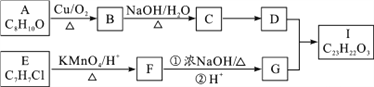
已知以下信息:
①A~I均为芳香族化合物,B能发生银镜反应,D的相对分子质量比C大4,E的苯环上的一溴代物有两种。
②![]()
③
请回答下列问题:
(1)A→B的反应类型为________,D所含官能团的名称为________,E的名称为________。
(2)E→F与F→G的顺序能否颠倒________(填“能”或“否”),理由________。
(3)B与银氨溶液反应的化学方程式为______________________________________________________。
(4)I的结构简式为_____________________________。
(5)符合下列要求A的同分异构体还有________种。
①与Na反应并产生H2 ②芳香族化合物
(6)根据已有知识并结合相关信息,写出以CH3CH2OH为原料制备CH3CH2CH2CH2OH的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:_____________________
CH3CH2Br![]() CH3CH2OH
CH3CH2OH![]() CH3COOCH2CH3
CH3COOCH2CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修 3:物质结构与性质]
(1) 过渡金属元素铁能形成多种配合物,如:[Fe (CN) 6] 4-、[Fe(SCN)6]3-等。
Fe3+的核外电子排布式为______________,从原子结构的角度解释Fe3+比Fe2+稳定的理由是_______________。
(2) N的基态原子中能量最高的电子,其电子云在空间有________个方向,原子轨道呈________形。
(3) (NH4)2SO4阴离子的立体构型是________,NH4+中心原子的杂化类型是________。
(4) Fe有δ、γ、α三种同素异形体,其晶胞结构如下图所示:

① δ、α两种晶体晶胞中铁原子的配位数之比为_____________。
②1个γ晶体晶胞中所含有的铁原子数为_____________。
③若Fe原子半径为rpm,NA表示阿伏加德罗常数的值,则δ-Fe单质的密度为____________g/cm3(列出算式即可)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com