
【题目】化学与生产、生活密切相关,下列说法不正确的是![]()
A.酸雨样品露天放置一段时间,酸性增强,是因为发生了氧化还原反应
B.纳米铁粉可将地下水中的![]() 转化为
转化为![]() ,是因为纳米铁粉具有还原性
,是因为纳米铁粉具有还原性
C.将草木灰与![]() 混合施用,可更好为植物全面提供N、P、K三种营养元素
混合施用,可更好为植物全面提供N、P、K三种营养元素
D.生活中常用可溶性铝盐净水,可加速水中悬浮物沉降
 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案科目:高中化学 来源: 题型:
【题目】硫代硫酸钠(Na2S2O3)可以除去自来水中的氯气,在水产养殖上被广泛应用。用纯碱和硫化碱(主要成分Na2S,含少量Na2SO4、Na2CO3等)为原料制备Na2S2O3·5H2O的实验流程如下:

回答下列问题:
(1)试剂X是一种二元化合物的钡盐,它与Na2SO4反应的化学方程式为___________________。
(2)用热水溶解并趁热过滤的目的是______________________。
(3)利用SO2与Na2CO3、Na2S的混合溶液反应制备Na2S2O3,所需仪器如下图:
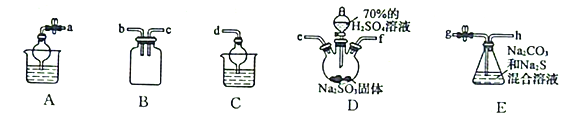
①从左到右连接各仪器,导管的接口顺序为:___________接e、f接___________、___________接___________、___________接d。___________
②E中发生反应的离子方程式为______________________。
③装置B的作用是______________________。
(4)操作1包括蒸发浓缩、______________________、___________、洗涤、干燥
(5)为测定产品Na2S2O3·5H2O的纯度,准确称取12.4gNa2S2O3·5H2O产品,配制成100mL溶液,取25.00mL溶液,以淀粉溶液作指示剂,用0.2500mol·L-1碘的标准溶液滴定,发生反应2S2O32-+I2= S4O62-+2I-,消耗碘的标准溶液20.00mL,则该产品的纯度为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.按系统命名法![]() 的名称为2一甲基一3,5一二乙基己烷
的名称为2一甲基一3,5一二乙基己烷
B.用Na2CO3溶液能区分CH3COOH、CH3CH2OH、苯、硝基苯四种物质
C.等质量的甲烷、乙烯、1,3一丁二烯分别充分燃烧,所耗氧气的量依次增加
D.下列物质的沸点按由低到高顺序为:(CH3CH2)2CH2<(CH3)3CH<CH3(CH2)3CH3<(CH3)2CHCH2CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.激素类药物乙烯雌酚的结构简式为: ,它的分子式是:C18H20O2
,它的分子式是:C18H20O2
B.等质量的甲烷、乙烯、乙醇分别充分燃烧,所耗用氧气的量依次减少
C.聚乳酸(![]() )是由单体之间通过加聚反应合成的
)是由单体之间通过加聚反应合成的
D.实验证实![]() 可使溴的四氯化碳溶液褪色,说明该分子中存在碳碳双键
可使溴的四氯化碳溶液褪色,说明该分子中存在碳碳双键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备溴苯可用如图所示装置。

填空:
(1)关闭G夹,打开C夹,向装有少量苯的三颈烧瓶的A口加适量溴,再加入少量铁屑,塞住A口,三颈烧瓶中发生反应的有机反应方程式为___。
(2)E试管内出现的现象为___。
(3)F装置的作用是___。
(4)待三颈烧瓶中的反应进行到仍有气泡冒出时松开G夹,关闭C夹,可以看到的现象是___。
(5)反应结束后,拆开装置,从A口加入适量的NaOH溶液,然后将液体倒入__中(填仪器名称),振荡静置,从该仪器__口将纯净溴苯放出(填“上”或“下”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是( )
A. 图甲表示可逆反应A(g)+2B(g)2C(g),速率随外界条件的改变曲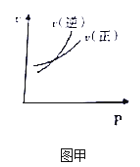
B. 图乙表示CH3COOH溶液中通入NH3至过量的过程中溶液导电性的变化
C. 图丙表示用0.1mol/L NaOH溶液滴定20.00mL 0.1mol/LCH3COOH溶液得到的滴定曲线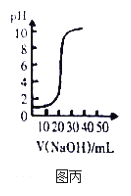
D. 图丁表示等量NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应:2NO2(g)N2O4(g)相同时间后测得NO2含量的曲线,则该反应的△H<0 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X 、Y 和Z 在周期表中的相对位置如表所示,这四种元素原子的最外层电子数之和为21。回答下列问题:
W | X | |||
Y | Z |
(1) X在元素周期表中的位置为_______;画出X的简单离子结构示意图_______。
已知X元素的一种原子,其中子数为10,写出这种原子的原子符号_____________。
(2)四种元素简单离子的半径由大到小为_____________(用离子符号表达)。
(3)W、X的最简单氢化物稳定性为_______>________(填化学式)。
(4)Z最高价氧化物的水化物与Y最高价氧化物对应水化物反应的化学方程式为______ 。
(5)ZX2气体是一种广谱杀菌消毒剂。工业上可利用NaZX3和NaZ 在酸性条件下制得ZX2 同时得到Z元素的单质,该反应的离子方程式为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知醋酸达到电离平衡后,改变某条件电离平衡向正反应方向移动,则下列说法正确的是
A.实现该变化的只能是升高温度B.溶液的导电能力一定变强
C.溶液的pH一定减小D.发生电离的分子总数增多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ/mol。回答有关中和反应的问题。
(1)用0.1molBa(OH)2配成稀溶液与足量稀硝酸反应,能放出___kJ热量。
(2)如图装置中仪器A的名称___,作用是___;仪器B的名称___,作用是___;碎泡沫塑料的作用是___。

(3)若通过实验测定中和热的ΔH,其结果常常大于-57.3kJ/mol,其原因可能是___。
(4)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得中和热的数值会___(填“偏大”、“偏小”或“无影响”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com