
����Ŀ����ͼ��Ԫ�����ڱ���һ���֣�A��B��C��D��E��X�����ڱ�����Ԫ����ɵij������ʻ�� 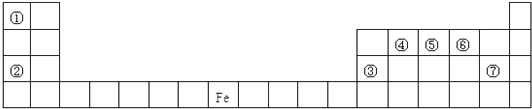
��֪A��B��C��D��E��X������ͼ��ʾת����ϵ������������ͷ�Ӧ������ȥ��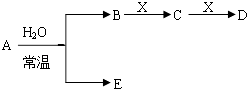
��1����EΪ�������A��ˮ��Ӧ�Ļ�ѧ����ʽΪ �� �ٵ�X�Ǽ�������Һ��C��������22������ʱ����ʾX�ʼ��Ե����ӷ���ʽΪ �ڵ�XΪ��������ʱ����X��B��ϡ��Һ��Ӧ����C�����ӷ�Ӧ����ʽΪ
��2����EΪ�������壬DΪ��ɫ������A�Ļ�ѧʽ������ ��
���𰸡�
��1��3NO2+H2O�T2HNO3+NO��![]() +H2O?
+H2O? ![]() +
+ ![]() ��Fe+4H++
��Fe+4H++ ![]() �TFe3++NO��+2H2O
�TFe3++NO��+2H2O
��2��Na��Na2O2��NaH
���������⣺����Ԫ�������ڱ��е�λ�ÿ��ж�Ԫ�ص����࣬��ΪHԪ�أ���ΪNaԪ�أ���ΪAlԪ�أ���ΪCԪ�أ���ΪNԪ�أ���ΪOԪ�أ���ΪClԪ�أ���1�����ݱ��е�Ԫ�ؿ�֪��ֻ�Т��γɵ�������ˮ��Ӧ����NO������ϣ���AΪNO2 �� A��ˮ��Ӧ���������һ���������䷴ӦΪ3NO2+H2O�T2HNO3+NO����������̼���η�Ӧ���ɶ�����̼����������6+8��2=22�����ӣ�XΪ̼���Σ�ˮ���Լ��ԣ�ˮ�����ӷ�ӦΪCO32��+H2OHCO3��+OH�� �� �ڵ�XΪ����ʱ��ӦΪ��۽���Fe��X��B��ϡ��Һ��Ӧ����C�����ӷ���ʽΪFe+4H++NO3���TFe3++NO��+2H2O�����Դ��ǣ�3NO2+H2O�T2HNO3+NO��CO32��+H2OHCO3��+OH����Fe+4H++NO3���TFe3++NO��+2H2O����2�����ݱ��е�Ԫ�ؿ�֪��ֻ�Т��γɵ�������ˮ��Ӧ����������BΪNaOH��DΪAl��OH��3 �� ��A����ΪNa��Na2O2��NaH�����Դ��ǣ�Na��Na2O2��NaH��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ������ȤС��Ϊ̽��ͭ��Ũ����ķ�Ӧ������������ͼ��ʾװ�ý����й�ʵ�飺 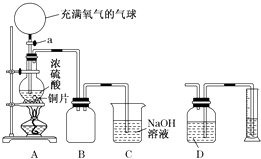
��1���ȹرջ���a����6.4gͭƬ��10mL 18mol/L��Ũ�������Բ����ƿ�й�������Ӧ��ɣ�������ƿ�л���ͭƬʣ�࣮�ٴ���a���������е�������������Բ����ƿ�����ͭƬ��ȫ��ʧ�� ��д������������Բ����ƿ�ڷ�����Ӧ�Ļ�ѧ����ʽ��
����a֮ǰ��
����a֮�� ��
��B�������ռ�ʵ���в����������װ�ã�������ƿ�ڵĵ���δ��ȫ����ֱ����ͼ�ϰѵ��ܲ���������
��2��ʵ���ϣ��ڴ���a֮ǰ��������ʣ�࣮Ϊ�����ⶨ��������ʵ������ס�����ѧ��������������ƣ� �ټ�ѧ����Ƶķ����ǣ��Ȳⶨͭ��Ũ���ᷴӦ����SO2��������ͨ������ȷ����������ʵ��������ⶨSO2�ķ����ǽ�װ��A���������建��ͨ��װ��D���Ӷ����װ��A��������������������ɱ�״���£�������Ϊ��ѧ����Ƶ�ʵ�鷽����Dװ���е��Լ�Ϊ���ѧʽ����
����ѧ����Ƶķ����ǣ�����Ӧ�����Һ��ȴ��ȫ�����뵽�ձ���ϡ�ͣ�������ȷ��������100mL��Һ����ȡ20mL����ƿ�У�����ָʾ�����ñ�����������Һ���еζ�[��֪��Cu��OH��2��ʼ������pHԼΪ5]��ѡ���ָʾ��������Ϊ���������������ʵ���������ȥa mol/L����������Һb mL����ԭ��������ʵ���Ϊmol���ú�a��b�ı���ʽ����ʾ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ֶ�����Ԫ�������ڱ��е����λ��������ʾ������EԪ��ԭ�Ӻ��������������������������3��������Ԫ�����ڱ���������Ԫ�����ʣ���ش�

��1��������Ԫ�ص��⻯���У����ȶ�����___________��(д��ѧʽ)��
��2��AF2�ĽṹʽΪ_____________��
��3����һ�������£���B������H2��Ӧ����1 molG����ʱ���ų�������Ϊ46.2 kJ��д���÷�Ӧ���Ȼ�ѧ����ʽ��_____________________��
��4����ҵ����G�������������Ĺܵ��Ƿ�©�����ɹ۲쵽�������̣�ͬʱ�е���B���ɣ�д����ѧ����ʽ__________________________���÷�Ӧ�б�������G����뷴Ӧ��G������֮��__________��
��5��F�ĵ��ʿ��������������⻯�ﷴӦ���ɣ�д���÷�Ӧ�Ļ�ѧ����ʽ��__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ϊ�������������;���ɲ�ȡ�Ĵ�ʩ�ǣ�������
������ú��ȼ�ϣ��ڰѹ����̴���ߣ���ȼ�����������ữ�������м�ʯ�ң��ݿ����µ���Դ��
A.�ڢ�
B.�ڢۢܢ�
C.�٢ۢ�
D.�٢ۢܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Դ�������������ᷢչ�Ļ������о���ѧ��Ӧ�е������仯�������ڸ��õ����û�ѧ��ӦΪ�������������
��1�����飨SiH4����һ����ɫ���壬���������ܷ�����ը����ȼ��
�� ���飨SiH4����̬ʱ����___________���塣
�� ��֪������1 g������ȼ����SiO2��Һ̬ˮ�ų�����44.6 kJ�������Ȼ�ѧ����ʽΪ______________________��
��2���״�ȼ�ϵ�ص��ܷ�ӦΪ��2CH3OH+3O2�T2CO2��+4H2O���乤��ԭ������ͼ��ʾ��
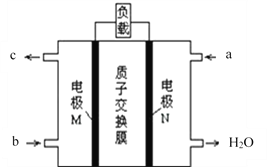
��ͼ��CH3OH��_____________����a��b��ͨ�룬�õ�ص�������____________����M��N���缫��������N�������ĵ缫��Ӧʽ��_____________________��
����������·����1mol����ת�ƣ������ı�״����O2�����Ϊ_______L��
��3��25�棬101kPa�����£�14g N2��3g H2��Ӧ����NH3�������仯����ͼ��ʾ��
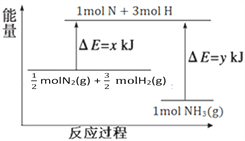
��֪���� x = 1127��
�� 25�� 101kPa�£�N2(g)+3H2(g)![]() 2NH3(g)��H=��92kJ��mol��1��
2NH3(g)��H=��92kJ��mol��1��
�� y =__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ����̼��������̼�����þ���ʮ����Ҫ�����壬��ѧ��������¼������룺
��.������̼�������ڴ��������¿���ȡ��̼ϩ������һ�����ܱ������зֱ�Ͷ��1molCO2��3molH2��������Ӧ��2CO2(g)+6H2(g)![]() C2H4(g)+4H2O(g) ��H���ڲ�ͬ�¶��£��ô��м������ƽ��ʱH2�����ʵ����仯��ϵ��ͼ��ʾ��
C2H4(g)+4H2O(g) ��H���ڲ�ͬ�¶��£��ô��м������ƽ��ʱH2�����ʵ����仯��ϵ��ͼ��ʾ��
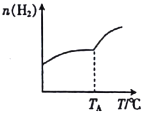
��1�������������䣬��ʼʱ����1molCO2��2molH2����Ͷ�ϣ���CO2��ת���ʽ�____________(����� ��С�����䡱)��
��2����H____________ (�>����<������ȷ����)0��
��3������������ϵ���������������Խ��ͼʾ�ƶ����ȶ��ԣ�C2H4_______(�>�� ��<������ȷ����)H2O��
��.�״�����Ҫ�Ļ���ԭ�ϣ��ֿ���Ϊȼ�ϣ���ҵ�Ͽ�����CO��CO2������ȼ�ϼ״�����֪�Ʊ��״����йط�Ӧ�Ļ�ѧ����ʽ�Լ��ڲ�ͬ�¶��µĻ�ѧƽ�ⳣ�����±���ʾ��
��ѧ��Ӧ |
| 500 | 700 | 800 |
��2H2(g)+CO(g) | K1 | 2.5 | 0.34 | 0.15 |
��H2(g)+CO2(g) | K2 | 1.0 | 1. 70 | 2.52 |
��3H2(g)+CO2 (g) | K3 |
��ش��������⣺
��4�����ݷ�Ӧ�Ƚϡ�H1__________(�>���� <����ȷ����)��H2��
��5��500��ʱ��÷�Ӧ����ijʱ��H2(g)��CO2
��6�����д�ʩ��ʹ��Ӧ�۵�ƽ����ϵ��![]() �������___________(����ĸ)��
�������___________(����ĸ)��
A.��H2O(g)����ϵ�з����ȥ B.����He(g)��ʹ��ϵѹǿ����
C.�����¶� D.�ٳ���1molH2
��.��7���������뽫CO�����з�Ӧ��ȥ:2CO(g)=2C(s)+O2(g)����������������ܷ�ʵ��?_______________(��ܡ����ܡ�)��������__________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ֶ�����Ԫ��A��B��C��D��E��ԭ��������������A��Cͬ�壬B��Dͬ�壬C�ļ����Ӻ�B�ļ����Ӿ�����ͬ�ĵ��Ӳ�ṹ��A��B��D��E�����γɹ����ͻ����A��B�γɵĻ�������ˮ�гʼ��ԣ�C��E�γɵĻ��������������ӵĸ�����Ϊ1:1�������жϳ���Ԫ�ؼ���Ӧ��ѧʽ�ش����⣺
(1)����Ԫ���У���������ǿ����_______(��Ԫ������)���ǽ�������ǿ��Ԫ����_____(��Ԫ������)��
(2)��Ԫ��A�ֱ��Ԫ��B��D��E���γɵĹ����ͻ������У����ȶ���������________________________________________(�û�ѧʽ��ʾ)��
(3)Ԫ��A��E�γɵĻ�������Ԫ��A��B�γɵĻ����ﷴӦ������ĵ���ʽΪ____________�����д��ڵĻ�ѧ������Ϊ_________________________��
(4)E���ӵĽṹʾ��ͼ��_______________������E��ˮ��Ӧ�����ӷ���ʽΪ_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������¾���ͬ�Ļ�ѧ��Ӧ������ʵ��ͼʾ�仯��AΪ��ʽ�Σ�BΪ��ɫ��ζ���壻��ɫ����D��ʹ��ɫʯ����ֽ������X��F��YΪ���嵥�ʣ���YΪ��ɫ���壬FΪ��������Ҫ�ɷ�֮һ��GΪ���Σ�G����ɫ����M����Һ�пɷ�Ӧ����B����Ӧ���dz�����ҵԭ���� 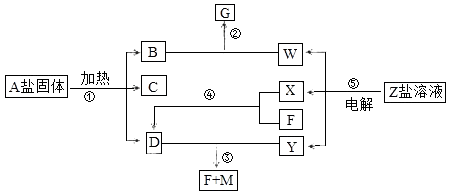
��1��д���������ʵĻ�ѧʽ��A��Y
��2��д����Ӧ�ڵ����ӷ���ʽ ��
��3��д����Ӧ�۵Ļ�ѧ����ʽ ��
��4��������pH=10�������Ϊ100mL��D��W����Һ��M��Ӧ�����ĵ�M�����ʵ�����ϵDW������ڡ���С�ڡ����ڡ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪A��B��C��DΪ������Ԫ�ع��ɵ��������ʣ�����������ת����ϵ��DΪǿ�����(����������ʿ���ʡ��)������˵������ȷ���ǣ� ��
![]()
A. ��AΪ�ǽ������ʣ�������Mg��Ӧ�IJ��������������Ӹ����ȿ���Ϊ2��3
B. ��AΪ�ǽ������ʣ��������Ԫ�������ڱ��е�λ�ÿ��ܴ��ڵ�2���ڢ�A��
C. ����AΪ���ʻ��ǻ����D���п�����ͬһ�����ʣ������ʵ�Ũ��Һ�ڳ����¶���ʹ�����������ۻ�
D. ��A�ǹ��ۻ����0.1molA�����к��еĵ���������ΪNA(NAΪ�����ӵ�������ֵ)
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com