
| A. | Ca2+ | B. | SO32- | C. | SiO32- | D. | Fe2+ |
分析 A.钙离子不与三种离子反应,能够共存;
B.亚硫酸根离子与钡离子反应,且硝酸根离子在酸性条件下能够氧化亚硫酸根离子;
C.硅酸根离子与氢离子、钡离子反应;
D.硝酸根离子在酸性条件下具有强氧化性,能够氧化亚铁离子.
解答 解:A.Ca2+不与H+、NO3-、Ba2+反应,在溶液中不能大量共存,故A正确;
B.SO32-与H+、Ba2+反应,酸性条件下NO3-能够氧化SO32-,在溶液中不能大量共存,故B错误;
C.SiO32-与H+、Ba2+反应,在溶液中不能大量共存,故C错误;
D.H+、NO3-具有强氧化性,能够氧化Fe2+,在溶液中不能大量共存,故D错误;
故选A.
点评 本题考查离子共存的正误判断,为高考的高频题,题目难度不大,注意掌握离子反应发生条件,明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;试题侧重对学生基础知识的训练和检验,有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.


科目:高中化学 来源: 题型:选择题
| A. | 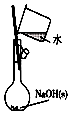 用于配制0.10 mol•L-1 NaOH溶液;评价:正确 | |
| B. |  用于测定中和热;评价:错误,装置中缺少了环形玻璃搅拌棒 | |
| C. | 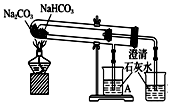 用于比较Na2CO3、NaHCO3的热稳定性;评价:正确 | |
| D. | 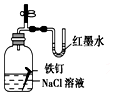 证明铁发生吸氧腐蚀时空气参加反应;评价:正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升高温度能加快反应②的化学反应速率,提高CH3OCH3产率 | |
| B. | 反应③使用催化剂,△H3减少 | |
| C. | 反应 3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g)的△H=-246.lkJ•mol-1 | |
| D. | 反应③对反应②无影响 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHSeO4溶液和Na2SeO4溶液均显碱性 | |
| B. | pH=3的H2SeO4和NaHSeO4溶液,后者水的电离程度大 | |
| C. | H2SeO4溶液中滴加少量氨水的离子方程式:H++NH3•H2O=NH4++H2O | |
| D. | Na2CO3溶液中加入少量H2SeO4的离子方程式为:CO32-+H+=HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
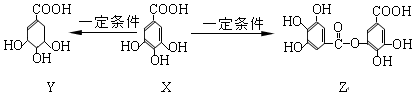
| A. | 1molZ最多能与7molNaOH发生反应 | |
| B. | 1molX最多能与2molBr2发生取代反应 | |
| C. | Y分子结构中有3个手性碳原子 | |
| D. | Y能发生加成、取代、消去、氧化、缩聚反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
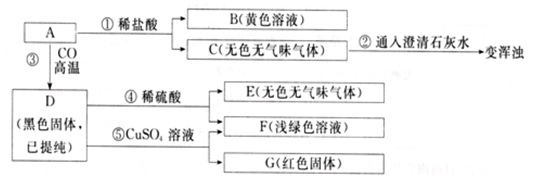
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 镀铜铁制品镀层破损后,铁制品比破损前更容易生锈 | |
| B. | 室温下向1LpH=2的醋酸溶液中加水,所得溶液中H+数目减少,酸性减弱 | |
| C. | 水的离子积常数KW随着温度的升高而增大,说明水的电离是放热反应 | |
| D. | Na2CO3溶液中加入少量Ca(OH)2固体,CO32-水解程度减小,溶液的pH值减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com