
【题目】精炼铜工业中阳极泥的综合利用具有重要意义。一种从铜阳极泥(主要含有铜、银、金、少量的镍)中分离提取多种金属元素的工艺流程如下:
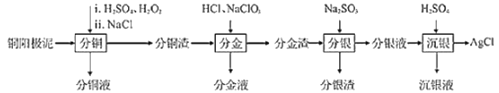
已知:ⅰ.分金液中含金离子主要成分为[AuCl4]-;分金渣的主要成分为AgCl;
ⅱ.分银液中含银离子主要成分为[Ag(SO3)2]3-,且存在[Ag(SO3)2]3-Ag++2SO32-
ⅲ.“分铜”时各元素的浸出率如表所示。

(1)由表中数据可知,Ni的金属性比Cu______。分铜渣中银元素的存在形式为(用化学用语表示)______。
(2)“分金”时,单质金发生反应的离子方程式为______。
(3)Na2SO3溶液中含硫微粒物质的量分数与pH的关系如图所示。
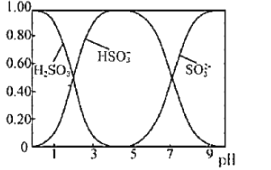
“沉银”时,需加入硫酸调节溶液的pH=4,分析能够析出AgCl的原因为______。调节溶液的pH不能过低,理由为______(用离子方程式表示)。
(4)工业上,用镍为阳极,电解0.1mol/L NiCl2溶液与一定量NH4Cl组成的混合溶液,可得高纯度的球形超细镍粉。当其他条件一定时,NH4Cl的浓度对阴极电流效率及镍的成粉率的影响如图所示:
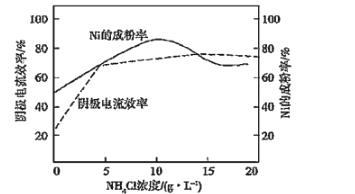
为获得高纯度的球形超细镍粉,NH4Cl溶液的浓度最好控制为______g/L,当NH4Cl溶液的浓度大于15g/L时,阴极有无色无味气体生成,导致阴极电流效率降低,该气体为______。
【答案】强 AgCl 2Au+ClO3-+7Cl-+6H+=2[AuCl4]-+3H2O H2SO4电离出的H+降低了SO32-的浓度,促使[Ag(SO3)2]3-Ag++2SO32-平衡正向移动,电离出Ag+,Ag+与分银液中的Cl-反应生成AgCl 避免产生污染气体SO2 10 H2
【解析】
由流程可知,铜阳极泥加入硫酸、过氧化氢和氯化钠分铜,“分铜”时,单质铜发生反应是铜在酸性溶液中被过氧化氢氧化生成硫酸铜和水,“分铜”时加人足量的NaCl的主要作用为使溶解出的Ag+形成AgCl进入分铜渣,加入盐酸和氯酸钠分金,分金液的主要成分为[AuCl4]-,“分金”时,单质金发生反应是金和加入的氯酸钠和盐酸发生氧化还原反应生成[AuCl4]-,分金渣加入亚硫酸钠过滤得到分银液中主要成分为[Ag(SO3)2]3-,且存在[Ag(SO3)2]3-Ag++2SO32-加入硫酸沉银,促使[Ag(SO3)2]3-Ag++2SO32-平衡正向移动,电离出Ag+,Ag+与分银液中的Cl-反应生成AgCl,以此解答该题。
(1)由表中数据可知,Ni的浸出率大,则Ni的金属性比Cu强,分铜渣中银元素的存在形式为AgCl;
故答案为:强;AgCl;
(2)分金液的主要成分为[AuCl4]-,“分金”时,单质金发生反应是金和加入的氯酸钠和盐酸发生氧化还原反应生成[AuCl4]-,反应的离子方程式为2Au+ClO3-+7Cl-+6H+=2[AuCl4]-+3H2O;
故答案为:2Au+ClO3-+7Cl-+6H+=2[AuCl4]-+3H2O;
(3)分银液中主要成分为[Ag(SO3)2]3-,且存在[Ag(SO3)2]3-Ag++2SO32-,H2SO4电离出的H+降低了SO32-的浓度,平衡正向进行,能够析出AgCl的原因为:H2SO4电离出的H+降低了SO32-的浓度,促使[Ag(SO3)2]3-Ag++2SO32-平衡正向移动,电离出Ag+,Ag+与分银液中的Cl-反应生成AgCl,调节溶液的pH不能过低理由为:避免产生污染气体SO2;
故答案为:H2SO4电离出的H+降低了SO32-的浓度,促使[Ag(SO3)2]3-Ag++2SO32-平衡正向移动,电离出Ag+,Ag+与分银液中的Cl-反应生成AgCl;避免产生污染气体SO2;
(4)根据图2可知,NH4Cl的浓度为10g![]() L-1时,镍的成粉率最高,所以NH4Cl的浓度最好控制为10g
L-1时,镍的成粉率最高,所以NH4Cl的浓度最好控制为10g![]() L-1,当NH4Cl浓度大于15g
L-1,当NH4Cl浓度大于15g![]() L-1时,阴极有气体生成,阴极发生还原反应,溶液中铵根离子水解溶液呈酸性,阴极电极反应式为2H++2e-=H2↑或2NH4++2H2O+2e-=2NH3
L-1时,阴极有气体生成,阴极发生还原反应,溶液中铵根离子水解溶液呈酸性,阴极电极反应式为2H++2e-=H2↑或2NH4++2H2O+2e-=2NH3![]() H2O+H2↑,阴极生成的气体为H2;
H2O+H2↑,阴极生成的气体为H2;
故答案为:10;H2。


科目:高中化学 来源: 题型:
【题目】分枝酸可用于生化研究。其结构简式如图。下列关于分枝酸的叙述正确的是

A. 分子中含有2种官能团
B. 可与乙醇、乙酸反应,且反应类型相同
C. 1mol分枝酸最多可与3molNaOH发生中和反应
D. 可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用所学化学知识,分析并回答下列各小题。
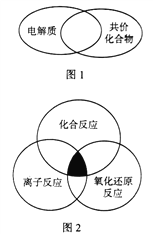
(1)下列物质属于图1所示化学概念交叉部分的有______(填标号)。
a.氨气 b.硝酸 c.乙醇 d.醋酸钠
(2)下列各反应属于图2中阴影部分所示关系的有_______(填标号)。
a.氨气与浓硝酸
b.氢气与氧气
c.氯气与氯化亚铁溶液
d.铜与氯化铁溶液
(3)下列有关说法正确的是_____(填标号)。
a.核电站把核能转化为电能
b.常温下铜与浓硫酸发生钝化。反应很快停止
c.海水中提取化学物质均涉及到氧化还原反应
d.电解法得到某元素单质,则该元素可能被还原,也可能被氧化
(4)下列各实验过程中,需要检查所用某些仪器是否漏水的有_______(填标号)。
a.氢气还原氧化铜
b.水与煤油混合物分离
c.氯化钠溶液与泥沙分离
d.配制100mL 10mol·L-1碳酸钠溶液
(5)下列关于试剂保存的叙述正确的是_________(填标号)。
a.氢氟酸保存在玻璃瓶中
b.KOH溶液保存在带玻璃塞的细口瓶中
c.溴水保存在带橡胶塞的棕色瓶中
d.KMnO4与乙醇不能放在同一药品厨中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学课外兴趣小组学生在实验室里制取的乙烯中常混有少量的二氧化硫,老师启发他们并由他们自己设计了下列实验图以确认上述混合气体中有C2H4和SO2,回答下列问题:

(1)装置应盛放的试剂是I ____,IV _______(将下列有关试剂的序号填入空格内);
A.品红溶液 B.NaOH溶液 C.浓硫酸 D.酸性KMnO4溶液
(2)能说明SO2气体存在的现象是____________________________;
(3)使用装置II的目的是____________________________________ ;
(4)使用装置III的目的是 ___________________________________;
(5)确定含有乙烯的现象是___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Q、W、X、Y、Z是5种短周期元素,原子序数逐渐增大,Q与W组成的化合物是一 种温室气体,W与Y、X与Y组成的化合物是机动车排出的大气污染物,Y和Z能形成原子个数比为1:1和1:2的两种离子化合物。
(1)W在元素周期表中的位置是______。
(2)2.24L(标准状况)XQ3被200mL 1mol/L QXY3溶液吸收后,所得溶液中离子浓度从大到小的顺序是______。
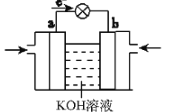
(3)WQ4Y与Y2的反应可将化学能转化为电能,其工作原理如图所示,a极的电极反应式是______。
(4)已知:W(s)+Y2(g)═WY2(g)△H=-393.5kJ/mol WY(g)+ ![]() Y2(g)═WY2(g)△H=-283.0kJ/mol24g W与一定量的Y2反应,放出热量362.5kJ,所得产物的物质的量之比是______。
Y2(g)═WY2(g)△H=-283.0kJ/mol24g W与一定量的Y2反应,放出热量362.5kJ,所得产物的物质的量之比是______。
(5)X和Z组成的一种离子化合物,能与水反应生成两种碱,该反应的化学方程式是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)请用序号填空:
①13C与14C ②正丁烷与异丁烷
③CH3CH3与CH3CH2CH3 ④![]()
属于同位素的是______;属于同系物的是______;属于同分异构体的是______。
(2)写出下列物质的电子式:
NaCl____________ NH3______________
(3)第三周期元素中的最高价氧化物对应的水化物中,酸性最强的是______,碱性最强的是___________,呈两性的氢氧化物是___________。半径最大的原子是___________,氢化物最稳定的元素是__________。
(4)1molN2(g)与适量O2(g)反应生成NO(g),需吸收68kJ的热量,写出该反应的热化学方程式______________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电能是现代社会应用最广泛的能源之一。
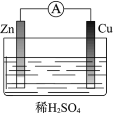
(1)某原电池装置如图所示。其中,Zn电极为原电池的______极(填“正”或“负”),电极反应式是______。Cu电极上发生的反应属于______(填“氧化”或“还原”)反应。电子由______极流出(Zn或Cu),电解质溶液中SO![]() 移向______(Zn或Cu)。
移向______(Zn或Cu)。
(2)下列反应通过原电池装置,可实现化学能直接转化为电能的是______(填序号)。
①CaO+H2O=Ca(OH)2
②2H2+O2 =2H2O
③2FeCl3+Cu=CuCl2+2FeCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 是一种重金属离子,有一环境监测小组欲利用
是一种重金属离子,有一环境监测小组欲利用![]() 、
、![]() 、
、![]() 、NaOH等试剂测定某工厂废水中
、NaOH等试剂测定某工厂废水中![]() 的浓度。
的浓度。
(1)现需配制![]() 标准NaOH溶液,所需要的玻璃仪器除量筒、
标准NaOH溶液,所需要的玻璃仪器除量筒、![]() 容量瓶、玻璃棒外,还需要______、_____。
容量瓶、玻璃棒外,还需要______、_____。
(2)需准确称取NaOH固体的质量为______![]() 。
。
(3)在配置以上溶液时,下列操作会使所配溶液浓度偏低的是____(多选题)。
![]() .容量瓶洗涤干净后未干燥
.容量瓶洗涤干净后未干燥 ![]() .定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水
.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水
![]() .定容时俯视刻度线
.定容时俯视刻度线 ![]() .烧杯和玻璃棒未洗涤
.烧杯和玻璃棒未洗涤
(4)从对化合物分类方法出发,指出下列各组物质中与其他物质类型不同的一种物质.
![]() .
.![]() 、
、![]() 、
、![]() 、
、![]() ________;
________;
![]() .
.![]() 、
、![]() 、
、![]() 、
、![]() ________;
________;
![]() .
.![]() 、
、![]() 、
、、
![]() ________;
________;
![]() .
.![]() 、
、![]() 、
、![]() 、
、![]() ________。
________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关共价键键参数的的比较中,不正确的是( )
A. 键能:C—N < C=N < C≡N
B. 键长:I—I > Br—Br > Cl—Cl
C. 分子中的键角:H2O > NH3
D. 乙烯分子中碳碳键的键能:σ键 > π键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com