
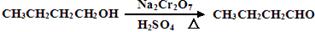 。反应物和产物的相关数据列表如下:
。反应物和产物的相关数据列表如下:| | 沸点/℃ | 密度/g·cm-3 | 水中溶解性 |
| 正丁醇 | 117.2 | 0.8109 | 微溶 |
| 正丁醛 | 75.7 | 0.8017 | 微溶 |
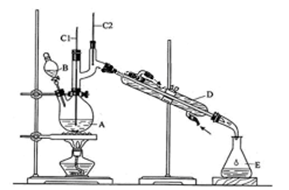


科目:高中化学 来源:不详 题型:单选题
| A.检验某溶液中是否含有SO42-,通常是先向试液中滴加BaCl2溶液,然后再滴加稀盐酸 |
| B.向某溶液中滴加稀氢氧化钠溶液,若未嗅到氨的气味,则说明该溶液中无铵盐 |
| C.某白色固体与强酸溶液接触产生大量无色气体,则该固体一定是碳酸钙 |
| D.检验某溶液中是否含有Fe3+,通常是向试液中滴加KSCN溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题

| 物质 | K2CO3 | KHCO3 | K2SO4 | CH3COOK |
| 293K溶解度(g) | 111 | 33.7 | 11.1 | 217 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
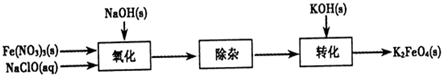
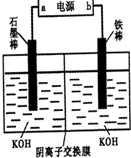
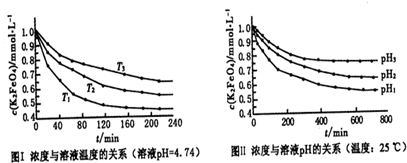
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 试管编号 | 1 | 2 | 3 |
| 加入的药品和数量 | 4 mL蒸馏水 | 4 mL 蒸馏水 +3滴浓H2SO4 | 4 mL 蒸馏水 +3滴NaOH浓溶液 |
| 3滴甲基橙试剂 2 mL乙酸乙酯 | 3滴甲基橙试剂 2 mL乙酸乙酯 | 3滴石蕊溶液 2 mL乙酸乙酯 |
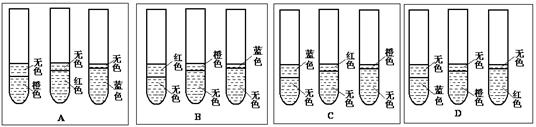
| 试管编号 | 1 | 2 | 3 |
| 加入的药品和数量 | 4 mL饱和食盐水 | 4 mL饱和食盐水 +3滴浓H2SO4 | 4 mL饱和食盐水 +3滴NaOH浓溶液 |
| 3滴甲基橙试剂 2 mL乙酸乙酯 | 3滴甲基橙试剂 2 mL乙酸乙酯 | 3滴石蕊溶液 2 mL乙酸乙酯 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
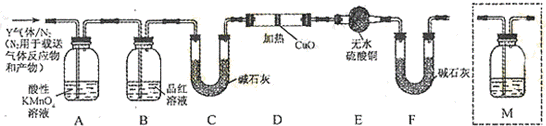
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
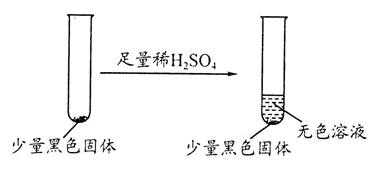
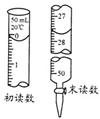
 3Na2S2O3+CO2。设计如下装置(夹持仪器省略)进行实验。
3Na2S2O3+CO2。设计如下装置(夹持仪器省略)进行实验。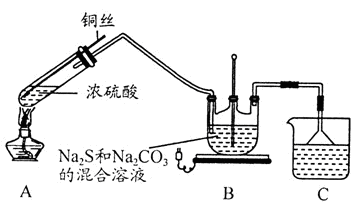

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.加热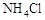 晶体时,将湿润的红色石蕊试纸靠近试管口,检验 晶体时,将湿润的红色石蕊试纸靠近试管口,检验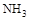 的生成 的生成 |
B.向某溶液中加入足量盐酸酸化,无现象,再加人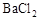 溶液,有白色沉淀生成,说明原溶液中存在 溶液,有白色沉淀生成,说明原溶液中存在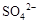 |
| C.酸碱中和滴定实验中用到的玻璃仪器仅有酸式滴定管、碱式滴定管和烧杯 |
D.用量筒量取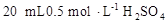 溶液于烧杯中,加水80mL,,配制成0.1 溶液于烧杯中,加水80mL,,配制成0.1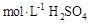 溶液 溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
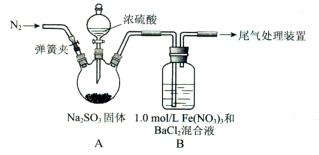
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com