
可用于鉴别以下三种化合物的一组试剂是
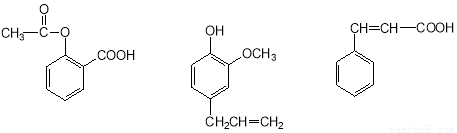
乙酰水杨酸 丁香酚 肉桂酸
① 银氨溶液 ② 溴的四氯化碳溶液 ③ 氯化铁溶液 ④ 氢氧化钠溶液
A.②与③ B.③与④ C.①与④ D.①与②
 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案科目:高中化学 来源:2016届辽宁沈阳市高三上学期期中考试化学试卷(解析版) 题型:填空题
已知M、Q、X、Y、Z是前四周期中元素(不包含稀有气体元素),有关性质和相关信息如下表:
元素 | 相关信息 |
M | 最高价氧化物对应的水化物能按1:1电离出电子数相等的阴、阳离子 |
Q | 所在主族序数与所在周期序数之差为4,非金属性在同周期元素中最强 |
X | 其单质为淡黄色晶体 |
Y | 某种核素原子的质量数为56,中子数为30 |
Z | X元素的单质在Z元素的单质中燃烧,发出明亮的蓝紫色火焰 |
(1)下图是不完整的元素周期表,补全元素周期表的轮廓,并将Y的元素符号填在元素周期表中相应的位置上。
(2)M与Z形成的含有共价键的化合物的电子式为 。
(3)M、Q、Z简单离子的半径由大到小的顺序为 (用离子符号表示)。
(4)用一个化学方程式表示证明非金属性Q>X: 。
(5)5.6L标准状况下的X的简单氢化物在足量的Z单质中完全燃烧生成液态水时,放出的热量为356.8kJ。该反应的热化学方程式为 。
(6)在碱性条件下,Q的单质可与YZ2-反应制备一种可用于净水的盐YZ42-,该反应的离子方程式为。
查看答案和解析>>
科目:高中化学 来源:2016届甘肃省高三12月月考化学试卷(解析版) 题型:实验题
现有铁、碳两种元素组成的合金,某实验小组为了研究该合金的性质并测定该合金中碳的质量分数,设计了如下实验方案和实验装置
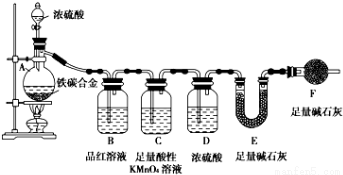
I.探究该合金的某些性质:
(1)取a g合金粉末放人蒸馏烧瓶,并加入足量浓H2SO4,A、B中均无明显现象,原因是_______;
(2)点燃酒精灯一段时间后,A中剧烈反应,请写出此时合金中成分铁的化学反应方程式_____;
(3)反应一段时间后,将C中所吸收的气体通入以下溶液中,判断能否产生沉淀,若不能则写“否”,若能则写出相应的沉淀成分:氯水和氯化钡溶液____,氨水和氯化钡溶液_____;
II.测定样品中碳的质量分数:
(4)装置F的作用__________________________________________________________;
(5)若将SO 2气体通入含有n molNa2S的溶液中,溶液中出现黄色浑浊,试分析该溶液最多能吸收SO2气体_____________mol。
2气体通入含有n molNa2S的溶液中,溶液中出现黄色浑浊,试分析该溶液最多能吸收SO2气体_____________mol。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年青海西宁第十四中学高二上期中考试化学卷(解析版) 题型:填空题
室温下将pH=13的强碱溶液和pH=2的强酸溶液混合,所得溶液的pH=12,则强碱溶液和强酸溶液的体积之比为 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏石嘴山第三中学高二上期中考试化学卷(解析版) 题型:推断题
有机物A是常用的食用油抗氧化剂,分子式为C10H12O5,可发生如下转化:
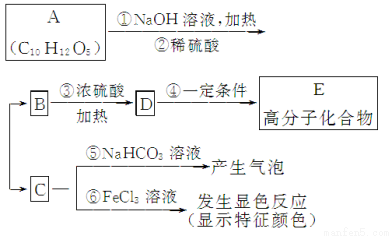
已知B的相对分子质量为60,分子中只含一个甲基。C的结构可表示为

请回答下列问题:
(1)根据系统命名法,B的名称为__________。
(2)官能团—X的名称为____________,高聚物E的链节为________。
(3)A的结构简式为______________。
(4)反应⑤的化学方程式为________________________________________________。
(5)C有多种同分异构体,写出其中2种符合下列要求的同分异构体的结构简式_______________。
Ⅰ.含有苯环 Ⅱ.能发生银镜反应 Ⅲ.不能发生水解反应
(6)从分子结构上看,A具有抗氧化作用的主要原因是_________________(填序号)。
a.含有苯环 b.含有羰基 c.含有酚羟基
查看答案和解析>>
科目:高中化学 来源:2016届辽宁抚顺第一中学高三上第一次模拟考试化学试卷(解析版) 题型:填空题
(1)下列有关说法正确的是_____________。
A.用pH试纸测得新制氯水的pH为4
B.碳酸钠和硫酸钡可按溶解、过滤、蒸发的操作顺序分离
C.除去C2H5OH中的CH3COOH,先加足量的氢氧化钠溶液,再分液
D.溶液中滴加盐酸酸化的BaCl2溶液出现白色沉淀,则该溶液中一定存在SO42-
E.将乙醇与浓硫酸共热制得的气体通入酸性KMnO4溶液中,检验气体中是否含有乙烯
F.用铂丝灼烧白色粉末,火焰成黄色,证明原粉末中有Na+,没有K+
G.金属氧化物不一定是碱性氧化物,但碱性氧化物一定是金属氧化物;非金属氧化物不一定是酸性氧化物,酸性氧化物也不一定是非金属氧化物
H.在两个容积相同的容器中,一盛有HCl气体,另一个盛有H2和Cl2的混合气体,在同温同压下,两容器内的气体一定具有相同的原子数
I.实验室配制1mol/L盐酸250mL,需要的仪器只有:250mL容量瓶、胶头滴管、量筒和烧杯
J.在MH4Al(SO4)2(一种复盐)的溶液中加入Ba(OH)2溶液至沉淀的质量达到最大时:
Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O
K.硝酸钡溶液中通入足量的SO2:2SO2+2NO3-+3Ba2++2H2O=3BaSO4↓+2NO↑+4H+
(2)ClO2的制备方法比较实用的有数十种,下列是几种常见的方法.
①方法一:2NaClO3+4HCl(浓)═2NaCl+Cl2↑+2ClO2↑+2H2O
对于该反应,下列说法中正确的是___________。
A.该反应中Cl2是氧化产物
B.该反应中NaCl、ClO2是还原产物
C.在反应中HCl既作氧化剂又具有酸的作用
D.1mol NaClO3参加反应时,有1mol电子发生转移
E.1mol NaClO3参加反应,理论上能得到33.6L气体
方法二:氯化钠电解法
该法工艺原理如图。
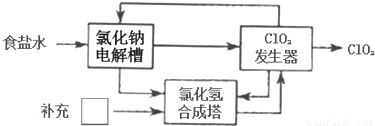
②其过程是将食盐水在特定条件下电解得到的氯酸钠(NaClO3)与盐酸反应生成ClO2。指出工艺中方框中物质为______(填化学式),理由为______________。
③将NCl3与NaClO2(亚氯酸钠)按物质的量之比1:6混合,在碱性溶液中恰好反应生成ClO2,试写出该反应的离子方程式____________。
查看答案和解析>>
科目:高中化学 来源:2016届内蒙古包头第九中学高三上期中考试理综化学试卷(解析版) 题型:填空题
第VA族元素及其化合物在生产、生活中有着广泛的应用
(1)砷的电子排布式为 ,N、P、As三种元素的最常见氢化物沸点由高到低的顺序为 ,高纯度砷可用于生产半导体材料GaAs,在GaAs晶体中,Ga、As原子最外电子层均达到8电子稳定结构,则GaAs晶体中砷的配位数为 。
(2)对硝基苯酚水合物是一种具有特殊功能的物质,其结构简式为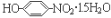 。该物质中几种元素的第一电离能由大到小的顺序是 ,该物质的晶体中肯定不存在的作用力是 。
。该物质中几种元素的第一电离能由大到小的顺序是 ,该物质的晶体中肯定不存在的作用力是 。
a.氢键 b.极性键 c.范德华力 d.离子键 e.σ键
(3)科学家将NaNO3和Na2O在一定条件下反应得到一种白色晶体,已知其中阴离子与SO42-互为等电子体,则该阴离子的化学式是 。
(4)PM2. 5富含大量的有毒、有害物质,易引发二次光化学烟雾污染,光化学烟雾中含有NOx、O3、CH2=CHCHO、HCOOH、CH3COOONO2 (PAN)等二次污染物。
①N2O结构式可表示为N=N=O,N2O中氮原子的杂化轨道类型为 ,1 mol PAN中含σ键数目为 。
②测定大气中PM2.5的浓度方法之一是β-射线吸收法,β-射线放射源可用85 Kr。Kr晶体为面心立方晶体,若晶体中与每个Kr原子相紧邻的Kr原子有m个,晶胞中含Kr原子为n个,则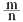 = (填数字)。已知Kr晶体的密度为ρg/cm3 ,摩尔质量为Mg/mol,阿伏伽德罗常数用NA表示,列式表示Kr晶胞参数a = nm。
= (填数字)。已知Kr晶体的密度为ρg/cm3 ,摩尔质量为Mg/mol,阿伏伽德罗常数用NA表示,列式表示Kr晶胞参数a = nm。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年陕西西安第一中学高二上期中考试化学试卷(解析版) 题型:填空题
在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力I随加入水的体积V变化的由线如图所示。请回答:
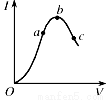
(1)“O”点导电能力为O的理由是 。
(2)a,b,c三点溶液中 c(H+)由小到大的顺序为 。
(3)a,b,c三点中电离程度最大的是 。
(4)使C点溶液中C(CH3COO-)增大,溶液c(H+)减小,可采取的
措施是:① ② ③  (至少填两个空)
(至少填两个空)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北衡水冀州中学高一上月考三理化学卷(解析版) 题型:选择题
某学生取某物质溶于水,制得无色透明溶液,进行以下实验:①与碱反应生成盐和水;②与铁反应生成氢气;③该溶液中阳离子只有H+。根据你学过的酸的概念,其中能说明该物质为酸类物质的是: ( )
A.①②③ B.①② C.②③ D.③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com