
【题目】关于化合物![]() 说法错误的是( )
说法错误的是( )
A. 1mol该化合在一定条件下加氢最多可消耗5mol H2
B. 该化合物最多有15个原子共面
C. 该化合物是乙炔的同系物
D. 该化合物与![]() 互为同分异构体
互为同分异构体
科目:高中化学 来源: 题型:
【题目】现有A、B、C、D、E、F六种位于周期表前四周期的元素,其原子序数依次增大,相关信息如下表所示:
元素 | 性质 |
A | 一种核素的原子核内不含中子 |
B | 原子核外电子有6种不同运动状态 |
C | 最高价氧化物的水化物与其氢化物可生成盐 |
D | 单质之一为淡蓝色气体,可阻挡对人体有害的紫外线 |
E | 周期表中位于短周期,基态原子M层成对电子数是未成对电子数的2倍 |
F | 该元素的一种氧化物可用作油漆颜料,与某单质反应可应用于焊接钢轨 |
根据以上信息,回答下列问题:
(1)F元素位于周期表的____区(填s、p、d、ds或f),B、C、D三种元素的第一电离能由大到小顺序为______________________(用元素符号表示)。
(2)ED2中E原子的杂化类型为__________________;ED2易溶于水的原因可能是___________(填序号)。
①ED2与水极性相同 ②ED2可以与水反应 ③ED2可以与水形成氢键
(3)F元素的一种氯化物常温下为固体,熔点282℃,沸点315℃,在300℃以上易升华,易溶于水,也易溶于乙醚、丙酮等有机溶剂,据此判断该氯化物晶体为________晶体。
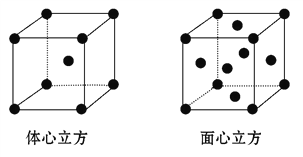
(4)F的单质晶体在不同温度下有两种堆积方式(晶胞结构如图所示),面心立方晶胞和体心立方晶胞中实际含有的F原子个数之比为________,其中体心立方晶胞空间利用率为___________(设F原子半径是r,列出含r的计算表达式,不需化简)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应N2+3H2![]() 2NH3是工业上合成氨的重要反应。
2NH3是工业上合成氨的重要反应。
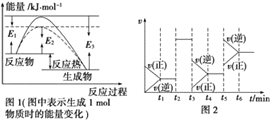
(1)根据图1请写出合成氨的热化学方程式__________________(热量用El、E2或E3表示)。
(2)图1中虚线部分是通过改变化学反应中的_________条件,该条件的改变与图2中哪一时刻条件的改变相同_________(用“t1……t6”表示)。
(3)图2中t3时刻改变的条件是_________,t5与时刻改变的条件是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家积极探索新技术对CO2进行综合利用。
Ⅰ.CO2可用FeO吸收获得H2。
i. 6FeO(s)+CO2(g)=2Fe3O4(s)+C(s) △Hl=-76.0 kJ·mol-1
ⅱ. C(s)+2H2O(g)=CO2(g)+2H2(g) △H2= +113.4 kJ·mol-1
(1)3FeO(s)+H2O(g)=Fe3O4(s)+H2(g) △H3=_________。
(2)在反应i中,每放出38.0 kJ热量,有______gFeO被氧化。
Ⅱ.CO2可用来生产燃料甲醇。
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1。在体积为1L的恒容密闭容器中,充入1 mol CO2和3 mol H2,一定条件下发生反应:测得CO2和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1。在体积为1L的恒容密闭容器中,充入1 mol CO2和3 mol H2,一定条件下发生反应:测得CO2和CH3OH(g)的浓度随时间变化如图所示。
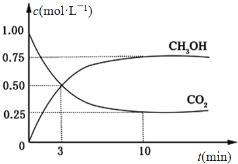
(3)从反应开始到平衡,氢气的平均反应速率v(H2)=___________________ mol·(L·min) -1。
(4)氢气的转化率=________________________。
(5)该反应的平衡常数为__________________________ (保留小数点后2位)。
(6)下列措施中能使平衡体系中n(CH3OH)/n(CO2)增大的是_____________________。
A.升高温度 B.充入He(g),使体系压强增大
C.再充入1 mol H2 D.将H2O(g)从体系中分离出去
(7)当反应达到平衡时,H2的物质的量浓度为c1,然后向容器中再加入一定量H2,待反应再一次达到平衡后,H2的物质的量浓度为c2,则c1________c2的关系(填“>”、“<”或“=”)。
III.CO2可用碱溶液吸收获得相应的原料。
利用100 mL 3 mol·L—1NaOH溶液吸收4.48 LCO2(标准状况),得到吸收液。
(8)该吸收液中离子浓度的大小排序为___________________。将该吸收液蒸干,灼烧至恒重,所得固体的成分是_________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】事物是相互影响、相互制约的。在有机化合物分子中,这种相互影响、相互制约同样存在。例如:
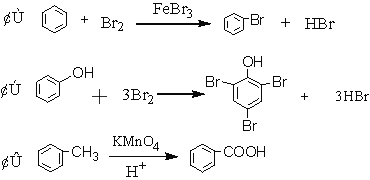
下列性质不能说明基团之间相互影响的是( )
A. ②用浓溴水而①用液溴;①需用催化剂而②不需用。
B. ②生成三溴取代产物而①只生成一溴取代产物。
C. CH3CH2OH无明显酸性,而![]() 显弱酸性。
显弱酸性。
D. 乙醇能使酸性高锰酸钾溶液褪色,而苯酚不能。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在100mL 稀HNO3和稀H2SO4组成的混合溶液中,两种酸的物质的量浓度之和为0.4mol/L.向该溶液中加入足量的铜粉后加热,充分反应后,所得溶液中Cu2+的物质的量浓度最大值为(反应前后溶液体积变化忽略不计)
A. 0.15mol/L B. 0.24mol/L C. 0.30mol/L D. 0.36mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】观察下图,下列叙述正确的是
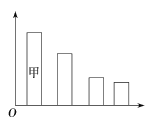
A. 若该图表示的是活细胞的各化学元素的含量,则甲应该为碳元素
B. 若该图表示的是细胞的各化学元素占干重的百分比,则甲应该为氧元素
C. 若该图为活细胞的化合物组成情况,则甲中含有的元素为C、H、0
D. 若该图是已经完全脱水后的细胞的化合物组成情况,则甲是蛋白质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了测定某铜银合金的组成,将30.0g合金溶于80.0mL 13.5mol·L1的浓HNO3中。待合金完全溶解后,收集到气体6.72L(标准状况下)并测得H+浓度为1mol·L1。假设反应后溶液的体积为80.0mL,试计算:
(1)被还原的硝酸的物质的量___________;
(2)合金中银的质量分数___________。
(3)确定6.72L气体中各成分的物质的量___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com