
【题目】铜板上铁铆钉长期暴露在潮湿的空气中,形成一层酸性水膜后铁铆钉会被腐蚀,示意图如下。下列说法不正确的是

A. 腐蚀过程中铜极上始终只发生: 2H++2e-= H2↑
B. 若水膜中溶有食盐将加快铁铆钉的腐蚀
C. 若在金属表面涂一层油脂能防止铁铆钉被腐蚀
D. 若将该铜板与直流负极相连,则铁铜均难被腐蚀
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案科目:高中化学 来源: 题型:
【题目】云南特色小吃“过桥米线”做法如下:先用滚沸的鸡汤一碗,上罩浮油,再辅以切得极薄的生肉片、乌龟片、火腿片、葱头等,最后把主料米线放入拌食即成。“过桥米线”汤鲜、肉嫩、料香、米线滑润,吃起来别有一番风味。以下有关“过桥米线”的说法不正确的是( )
A.上层浮油沸点较高,难以挥发
B.浮油对下层汤水起到很好的“液封”作用,使下层汤水及热量难以外逸
C.去掉上面的一层浮油,将减弱“过桥米线”的保温效果
D.上层浮油高温水解即产生美味的物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是 ( )
A. 澄清石灰水可用来鉴别Na2CO3和NaHCO3溶液
B. 能使湿润的碘化钾淀粉试纸变蓝的物质不一定是氯气
C. 常温下浓硝酸和稀硝酸均可用铁质容器盛装
D. 浓硫酸有氧化性,稀硫酸没有氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】被称为人体冷冻学之父的罗伯特·埃廷格在1962年写出《不朽的前景》一书。他在书中列举了大量事实,证明了冷冻复活的可能。比如,许多昆虫和低等生物冬天都冻僵起来,春天又自动复活。下列结论中与上述信息相关的是( )
A.化学反应前后质量守恒B.低温下分子无法运动
C.温度降低,化学反应停止D.温度越低,化学反应越慢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列措施不能使产生氢气的速率加快的是
A. 用锌片替换铁片与稀硫酸反应
B. 将铁片与稀硫酸反应的温度升高
C. 用铁粉替换铁片与稀硫酸反应
D. 用浓硫酸替换稀硫酸与铁片反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二水氯化钡晶体(BaCl22H2O)在工业上主要用于制造各种钡盐、颜料和有机染料,某研究小组以重晶石(主要成分 BaSO4)制备BaCl22H2O 流程如下图。
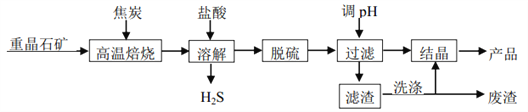
(1)已知:
① BaSO4(s)+ 4C(s)= 4CO(g) + BaS(s) △H1 = 571.2kJmol﹣1
② C(s)+ CO2(g)= 2CO(g) △H2 = 172.5 kJmol﹣1
反应 BaSO4(s)+ 2C(s)= 2CO2(g)+ BaS(s)的△H = _____ kJmol﹣1
(2)高温焙烧须加入过量的炭,同时还要通入空气,其目的是_____、_____。
(3)脱硫过程中分为两步, 第一步是物理脱硫, 第二步是化学脱硫。
① 物理脱硫是直接用蒸汽升温,并用空气“爆气法”除去的物质是_____。
② 下列物质不宜用作脱硫剂的是_____ (填字母)。
A. 高锰酸钾 B. 次氯酸钠 C. 双氧水 D.氯气
(4)上述流程中洗涤滤渣的主要目的是_____。
(5)溶解时产生的 H2S 可用 80~85 ℃时的石灰氮料浆(CaCN2的浆水混合物)吸收并制得更有价值的产品——硫脲[CS(NH2)2]和熟石灰。请写出制备硫脲的化学方程式_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 碱金属的单质中,锂的还原性最强
B. 第ⅠA族元素比第ⅡA族元素的金属性强
C. 随核电荷数递增,第三周期元素的氧化物对应的水化物酸性逐渐增强
D. 随着核电荷数的递增,卤族元素的气态氢化物的稳定性逐渐减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据表中信息,判断下列叙述中正确的是( )
序号 | 氧化剂 | 还原剂 | 其他反应物 | 氧化产物 | 还原产物 |
① | Cl2 | FeBr2 | / | Fe3+、Br2 | |
② | KClO3 | 浓盐酸 | / | Cl2 | |
③ | KMnO4 | H2O2 | H2SO4 | O2 | Mn2+ |
A. 由表中①组的信息可知通入Cl2的量不同,氧化产物可能不同
B. 反应①中,当只有少量Cl2时,反应可表示为Cl2+ Fe2+===Fe3++ 2Cl-
C. 表中②组反应的还原产物是KCl,电子转移数目是6e-
D. 表中③组反应的离子方程式为2MnO![]() + 3H2O2+6H+===2Mn2++ 4O2↑+ 6H2O
+ 3H2O2+6H+===2Mn2++ 4O2↑+ 6H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com