
| A. | 常温下,铝和铂都不能与浓硝酸发生反应 | |
| B. | 氯气和硫酸铁都可以用于处理生活用水 | |
| C. | 加热I2和NH4Cl晶体,最后都无固体残留 | |
| D. | SO2气体和Na2SO3溶液都能使溴水褪色 |
分析 A.依据常温下铝与浓硝酸钝化,铂性质稳定解答;
B.氯气与水那样生成次氯酸具有强氧化性,能够杀菌消毒,硫酸铁中铁水解生成氢氧化铁胶体,具有吸附性;
C.加热碘升华,加热氯化铵,固体受热分解生成氨气和氯化氢;
D.二氧化硫、亚硫酸钠都具有还原性,能够还原溴水;
解答 解:A.常温下铝与铂都与浓硝酸不反应,原因分别是铝与浓硝酸钝化,铂性质稳定,原理不同,故A不选;
B.氯气能够用于自来水的杀菌消毒,硫酸铁用于处理自来水可以吸附水中固体杂质颗粒,二者原理不同,故B不选;
C.加热碘升华,加热氯化铵,固体受热分解生成氨气和氯化氢,前者是物理变化,后者是化学变化,二者原理不同,故C不选;
D.SO2气体和Na2SO3溶液都能使溴水褪色,二氧化硫、亚硫酸都体现还原性,故D选;
故选:D.
点评 本题考查了元素化合物知识,明确物质的性质是解本题关键,注意盐类水解的应用,题目难度不大.


 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 漂白粉、氨水和液氯都属于混合物 | |
| B. | 稀硝酸可除去试管内壁的银镜 | |
| C. | Fe(OH)3胶体无色、透明,能产生丁达尔现象 | |
| D. | SiO2既能和NaOH溶液反应又能和氢氟酸反应,所以是两性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| B | C |
| D |
| A. | 简单离子的半径大小关系:B>C>E | |
| B. | D元素的气态氢化物比C元素的气态氢化物稳定 | |
| C. | 由A、B、C三种元素组成的离子化合物中,阴、阳离子个数比为1:1 | |
| D. | A、D、E均可形成两种常见氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2XO3 | B. | HXO3 | C. | H3XO4 | D. | H2XO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH、KOH、CsOH碱性依次增强 | |
| B. | Li、Na、K、Rb、Cs单质的失电子能力逐渐增强 | |
| C. | Al、Mg、Na的原子半径依次减小 | |
| D. | Li、Na、K、Rb、Cs原子半径依次增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子序数d>c>b>a | B. | 离子半径C2->D->B+>A2+ | ||
| C. | 原子半径A>B>C>D | D. | 非金属性:C>D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 化学键 | C-H | C-C | C=C | H-H |
| 键能/kJ•mol?1 | 412 | 348 | 612 | 436 |
 的反应热为( )
的反应热为( )| A. | +124 kJ/mol | B. | +246 kJ/mol | C. | +368 kJ/mol | D. | +429 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 少量SO2通入CaCl2溶液能生成白色沉淀 | |
| B. | 可以用澄清石灰水鉴别SO2和CO2 | |
| C. | 硫粉在过量的纯氧中燃烧可以生成SO3 | |
| D. | SO2能使FeCl3、KMnO4水溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
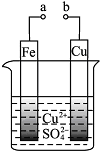
| A. | 构成原电池时,电子流动方向是:从铁片流出,经过溶液,流到铜片,再回流到铁片,形成电流 | |
| B. | 构成原电池时溶液中SO42-离子移向Cu片 | |
| C. | 要使Fe片不被腐蚀,可将铜片换成锌片或将铁片直接接直流电源正极 | |
| D. | 要在铁片上镀一层薄薄的铜,在Cu片上反应为:Cu-2e→Cu2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com