
【题目】1mol O2在放电条件下发生下列反应:3O2![]() 2O3,如有30%O2转化为O3,则放电后混合气体对H2的相对密度是( )
2O3,如有30%O2转化为O3,则放电后混合气体对H2的相对密度是( )
A. 16 B. 17.8 C. 18.4 D. 35.6
【答案】B
【解析】
根据质量守恒定律可知,反应后混合气体的质量等于反应前氧气的质量,根据m=nM计算反应前氧气的质量,根据差量法计算反应后混合气体物质的量变化量,进而计算反应后混合气体总物质的量,再根据M=m/n计算混合气体的平均摩尔质量,相同条件下密度之比等于其摩尔质量之比,据此答题。
反应前氧气的质量为1mol×32g/mol=32g,根据质量守恒定律可知,反应后混合气体的质量为32g,参加反应氧气为1mol×30%=0.3mol
3O2![]() 2O3,物质的量减少
2O3,物质的量减少
3 2 1
0.3mol 0.1mol
故反应后混合气体总物质的量为1mol-0.1mol=0.9mol
则反应后混合气体的平均摩尔质量为32g/0.9mol=32/0.9g/mol
故混合气体相对氢气的密度为32/0.9g/mol÷2g/mol=17.8,故答案B正确。
故选B。


科目:高中化学 来源: 题型:
【题目】利用酸解法制钛白粉产生的废液生产铁红(Fe2O3)和补血剂乳酸亚铁的生产工业流程如下图所示:
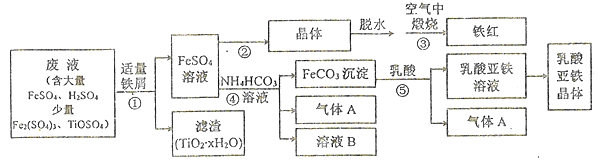
已知;TiOSO4在大量水中加热条件下可完全水解成为TiO2·xH2O沉淀。
请按要求回答下列问题:
(1)步骤①加入适量铁屑的目的是_________。TiOSO4完全水解的化学方程式为_________。
(2)步骤②的系列操作中,需要控制__________、_________条件下,再进行蒸发浓缩、冷却结晶,过滤、洗涤。其中洗涤液选用稀硫酸替代水的优点有__________。
(3)写出步骤③的化学方程式: _________。
(4)某兴趣小组学生以铁屑、稀硫酸、NH4HCO3溶液为原料,欲用下图装置,利用步骤④反应,达到制备FeCO3的目的。
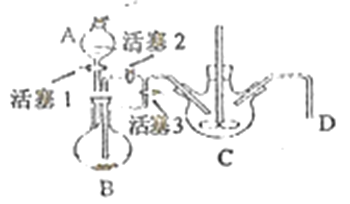
i.NH4HCO3溶液应盛放在装置(填字母) _______中。该装置中涉及的主要反应的离子方程式_________。
ii.达成步骤④反应的操作是__________。
(5)测定步骤②中所得晶体中FeSO4·7H2O的质量分数:
称取ag晶体样品,配成100.00mL溶液,取出25.00mL溶液,用硫酸酸化的0.1000mol/LKMnO4标准溶液滴定(杂质不与KMnO4溶液反应)。平行有效实验滴定消耗KMnO4溶液体积的平均值为20.00mL。则所得晶体中FeSO4·7H2O的质量分数为(设M(FeSO4·7H2O)=bg/mol,用含a、b的表达式表示)_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z的原子序数依次增加。A是元素Y的单质。常温下,甲的浓溶液和A发生钝化。丙、丁、戊是由这些元素组成的二元化合物,且丙是无色气体。上述物质的转化关系如图所示。下列说法正确的是
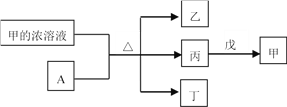
A. 丁和戊中所含元素种类相同
B. 简单离子半径大小:X<Y
C. 气态氢化物的还原性:X>Z
D. Y的简单离子与Z的简单离子在水溶液中可大量共存
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁、铝的混合物进行如下实验:

(1)操作X的名称是________________;
(2)气体A是___________(填化学式);
(3)溶液B中阴离子除OH- 外还有__________(填离子符号),溶液D中存在的金属离子为_________(填离子符号);
(4)加入足量NaOH溶液时发生反应的离子方程式为:_________;加入稀盐酸发生反应的离子方程式为:___________________________________________;
(5)向溶液D加入NaOH溶液,观察到产生的白色絮状沉淀迅速变为灰绿色,最终变为红褐色,请写出沉淀转化的化学方程式:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳是自然界中形成化合物种类最多的元素,CO和CO2是碳的最常见氧化物。
(1)研究和解决二氧化碳捕集和转化问题是当前科学研究的前沿领域。在太阳能的作用下,缺铁氧化物[Fe0.9O]能分解CO2,其过程如图1所示。过程①的化学方程式是______。在过程②中每产生0.1molO2,转移电子______mol。

(2)在催化剂作用下,将二氧化碳和氢气混合反应生成甲烷,是目前科学家们正在探索的处理空气中的二氧化碳的方法之一。
①已知:
共价键 | C=O | H—H | C—H | O—H |
键能/(kJmol-1) | 745 | 436 | 413 | 463 |
则CO2(g)+4H2(g)![]() CH4(g)+2H2O(g) △H=______kJmol-1。
CH4(g)+2H2O(g) △H=______kJmol-1。
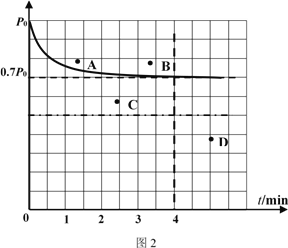
②向1L固定容积的密闭容器中加入4.0 mol H2(g)、1.0mol CO2,控制条件(催化剂:铑—镁合金、高温T1)使之反应,若测得容器内气体的压强随着时间的变化如图2所示。则4 min时容器内气体的密度为______;温度T1 下,该反应的化学平衡常为______。若采用2 L固定容积的密闭容器,投料量、催化剂和反应温度均保持不变,则反应重新达到平衡时对应体系内的压强的点是______(填字母)。
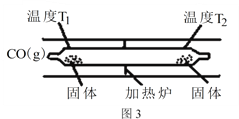
(3)工业合成原料气CO会与设备、管道及催化剂表面的金属铁、镍反应,生成羰基化合物。四羰基镍是热分解法制备高纯镍的原料,也是有机合成中供给一氧化碳的原料,还可做催化剂。Ni(s)+4CO(g)![]() Ni(CO)4(g) △H<0 Ni(CO)4(g)
Ni(CO)4(g) △H<0 Ni(CO)4(g)![]() Ni(s)+4CO(g)。如图3所示,在石英真空管的温度为T1一端,放入少量粗镍和CO(g),一段时间后,在温度为T2的一端可得到纯净的镍。则温度T1______T2(填“>”“<”或“=”),上述反应体系中循环使用的物质为______(填化学式)。
Ni(s)+4CO(g)。如图3所示,在石英真空管的温度为T1一端,放入少量粗镍和CO(g),一段时间后,在温度为T2的一端可得到纯净的镍。则温度T1______T2(填“>”“<”或“=”),上述反应体系中循环使用的物质为______(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钴的化合物在磁性材料生产、电池制造、催化剂制备等方面应用十分广泛。
(1)二价钴离子的核外电子排布式为______。基态Co原子核外3d能级上有______个未成对电子。Co与Ca属同周期,且核外最外层电子构型相同,但金属钴熔沸点都比钙高,原因是______。
(2)0.1mol[Co(NO2)6]3-中所含的σ键数目是______,K3[Co(NO2)6]中K、N、O三种元素的第一电离能由大到小的顺序是______。
(3)化合物四氨基钴酞菁分子的结构式如图。四氨基钴酞菁中N原子的杂化轨道类型为______。
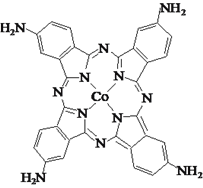
(4)[Co(NH3)6]Cl3晶体可由CoCl2溶于氨水并通入空气制得,该配合物中配体分子的立体构型是______。
(5)一种钴的化合物可用作石油脱硫的催化剂,其晶胞结构如图所示,则晶体中与每个O2-紧邻的O2-有______个,该钴的化合物的化学式是______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙二醛是一种低级醛,它有着极其活跃的化学反应性,并有广泛的用途。
I.乙二醛的工业制法如下:
(1)乙醛(CH3CHO)液相硝酸氧化法
在Cu(NO3)催化下,用稀硝酸氧化乙醛制取乙二醛,反应的离子方程式为___________。该法具有原料易得、反应条件温和等优点,但也存在比较明显的缺点是____________ 。
(2)乙二醇(HOCH2CH2OH)气相氧化法
①已知:OHC-CHO(g)+2H2(g)![]() HOCH2CH2OH(g) △H=-78kJ/mol K1
HOCH2CH2OH(g) △H=-78kJ/mol K1
2H2(g)+O2(g)![]() 2H2O(g) △H=-484kJ/mol K2
2H2O(g) △H=-484kJ/mol K2
乙二醇气相氧化反应HOCH2CH2OH(g)+O2(g)![]() OHC-CHO(g)+2H2O(g)的相同温度下,该反应的化学平衡常数K=___(用含K1、K2的代数式表示)。
OHC-CHO(g)+2H2O(g)的相同温度下,该反应的化学平衡常数K=___(用含K1、K2的代数式表示)。
②当原料气中氧醇比为1.35时,乙二醛和副产物CO2的产率与反应温度的关系如图所示。反应温度在450~495℃之间和超过495℃时,乙二醛产率降低的主要原因分别是____、____。
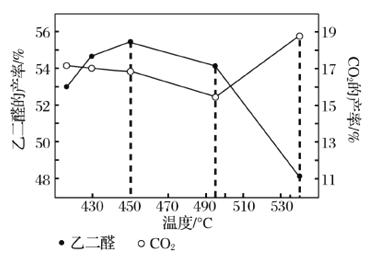
II.乙二醛的用途之一是可以电解氧化制备乙醛酸(OHC-COOH),其生产装置如图所示,通电后,阳极产生的Cl2与乙二醛溶液反应生成乙醛酸。
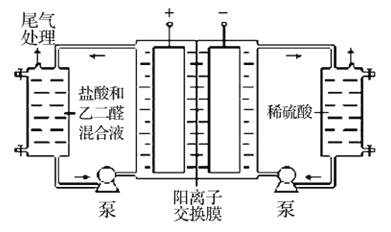
(3)阴极反应式为_________。
(4)阳极液中盐酸的作用,除了产生氯气外,还有__________作用。
(5)保持电流强度为aA,电解tmin,制得乙醛酸mg,列式表示该装置在本次电解中的电流效率η=__________ (已知:法拉第常数为fC·mol-l;![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图所示装置进行气体x的性质实验,得出的实验结论正确的是
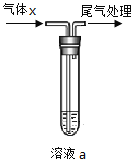
选项 | 实验操作 | 实验现象 | 实验结论 | |
制备气体x | 溶液a | |||
A | 乙醇与浓硫酸共热至170℃ | KMnO4酸性溶液 | 紫色褪去 | C2H4被氧化 |
B | 碳酸钠与醋酸溶液作用 | Na2SiO3溶液 | 产生白色沉淀 | H2CO3的酸性强于H2SiO3 |
C | 双氧水与二氧化锰作用 | KI淀粉溶液 | 溶液变蓝 | O2能将I-氧化为I2 |
D | 溴乙烷与氢氧化钠醇溶液共热 | Br2的四氯化碳溶液 | 橙红色褪去 | C2H4与Br2发生加成反应 |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com