
| A. | KOH和Al2(SO4)3 | B. | NaOH和Ca(HCO3)2 | C. | NaAlO2和 HCl | D. | K2CO3和HNO3 |
分析 只要用试管和胶头滴管,不用任何化学试剂就可以鉴别的物质可以采用相互滴加的方法检验,滴加顺序不同,现象不同的可以鉴别.反之不能鉴别,以此解答该题.
解答 解:A.KOH和Al2(SO4)3滴加顺序不同,现象不同,将KOH滴加到Al2(SO4)3中,先生成沉淀,后溶解,将Al2(SO4)3滴加到KOH中,先没有现象,后生成沉淀,二者反应现象不同,可鉴别,故A不选;
B.无论是Ca(HCO3)2滴加到NaOH中,还是NaOH滴加到Ca(HCO3)2中,都产生碳酸钙沉淀,不能鉴别,故B选;
C.盐酸滴加到偏铝酸钠溶液中,先生成沉淀,后沉淀溶解,偏铝酸钠滴加到盐酸中,先无沉淀,后生成沉淀,现象不同,可鉴别,故C不选;
D.HNO3滴加到中K2CO3,开始不生成气体,HNO3足量生成气体,碳酸钾滴加到硝酸中立即生成气体,不用任何化学试剂改变滴定顺序就可以鉴别,故D不选.
故选B.
点评 本题考查物质的鉴别和检验,为高频考点,把握物质的性质、与量有关的反应和现象为解答的关键,侧重分析与实验能力的考查,注意元素化合物性质的应用,题目难度不大.


 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 沉淀溶解后,将会生成深蓝色的配合离子[Cu(NH3)4]2+ | |
| B. | 反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变 | |
| C. | 向反应后的溶液加入乙醇,溶液不会有变化,因为[Cu(NH3)4]2+不会与乙醇发生反应 | |
| D. | 在[Cu(NH3)4]2+离子中,Cu2+给出孤对电子,NH3提供空轨道 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学键 | H-H | C-O | C=O | H-O | C-H |
| E/(kJ•mol-1) | 436 | 343 | 745 | 465 | 413 |
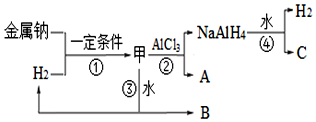
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
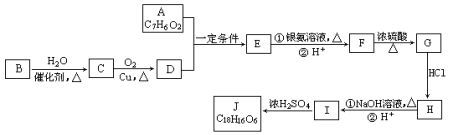
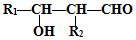
 ,G中含氧官能团的名称羟基、羧基.
,G中含氧官能团的名称羟基、羧基. $?_{△}^{浓H_{2}SO_{4}}$
$?_{△}^{浓H_{2}SO_{4}}$  +2H2O.
+2H2O.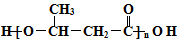 的路线图
的路线图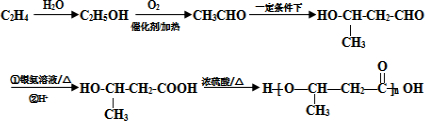 (提示:路线图的书写方法RCH=CH2
(提示:路线图的书写方法RCH=CH2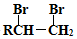 $→_{水/加热}^{NaOH}$
$→_{水/加热}^{NaOH}$ 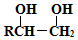 )
)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 立方烷( 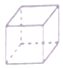 )的六氨基(-NH2)取代物有3种 )的六氨基(-NH2)取代物有3种 | |
| B. | C3H7ClO(有羟基)的同分异构体数目有5种 | |
| C. | 甲苯与氢气充分加成后的一溴代物有4种 | |
| D. | 分子式为C5H10O2的有机物中能与NaOH溶液反应的有13种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
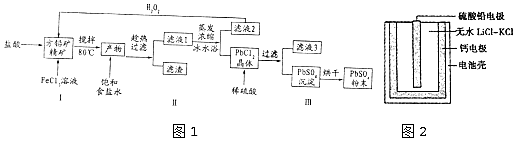
| 物质 | Ksp | 物质 | 开始沉淀时pH | 完全沉淀时pH |
| PbSO4 | 1.0×10-8 | Fe(OH)3 | 2.7 | 3.7 |
| PbCl2 | 1.6×10-5 | Fe(OH)2 | 6 | 7.04 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1,2-二甲苯也称邻二甲苯 | |
| B. | 氨基乙酸与a-氨基丙酸的混合物一定条件下脱水能生成4种二肽 | |
| C. | 苯与溴水不能发生加成反应,所以两者混合后无明显现象 | |
| D. | C5H10O2属于羧酸的同分异构体有4种 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
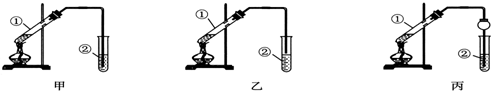
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com