
某校研究性学习小组拟利用分光光度法对空气中二氧化硫含量(mg/m3)进行测定。分光光度法则是通过测定被测物质在特定波长时光的吸收度,对该物质进行定性和定量分析。其工作原理可以简单的用公式表示为A=kc,其中A为吸光度,k为一定条件下的常数,c为溶液浓度。
 实验步骤如下:
实验步骤如下:
⑴ 采样:
① 如果你是该小组成员,你对采样的地点和时间有何建议: 。
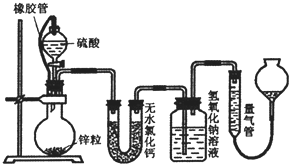
② 用右图装置采样,通过50L空气后,将吸收液移入100ml容量瓶,用少量吸
收液分两次洗涤吸收装置,合并洗涤液于容量瓶中,定容备用。用多孔球泡而不
用导管的原因是 。
⑵ 吸光度与SO2含量标准曲线的绘制:在6支25ml比色管中,用每毫升含25μg
二氧化硫的标准液配置下表标准SO2含量系列。
二氧化硫标准系列
| 管 号 | 0 | 1 | 2 | 3 | 4 | 5 |
| 标准液(ml) | 0 | 0.20 | 0.40 | 0.60 | 0.80 | 1.00 |
| 吸收液(ml) | 10.00 | 9.80 | 9.60 | 9.40 | 9.20 | 9.00 |
| 二氧化硫含量(μg) | 0 | 5.00 | 10.00 | 15.00 | 20.00 | 25.00 |
用10mL比色皿,以水为参比,测定各管吸光度,实验结果如下。
| 管 号 | 0 | 1 | 2 | 3 | 4 | 5 |
| 吸光度 | 0 | 0.20 | 0.40 | 0.60 | 0.80 | 1.00 |
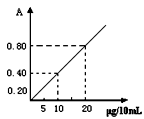
 请在右图所示的坐标系中绘制标准曲线:
请在右图所示的坐标系中绘制标准曲线:
⑶ 准确量取容量瓶中溶液10mL加入比色皿,测得其吸光度值
为0.10,则空气中二氧化硫含量为 mg/m3。我国环境空气
质量标准中对每次空气质量测定中SO2的最高浓度限值(mg/m3):
一级标准:0.15;二级标准:0.50;三级标准:0.70。
则该市空气为 级标准。
⑷ 甲、乙两组同学测定结果相差较大,乙组同学测定空气中SO2
含量偏小,试分析乙组同学出现误差的可能原因: (两个所用
药品和装置均无问题)。
 ⑴ ① 在不同地点、不同时间采样,如学校、工厂、居民区附近;早晨、中午、晚上分别采样
⑴ ① 在不同地点、不同时间采样,如学校、工厂、居民区附近;早晨、中午、晚上分别采样
② 使二氧化硫能被吸收液充分吸收
⑵ (见右图)
⑶ 0.5 二级标准
⑷ 抽气速率过快,造成空气中SO2与吸收液未充分反应,产生较大误差
B.本题考查化学实验。(1)①时间与地点的不同,可以提高测定数据的准确性。②多孔球泡的表面积比导管与溶液的接触面积要大得多,这样吸收更充分。(2)结合表中数据,找出关键点,如10.00ml对应的A为0.4,20.00ml对应的A为0.8,其他采用描点,即可作出标准线。(3)表格中的比例关系知,吸光度为0.1时,二氧化硫的含为2.5μg/ 10mL= 25ug/100mL,而空气为50L,则空气中二氧化硫含量为:25ug/50L=0.5 mg/m3,则对应为二级标准。(4)SO2含量偏小,其原因应为SO2的反应不充分,没有全部吸收。


科目:高中化学 来源: 题型:
 不同浓度的硫酸与锌反应时,硫酸可以被还原为S02,也可被还原为氢气.某校研究性学习小组拟设计实验验证这一事实,并进行数据测定和相关计算.
不同浓度的硫酸与锌反应时,硫酸可以被还原为S02,也可被还原为氢气.某校研究性学习小组拟设计实验验证这一事实,并进行数据测定和相关计算.查看答案和解析>>
科目:高中化学 来源: 题型:
某省2007年工业(主要是热电厂)二氧化硫排放总量为1.24×106 t,全省酸雨污染比较严重。分析降雨成分发现,雨水中阴离子仍以硫酸根离子为主,约占阴离子总量的61.9 %,阳离子以铵根离子为主,约占阳离子总量的84.1 %。阴离子中![]() 和
和![]() 的质量比为4.13∶1,
的质量比为4.13∶1,![]() 的比例呈明显上升的趋势。
的比例呈明显上升的趋势。
回答下列问题:
(1)该省大气污染特征是_________
A.煤烟型
B.机动车尾气型
C.由煤烟型向煤烟型与机动车尾气混合型转化
D.由机动车尾气型向煤烟型与机动车尾气混合型转化
(2)请你提出该省防治酸雨的两条主要措施_________________________;
(3)某校研究性学习小组拟选择“不同地点空气中二氧化硫的含量分析”的课题进行探究。
①参加该课题的探究,在小组讨论测定地点时,选择的测定地点分别是工厂、学校、村庄(或居民住宅区)、公园(或农田)等。
②通过查阅资料后发现,1994年以前,人们常采用HgCl2、NaCl的混合溶液吸收二氧化硫,1994年国家颁布标准(GB/T15262—94)规定用甲醛溶液吸收二氧化硫。变更吸收剂的原因除了用甲醛溶液的吸收效果比较好外,另一个原因可能是_______________________。③甲醛溶液吸收二氧化硫以后发生了如下反应,生成稳定的羟基甲磺酸:

该反应类型属于______________________________________________。
查看答案和解析>>
科目:高中化学 来源:河南省模拟题 题型:实验题

查看答案和解析>>
科目:高中化学 来源:河南省模拟题 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com