
| A. | Cl2是在反应②中既是氧化产物又是还原产物 | |
| B. | 氧化性强弱的顺序为:BrO3->ClO3->Cl2>Fe3+ | |
| C. | 溶液中可发生:ClO3-+6Fe2++6H+═Cl-+6Fe3++3H2O | |
| D. | Cl2在①、③反应中均作氧化剂 |
分析 A、根据②ClO-+5Cl-+6H+═3Cl2+3H2O反应中ClO-中Cl元素化合价由+5降低到0价的Cl2,Cl-中Cl元素化合价由-1价升高到0价的Cl2判断;
B、根据氧化剂的氧化性大于氧化产物的氧化性判断;
C、根据氧化剂的氧化性大于氧化产物的氧化性判断反应是否能发生;
D、根据Cl2在反应中化合价降低作氧化剂判断.
解答 解:A、②ClO-+5Cl-+6H+═3Cl2+3H2O反应中ClO-中Cl元素化合价由+5降低到0价的Cl2,Cl-中Cl元素化合价由-1价升高到0价的Cl2,所以Cl2是在反应②中既是氧化产物又是还原产物,故A正确;
B、①2BrO3-+Cl2═Br2+2ClO3-中,氧化性:BrO3->ClO3-,
②ClO3-+5Cl-+6H+═3Cl2+3H2O中,氧化性:ClO3->Cl2;
③2FeCl2+Cl2═2FeCl3中,氧化性:Cl2>Fe3+,所以氧化性强弱的顺序为:BrO3->ClO3->Cl2>Fe3+,故B正确;
C、氧化性:ClO3->Cl2>Fe3+,反应ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O能发生,故C正确;
D、①2BrO3-+Cl2═Br2+2ClO3-中,Cl2在反应中化合价升高作还原剂,③2FeCl2+Cl2═2FeCl3中,Cl2在反应中化合价降低作氧化剂,故D错误.
故选D.
点评 本题考查学生氧化还原反应中氧化剂和还原剂强弱的判断知识,属于综合知识的考查,难度中等,抓住化合价变化即可解题.


 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案科目:高中化学 来源: 题型:实验题
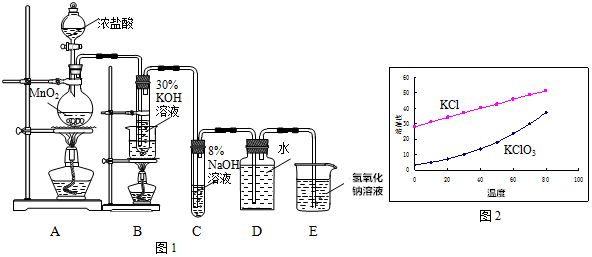
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能自发进行的反应一定能迅速发生 | |
| B. | 反应NH4HCO3(s)=NH3(g)+H2O(g)+CO2(g)△H=+185.57 kJ•mol-1能自发进行,是因为体系有自发地向混乱度增大的方向转变的倾向 | |
| C. | 因为焓变和熵变都与反应的自发性有关,因此焓变或熵变均可以单独作为判断反应能否自发进行的判据 | |
| D. | 在其他外界条件不变的情况下,使用催化剂,可以改变化学反应进行的方向 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁与氯化铁溶液反应:Fe+Fe3+=2Fe2+ | |
| B. | 大理石与稀盐酸反应:CO32-+2H+=CO2↑+H2O | |
| C. | 铜与稀硫酸反应:Cu+2H+=Cu2++H2↑ | |
| D. | 氯气与氢氧化钠溶液反应:Cl2+2OH-=Cl-+ClO-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯和甲苯分子中所有原子均在同一平面上 | |
| B. | 苯不可以使KMnO4酸性溶液褪色而甲苯可以 | |
| C. | 苯和甲苯都能与卤素单质、硝酸等发生取代反应 | |
| D. | 苯的同系物的分子通式是CnH2n-6(n≥7) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2O | B. | N2O3 | C. | NO2 | D. | N2O4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气溶于水:Cl2+H2O═Cl-+ClO-+2H+ | |
| B. | 金属钠加入稀硫酸中:Na+2H+═Na++H2↑ | |
| C. | 明矾溶液中加入足量Ba(OH)2溶液:SO42-+Al3++Ba2++4OH-═AlO2-+BaSO4↓+2H2O | |
| D. | 向含有稀盐酸的氯化亚铁溶液中通入氧气:4Fe2++O2+4H+═4 Fe3++2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 加3%Na2S2O3/mL | 加1:5的H2SO4/滴 | 温度/℃ | |
| A | 5 | 25 | 25 |
| B | 5 | 15 | 35 |
| C | 5 | 25 | 45 |
| D | 5 | 15 | 45 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将NaCl固体置于托盘天平右盘称量:左盘砝码(8g)和游码(0.6g)读数的和为8.6g | |
| B. | 容量瓶上标有刻度线、温度和浓度,使用前要事先检查是否漏水 | |
| C. | 配制一定物质的量浓度的溶液用到的主要仪器有:托盘天平、量筒、烧杯、玻璃棒、容量瓶、胶头滴管 | |
| D. | 配制1L0.2mol/L的H2SO4溶液,定容时仰视刻度线操作,则配出浓度偏高 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com