
组成和结构可用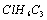
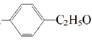 表示的有机物中,能发生消去反应的共有( )
表示的有机物中,能发生消去反应的共有( )
A.10种 B.16种 C.20种 D.25种
科目:高中化学 来源: 题型:
丙酮醛(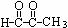 )是重要的制药中间体,如果以2-溴丙烷为初始原料,通过多步反应制得。需要经过的反应依次是( )
)是重要的制药中间体,如果以2-溴丙烷为初始原料,通过多步反应制得。需要经过的反应依次是( )
A.取代-氧化-加成-消去 B.消去-取代-加成-氧化
C.消去-加成-取代-氧化 D.取代-消去-加成-氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
I:常温下,将某一元酸HA和NaOH溶液等体积混合,分别进行编号为①、②、③的实验,实验数据记录如下表
| 序号 | HA物质的量浓度(mol·L-1) | NaOH物质的量浓度(mol·L-1) | 混合溶液的pH |
| ① | 0.1 | 0.1 | pH=9 |
| ② | c | 0.2 | pH=7 |
| ③ | 0.2 | 0.1 | pH<7 |
请回答:(1)根据①组实验情况,分析混合溶液的pH=9的原因是_________________。
(用反应的离子方程式表示),在该溶液中下列关系式不正确的是(填序号字母)________。
A.c(Na+)+c(H+)=c(OH-)+c(A-) B.c(Na+)=c(HA)+c(A-)
C.c(HA)+c(H+)=c(OH-) D.c(Na+)+c(H+)=c(OH-)+c(A-)+c(HA)
(2)②组情况表明,c 0.2mol·L-1(选填“>”、“<”或“=”)。混合溶液中离子浓度
c(A-)_____c(Na+)(选填“>”、“<”或“=”)从③组实验结果分析,说明HA的电离程度________NaA的水解程度(选填“>”、“<”或“=”)。
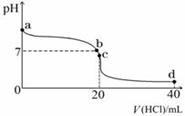 Ⅱ:室温下,若将0.1 mol·L-1盐酸滴入20 mL 0.1 mol·L-1氨水中,溶液pH随加入盐酸体积的变化曲线如下图所示。 (1)NH3·H2O的电离方程式是 。
Ⅱ:室温下,若将0.1 mol·L-1盐酸滴入20 mL 0.1 mol·L-1氨水中,溶液pH随加入盐酸体积的变化曲线如下图所示。 (1)NH3·H2O的电离方程式是 。
(2)b点所示溶液中的溶质是 。
(3)c点所示溶液中,离子浓度从大到小的关系为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知1~18号元素的离子aW3+、bX+、cY2-、dZ-都具有相同的电子层结构,下列关系正确的是( )
A.质子数:c>d B.离子的还原性:Y2->Z-
C.氢化物的稳定性:H2Y>HZ D.原子半径:X<W
查看答案和解析>>
科目:高中化学 来源: 题型:
下表标出的是元素周期表的一部分元素,回答下列问题:
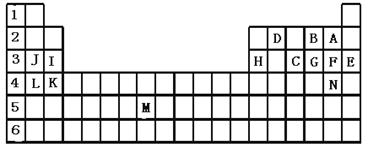 |
(1)表中用字母标出的15种元素中,化学性质最不活泼的是 (用元素符号表示,下同),金属性最强的是 ,非金属性最强的是 ,常温下单质为液态的非金属元素是 ,属于过渡元素的是 (该空用字母表示)。
(2)B,F,C气态氢化物的化学式分别为 、 、 ,其中以 最不稳定。
(3)第三周期中原子半径最小的是 (稀有气体元素除外)。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)某酯的分子式为C6H12O2,其变化如图所示:
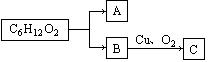
若A能发生银镜反应,C不能发生银镜反应,则该酯的可能结构有 种。
(2)将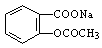 转变为
转变为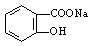 的流程为
的流程为
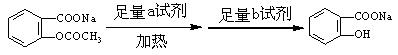
则a试剂是 ,b试剂是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
苯酚是一种重要的化工原料。以苯酚为主要起始原料,经下列反应可制得香料M和高分子化合物N(部分产物及反应条件已略去)。
(1)生成M、N的反应类型分别是 、 ; D的结构简式是 。
(2)已知C的分子式为C5H12O,C能与金属Na反应,C的一氯代物有2种。C的结构简式是 。
(3)由苯酚生成A的化学方程式是 。
B与C反应的化学方程式是 。
(4)以苯酚为基础原料也可以合成芳香族化合物F。经质谱分析F的相对分子质量为152,其中氧元素的质量分数为31.6%,F完全燃烧只生成CO2和H2O。则F的分子式是 。
已知:①芳香族化合物F能发生银镜反应,且还能发生水解反应;
②F的核磁共振氢谱显示其分子中含有4种氢原子;
③分子结构中不存在“-O-O- ”的连接方式。F的结构简式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
氢能的存储是氢能应用的主要瓶颈,目前所采用或正在研究的主要储氢材料有:配位氢化物、富氢载体化合物、碳质材料、金属氢化物等。
(1) Ti(BH4)2是一种过渡元素硼氢化物储氢材料。
①Ti2+基态的电子排布式可表示为________。
 ②BH
②BH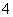 的空间构型是________(用文字描述)。
的空间构型是________(用文字描述)。
(2) 液氨是富氢物质,是氢能的理想载 体,利用N2+3H2
体,利用N2+3H2
 2NH3实现储氢和输氢。下列说法正确的是________(多项选择)。
2NH3实现储氢和输氢。下列说法正确的是________(多项选择)。
A. NH3分子中N原子采用sp3杂化
B. 相同压强时,NH3沸点比PH3高
C.[Cu (NH3)4]2+离子中,N原子是配位原子
D.CN-的电子式为[:C┇┇N:]-
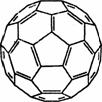 (3) 2008年,Yoon等人发现Ca与C60(分子结构如下图左)生成的Ca32C60能
(3) 2008年,Yoon等人发现Ca与C60(分子结构如下图左)生成的Ca32C60能 大量吸附H2分子。
大量吸附H2分子。

①C60晶体 易溶于苯、CS2,C60是________分子(填“极性”或“非极性”)。
易溶于苯、CS2,C60是________分子(填“极性”或“非极性”)。
②1 mol C60分子中,含有σ键数目为________。
(4) MgH2是金属氢化物储氢材料,其晶胞结构如上图右所示,已知该晶体的密度为a g·cm-3,则晶胞的体积为________cm3[a、NA表示(NA表示阿伏加德罗常数的值)]。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com