
有关下列四个常用电化学装置的叙述中,正确的是
|
|
|
|
图Ⅰ 碱性锌锰电池 | 图Ⅱ 铅-硫酸蓄电池 | 图Ⅲ 电解精炼铜 | 图Ⅳ 银锌纽扣电池 |
A.图Ⅰ所示电池中,MnO2的作用是催化剂
B.图II所示电池放电过程中,硫酸浓度不断增大
C.图III所示装置工作过程中,电解质溶液中Cu2+浓度始终不变
D.图IV所示电池中,Ag2O是氧化剂,电池工作过程中还原为Ag
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源:2015-2016学年广东省高一下期末化学试卷(解析版) 题型:选择题
如图是制取、净化并测量生成气体体积的装置示意图。利用如图装置进行下表所列实验,能达到实验目的的是( )
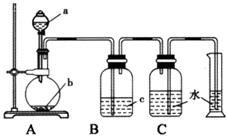
选项 | a(液体) | b(固体) | c(液体) |
A. | 稀盐酸 | 锌粒 | 浓硫酸 |
B. | 浓氨水 | 生石灰 | 浓硫酸 |
C. | 浓硫酸 | Cu片 | NaOH溶液 |
D. | 稀硝酸 | Cu片 | H2O |
查看答案和解析>>
科目:高中化学 来源:2015-2016年湖南省高一下期末化学试卷(解析版) 题型:实验题
已知铁生锈的过程为:Fe → Fe(OH)2 → Fe(OH)3 → Fe2O3·xH2O。又知草酸(H2C2O4)分解产生CO等气体某化学小组为测定两种不同生锈铁片的组成(设只含有铁和Fe2O3·xH2O),进行了以下探究,请你参与并完成对有关问题的解答。
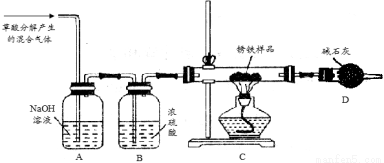
(1)甲同学利用草酸分解产生的混合气体和下图所示装置测定其中一种锈铁的组成。
主要操作为:取锈铁样品12.6 g置于装置C的硬质玻璃管中,加热完全反应后得到固体的质量为8.4 g,装置D增重8.4 g。
草酸(H2C2O4)分解的化学方程式为 。
(2)乙同学在甲同学装置的基础上将装置D换成装浓硫酸的洗气瓶(装置E,此装置图略),经改进后,重新按甲同学的操作和样品取用量进行实验,若完全反应后得到固体的质量仍为8.4 g,而装置E增重1.8 g,则x = ;m(Fe):m (Fe2O3·xH2O) =
查看答案和解析>>
科目:高中化学 来源:2015-2016年湖南省高一下期末化学试卷(解析版) 题型:选择题
一般地,同一主族的元素最外层电子数相同,其单质及其化合物具有相似的化学性质,下列关于同主族元素所形成物质的性质的推理中,正确的是
A. 钠与氯气反应能形成离子键,故钾与氯气反应也能形成离子键
B. 氯气能置换出NaBr溶液中的溴,故F2能置换出NaCl溶液中的氯
C. Li在氧气中燃烧生成Li2O,故Na在氧气中燃烧生成Na2O
D. C在自然界有稳定的单质存在,故Si在自然界也有稳定的单质存在
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江哈尔滨六中高二下期末化学试卷(解析版) 题型:填空题
(1)用零价铁(Fe)去除水体中的硝酸盐(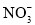 )已成为环境修复研究的热点之一。Fe还原水体中
)已成为环境修复研究的热点之一。Fe还原水体中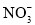 的反应原理如右图所示。
的反应原理如右图所示。
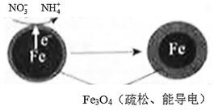
①作负极的物质是________。②正极的电极反应式是________ _。
(2)甲醇既是重要的化工原料,又可作为燃料,利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g)  CH3OH(g) △H1
CH3OH(g) △H1
②CO2(g)+3H2(g)  CH3OH(g)+H2O(g) △H2
CH3OH(g)+H2O(g) △H2
③CO2(g)+H2(g)  CO(g) +H2O(g) △H3
CO(g) +H2O(g) △H3
已知反应①中相关的化学键键能数据如下:
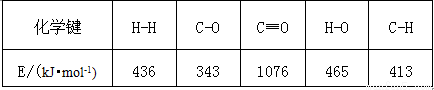
由此计算△H1= kJ·mol-1.已知△H2= –58kJ·mol-1,则△H3= kJ·mol-1.
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江哈尔滨六中高二下期末化学试卷(解析版) 题型:选择题
下列关于离子共存或离子反应的说法正确的是
A.某无色溶液中可能大量存在H+、Cl-、MnO4-
B.pH=2的溶液中可能大量存在Na+、NH4+、SiO32-
C.Fe2+与H2O2在酸性溶液中的反应:2Fe2++H2O2+2H+=2Fe3++2H2O
D.稀硫酸和Ba(OH)2溶液反应:H++SO42-+Ba2++OH-=BaSO4↓+H2O
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江哈尔滨六中高二下期末化学试卷(解析版) 题型:选择题
已知:H2O(g)===H2O(l) ΔH1=Q1 kJ/mol①
C2H5OH(g)===C2H5OH(l) ΔH2=Q2 kJ/mol②
C2H5OH(g)+3O2(g)===2CO2(g)+3H2O(g) ΔH3=Q3 kJ/mol③
若使23 g酒精液体完全燃烧,最后恢复到室温,则放出的热量为( )
A.Q1+Q2+Q3
B.0.5(Q1+Q2+Q3)
C.0.5Q1-1.5Q2+0.5Q3
D.1.5Q1-0.5Q2+0.5Q3
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江大庆实验中学高二下期末化学试卷(解析版) 题型:推断题
有机物A(C10H20O2)具有兰花香味,可用作香皂、洗发香波的芳香赋予剂。已知:
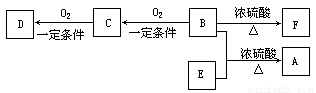
①B分子中没有支链。
②D能与碳酸氢钠溶液反应放出二氧化碳。
③D、E互为具有相同官能团的同分异构体。E分子烃基上的氢若被Cl取代,其一氯代物只有一种。
④F可以使溴的四氯化碳溶液褪色。
(1)B可以发生的反应有 (选填序号)。
①取代反应 ②消去反应 ③加聚反应 ④氧化反应
(2)D、F分子所含的官能团的名称依次是 、 。
(3)写出与D、E具有相同官能团的同分异构体的可能结构简式: 。
(4)E可用于生产氨苄青霉素等。已知E的制备方法不同于其常见的同系物,据报道,可由2—甲基—1—丙醇和甲酸在一定条件下制取E。该反应的化学方程式是 。
(5)某学生检验C的官能团时,取1mol/LCuSO4溶液和2mol/LNaOH溶液各1mL,在一支洁净的试管内混合后,向其中又加入0.5mL40%的C,加热后无红色沉淀出现。该同学实验失败的原因可能是 。(选填序号)
①加入的C过多
②加入的C太少
③加入CuSO4溶液的量过多
④加入CuSO4溶液的量不够
查看答案和解析>>
科目:高中化学 来源:2015-2016学年青海乐都一中高二下期末化学试卷(解析版) 题型:实验题
欲测定某NaOHmol•L-1溶液的物质的量浓度,可用0.100的HCl标准溶液进行中和滴定(用甲基橙作指示剂)。
请回答下列问题:
(1)滴定时,盛装待测NaOH溶液的仪器名称为______________;
(2)盛装标准盐酸的仪器名称为______________;
(3)滴定至终点的颜色变化为______________;
(4)若甲学生在实验过程中,记录滴定前滴定管内液面读数为0.50mL,滴定后液面如图,则此时消耗标准溶液的体积为______________;
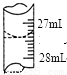
(5)乙学生做了三组平行实验,数据记录如下:
选取下述合理数据,计算出待测NaOH溶液的物质的量浓度为______________; (保留四位有效数字)
实验序号 | 待测NaOH溶液的体积/mL | 0.1000mol•L-1HCl溶液的体积/mL | |
滴定前刻度 | 滴定后刻度 | ||
1 | 25.00 | 0.00 | 26.29 |
2 | 25.00 | 1.00 | 31.00 |
3 | 25.00 | 1.00 | 27.31 |
(6)下列哪些操作会使测定结果偏高_________(填序号)。
A.锥形瓶用蒸馏水洗净后再用待测液润洗
B.酸式滴定管用蒸馏水洗净后再用标准液润洗
C.滴定前酸式滴定管尖端气泡未排除,滴定后气泡消失
D.滴定前读数正确,滴定后俯视滴定管读数.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com