
| A. | 在含Al3+、H+的溶液中缓慢滴加NaOH溶液:Al3+、H+ | |
| B. | 在含SiO32-的溶液缓慢滴加稀盐酸:SiO32-、CO32- | |
| C. | 在含Br-、Fe2+的溶液中缓慢通入氯气:Br-、Fe2+ | |
| D. | 在含有Cu2+、Fe3+的溶液中加入锌粉:Cu2-、Fe3+ |
分析 A.酸性强的与NaOH先反应;
B.弱酸跟越弱越易与氢离子结合;
C.还原性强的先被氯气氧化;
D.氧化性强的先与Fe反应.
解答 解:A.酸性由强到弱为H+、A13+、Al(OH)3,则逐滴加入NaOH溶液,反应先后顺序为H+、A13+、Al(OH)3,故A错误;
B.水解程度强到弱为SiO32-、CO32-,则缓慢滴加稀盐酸,反应先后顺序为SiO32-、CO32-,故B正确;
C.还原性由强到弱为Fe2+、Br-,则缓慢通入氯气的先后顺序为Fe2+、Br-,故C错误;
D.氧化性为Fe3+>Cu2+,则加入铁粉反应的先后顺序为Fe3+、Cu2+,故D错误;
故选B.
点评 本题考查反应的先后顺序,为高频考点,把握酸性、还原性、氧化性、溶度积等为解答的关键,侧重分析与应用能力的考查,综合性较强,题目难度不大.


科目:高中化学 来源: 题型:解答题
| 化合物 | A | B | C |
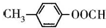
| 结构简式 | 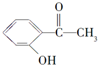 | 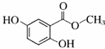 | 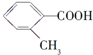 |
| 化合物 | D | E | F |
| 结构简式 |  | 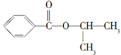 |  |
 .
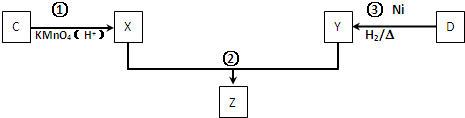
.
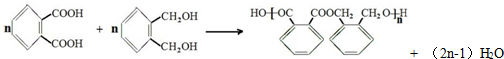 .
.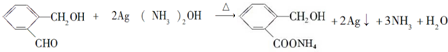 .
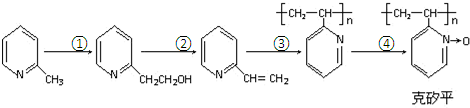
.
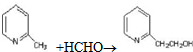 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在Fe2(SO4)3溶液中加入过量的铁粉,过滤,在滤液中加入过量的NaOH溶液 | |
| B. | 用铁粉与稀硫酸充分反应,然后再加入过量的氨水 | |
| C. | 在FeCl2溶液上加一层苯,然后将滴管插入到FeCl2溶液液面以下,慢慢滴加NaOH溶液(溶液中不能有气泡,配制FeCl2和NaOH溶液的蒸馏水必须加热煮沸) | |
| D. | 在生成Fe(OH)3的悬浊液中加过量的铁粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 实验一 | 实验二 | |
| 实验药品 | 4g P2O5、8mL无水乙醇 | |
| 实验条件 | 酒精灯加热 | 水浴加热 |
实验现象 | 无水乙醇加入时,圆底烧瓶B中P2O5溶于乙醇,立即产生白雾,当用酒精灯加热后,有气泡产生,并逐渐沸腾,生成粘稠状液体,集气瓶C中有无色液体产生. | 无水乙醇加入时,圆底烧瓶B中P2O5溶于乙醇立即产生白雾,当用水浴加热后,无气泡产生,生成粘稠状液体,集气瓶C中有无色液体产生. |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 钠和铜的单质及其化合物在生活实际中有着广泛的应用.
钠和铜的单质及其化合物在生活实际中有着广泛的应用.| NaF | NaCl | NaBr | NaI | |
| 熔点/℃ | 993 | 801 | 747 | 661 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
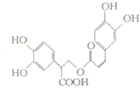 迷迭香酸是从蜂花属植物中提取的物质,其结构简式如图所示.则等量的迷迭香酸消耗的Br2、NaOH、NaHCO3的物质的量之比为( )
迷迭香酸是从蜂花属植物中提取的物质,其结构简式如图所示.则等量的迷迭香酸消耗的Br2、NaOH、NaHCO3的物质的量之比为( )| A. | 7:6:1 | B. | 7:6:5 | C. | 6:7:1 | D. | 6:7:5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(H2)=0.03 mol/(L•min) | B. | v(N2)=0.02 mol/(L•min) | ||
| C. | v(NH3)=0.01 mol/(L•min) | D. | v(NH3)=0.17 mol/(L•min) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com