
 如图表示的反应关系中,部分产物被略去.已知2mol白色固体粉末X受热分解,恢复到室温生成白色固体A、无色液体B、无色气体C各1mol.X、E、G的焰色反应均为黄色.回答下列问题:
如图表示的反应关系中,部分产物被略去.已知2mol白色固体粉末X受热分解,恢复到室温生成白色固体A、无色液体B、无色气体C各1mol.X、E、G的焰色反应均为黄色.回答下列问题:| Na2O2 |
| Al |
| 足量盐酸 |
| Na2O2 |
| Al |
| 足量盐酸 |


科目:高中化学 来源: 题型:

| A、上一个计量点前发生反应的离子方程式为HCO3-+H+═H2O+CO2↑ |
| B、下一个计量点溶液中存在大量的阴离子是Cl-、HCO3- |
| C、此样品n(NaHCO3)=(28.1-2×11.9)×10-3 mol |
| D、使用该方法测定Na2CO3和NaOH混合溶液中的氢氧化钠含量,将会得到1个计量点 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
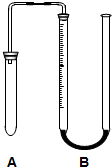 某小组学生想研究不同物质对双氧水分解速率的影响,以生成气体量50mL为标准,设计了如下实验方案:
某小组学生想研究不同物质对双氧水分解速率的影响,以生成气体量50mL为标准,设计了如下实验方案:| 实验序号 | 双氧水体积 | 双氧水浓度 | 添加的物质 | 待测数据X |
| 1 | 100mL | 20% | 无 | |
| 2 | 100mL | 20% | 10gMnO2 | |
| 3 | 100mL | 20% | 10gKI | |
| 4 | 100mL | 20% | 新鲜猪肝 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等量的CH4和Cl2在光照下反应生成纯净的CH3Cl |
| B、将苯与浓硝酸和浓硫酸共热制取硝基苯 |
| C、将红热的铜丝迅速插入无水乙醇中可将乙醇氧化为乙醛 |
| D、可用浓硝酸鉴别淀粉溶液和鸡蛋白溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 化学事实 | 推论 | |
| A | 将SO2通入品红溶液中,溶液褪色 | SO2具有氧化性 |
| B | 铝热反应需要高温引燃 | 该反应的△H>0 |
| C | 聚光束仪照射淀粉溶液,看到一条“光亮通路” | 淀粉分子直径>10-7m |
| D | 向溶液中滴加KSCN,无明显现象,再加氯水,看 到溶液变为血红色 | 说明原溶液中含有Fe2+ |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
 乙酸正丁酯常用作织物、人造革和塑料生产过程中的溶剂,石油和医药工业中的萃取剂,也用于香料复配以及香蕉、菠萝、杏、梨等多种香味剂的成分.实验室制备乙酸正丁酯的化学方程式为:
乙酸正丁酯常用作织物、人造革和塑料生产过程中的溶剂,石油和医药工业中的萃取剂,也用于香料复配以及香蕉、菠萝、杏、梨等多种香味剂的成分.实验室制备乙酸正丁酯的化学方程式为:| 浓H2SO4 |
| △ |
| 浓H2SO4 |
| △ |
| 化合物 | 正丁醇 | 冰醋酸 | 乙酸正丁酯 | 正丁醚 |
| 密度/g?mL-1 | 0.810 | 1.049 | 0.882 | 0.7689 |
| 沸点/℃ | 117.8 | 118.1 | 126.1 | 143 |
| 在水中的溶解性 | 易溶 | 易溶 | 难溶 | 难溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、只② | B、只②③⑤ |
| C、只②③④ | D、①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在0.1 mol?L-1NH3?H2O溶液中:c(NH3H2O)>c(NH4+)=c(OH-)>c(H+) |
| B、0.1 mol?L-1 HCl溶液与0.1 molL-1NaOH溶液等体积混合:c(H+)+c(Na+)=c(OH-)+c(Cl-) |
| C、0.1 molL-1NaOH和0.1 mol?L-1NH4Cl溶液等体积混合后:c(Na+)=c(Cl-)>c(H+)>c(OH-) |
| D、25℃时,某物质的溶液pH<7,则该物质一定是酸或强酸弱碱盐 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com