
甲、乙两溶液中,分别含有大量的Cu2+、K+、H+、Cl-、CO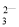 、OH-6种离子中的3种,已知甲溶液呈蓝色,则乙溶液中大量存在的离子是
、OH-6种离子中的3种,已知甲溶液呈蓝色,则乙溶液中大量存在的离子是
A.Cu2+、H+、Cl- B.K+、OH-、CO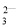
C.K+、H+、Cl- D.CO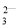 、OH-、Cl-
、OH-、Cl-
 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源:2015届北京理工附中高三第一次月考化学试卷(解析版) 题型:填空题
(10分)在一密闭容器中发生反应N2+3H2 2NH3.达到平衡后,只改变某一个条件时,反应速率与反应进程的关系如图所示:
2NH3.达到平衡后,只改变某一个条件时,反应速率与反应进程的关系如图所示:
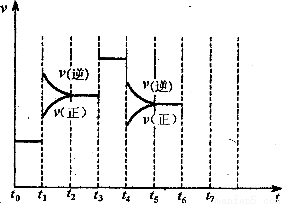
回答下列问题:
(1)处于平衡状态的时间段是 (填选项);
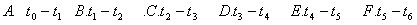
(2)t1 t2 t3时刻分别改变的一个条件是(填选项)
A 增大压强 B、减小压强 C.升高温度
D、降低温度 E、加催化剂 F、充人氮气
t1时刻 t3时刻 t4时刻
(3)依据(2)中的结论,下列时间段中,氨的百分含量最高的是 (填选项);
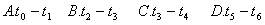
(4)如果在t6对刻,从反应体系中分离出部分氨,t7时刻反应达到平衡状态,请在图中画出反应速率的变化情况;
(5)一定条件下,合成氨反应达到平衡时,测得反应混合气中氨气的体积分数为20%,则反应后与反应前的混合气体体积之比为
查看答案和解析>>
科目:高中化学 来源:2015届北京市高三上学期第一次月考化学试卷(解析版) 题型:选择题
绿原酸的结构简式如图,下列有关绿原酸的说法不正确的是
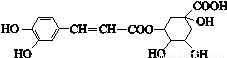
A.分子式为C16H18O9
B.能与Na2CO3反应
C.能发生取代反应和消去反应
D.0.1 mol绿原酸最多与0.8 mol NaOH反应
查看答案和解析>>
科目:高中化学 来源:2015届北京市高三上学期第一次质量检测化学试卷(解析版) 题型:选择题
物质的量之比为2:5的锌与稀硝酸反应,若硝酸被还原的产物为N2O,反应结束后锌没有剩余,则该反应中被还原的硝酸与未被还原的硝酸的物质的量之比是
A.1:4 B.1:5 C..2:3 D.2:5
查看答案和解析>>
科目:高中化学 来源:2015届北京市高三上学期第一次质量检测化学试卷(解析版) 题型:选择题
下列物质在水溶液中的电离方程式不正确的是
A.NaHSO4===Na++H++SO42-
B.AgCl===Ag++Cl-
C.Ba(OH)2===Ba2++2OH-
D.CH3COONH4 NH4++CH3COO-
NH4++CH3COO-
查看答案和解析>>
科目:高中化学 来源:2015届北京市高三上学期第一次质量检测化学试卷(解析版) 题型:选择题
分类法是一种行之有效、简单易行的科学方法。某同学用如表所示的形式对所学知识进行分类,甲与乙、丙、丁是包含关系。其中正确的是

查看答案和解析>>
科目:高中化学 来源:2015届北京市朝阳区高三年级第一学期期中统一考试化学试卷(解析版) 题型:实验题
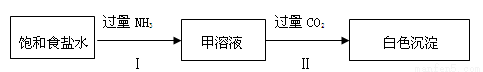
(10分) NaHCO3是重要的化工原料,在实验室里可通过下列两个步骤得到:
已知一些物质在20℃、30℃时溶解度数据:
温度(℃) | NH4Cl | NH4HCO3 | NaHCO3 | NaCl | Na2CO3 | (NH4)2CO3 |
20 | 28.7 | 21.7 | 9.6 | 31.5 | 21.5 | 100 |
30 | 41.1 | 27.0 | 11.1 | 36.3 | 39.7 | >100 |
请回答:
(1)步骤Ⅰ反应的化学方程式是 。
(2)若将NH3和CO2两种气体通入顺序互换后没有沉淀,原因是 。
(3)步骤Ⅱ所得白色沉淀中一定有NaHCO3,原因是 。
(4)步骤Ⅱ生成NaHCO3的离子方程式是 。
(5)根据气体物质溶解性及上列溶解度数据,简述上述两过程在较低温度下进行时效果更好的原因 。
查看答案和解析>>
科目:高中化学 来源:2015届北京市朝阳区高三年级第一学期期中统一考试化学试卷(解析版) 题型:选择题
下列生活中的化学事例对应的离子方程式书写正确的是
A.用醋酸除去暖瓶中的水垢:2H++CaCO3== Ca2++ CO2↑+ H2O
B.利用Na2CO3溶液可除油污:CO32- + 2H2O  H2CO3 + 2OH-
H2CO3 + 2OH-
C.氢氧燃料电池在酸性介质中的正极反应:O2 +4e- +2H2O = 4OH-
D.汽车用的铅蓄电池充电时阳极反应:PbSO4+2H2O-2e-== PbO2+4H++SO
查看答案和解析>>
科目:高中化学 来源:2015届内蒙古赤峰市高三上学期9月质量检测化学试卷(解析版) 题型:填空题
(9分)氮的氧化物对人体危害极大,实验时应防止其对空气的污染。
实验一:某同学利用下列装置实现铜与浓硝酸、稀硝酸的反应。
Ⅰ、取一段铜丝,用稀硫酸除去铜锈[主要成分是Cu2(OH)2CO3]。
Ⅱ、将洗涤后的铜丝做成匝数较多的螺旋状。
Ⅲ、按如图所示装置连接仪器、检查气密性、装入化学试剂。

(1)请完成过程Ⅰ发生反应的离子方程式:
Cu2(OH)2CO3+4H+= 。
(2)过程Ⅲ的后续操作如下:
① 为使浓硝酸与铜丝接触,操作是打开止水夹a和b, ,当红棕色气体较多时,轻抽注射器使反应停止,关闭a,取下注射器。生成红棕色气体的化学方程式是 。
② 控制b与分液漏斗活塞,玻璃管充满稀硝酸时,关闭b打开a,可见有无色气体产生。稀硝酸充满玻璃管的目的是 。
实验二:NO2与水反应的实验研究。
(3)将3支充满红棕色气体的小试管分倒置在盛有常温水、热水和冰水的3只烧杯中,发现液面上升的高度明显不一致。结果如下表所示(忽略温度对气体体积的影响):
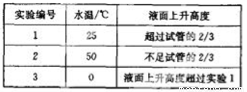
① 根据上表得出的结论是温度越 (填“高”或“低“),进入试管中的溶液越多。
② 查阅材料:a.NO2与水反应的实际过程为:2NO2+ H2O=HNO3+ HNO2,3 HNO2= HNO3+2NO↑+H2O;b. HNO2不稳定。则产生上述现象的原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com