
【题目】电离平衡常数(用Ka表示)的大小可以判断电解质的相对强弱。25℃时,有关物质的电离平衡常数如下表所示:
化学式 | HF | H2CO3 | HClO |
电离平衡 常数(Ka) | 7.2×10-4 | K1=4.4×10-7 K2=4.7×10-11 | 3.0×10-8 |
(1)将浓度为0.1mol·L-1HF溶液加水稀释一倍(假设温度不变),下列各量增大的是___。
A.c(H+) B.c(H+)·c(OH-) C.![]() D.
D.![]()
(2)25℃时,在20mL0.1mol·L-1氢氟酸中加入VmL0.1mol·L-1NaOH溶液,测得混合溶液的pH变化曲线如图所示,下列说法正确的是___。
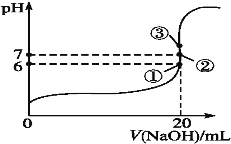
A.pH=3的HF溶液和pH=11的NaF溶液中,由水电离出的c(H+)相等
B.①点时pH=6,此时溶液中c(F-)-c(Na+)=9.9×10-7mol·L-1
C.②点时,溶液中的c(F-)=c(Na+)
D.③点时V=20mL,此时溶液中c(F-)<c(Na+)=0.1mol·L-1
(3)物质的量浓度均为0.1mol·L-1的下列四种溶液:①Na2CO3溶液;②NaHCO3溶液;③NaF溶液;④NaClO溶液。依据数据判断pH由大到小的是___。
(4)Na2CO3溶液显碱性是因为![]() 水解的缘故,请设计简单的实验事实证之___。
水解的缘故,请设计简单的实验事实证之___。
(5)长期以来,一直认为氟的含氧酸不存在。1971年美国科学家用氟气通过细冰末时获得HFO其结构式为H-O-F。HFO与水反应得到HF和化合物A,每生成1molHF转移___mol电子。
【答案】CD BC ①④②③(或①>④>②>③) 在碳酸钠溶液中滴入酚酞溶液变红,再加入BaCl2溶液后产生沉淀且红色褪去或变浅 1
【解析】
浓度为0.1mol·L-1HF溶液加水稀释一倍,虽然电离程度增大,但c(H+)、c(F-)、c(HF)都减小,c(OH-)增大。25℃时,在20mL0.1mol·L-1氢氟酸中加入VmL0.1mol·L-1NaOH溶液,①点时pH=6,说明HF、NaF混合溶液中以HF电离为主;②点时,pH=7,则表明HF、NaF混合溶液中,HF电离的程度与F-水解的程度相等;③点时V=20mL,溶液中只有NaF一种溶质,则F-水解而使溶液显碱性。在盐溶液中,酸电离常数越大,酸根离子水解的程度越小;若想证明酸根离子发生水解而使溶液显碱性,需证明离子浓度改变后,溶液的性质发生明显的改变;HFO与水反应得到HF和化合物A,依据质量守恒,A应为H2O2。
(1)A.浓度为0.1mol·L-1HF溶液加水稀释一倍,虽然电离程度增大,但c(H+)减小,A不合题意;
B.c(H+)·c(OH-)=KW,温度不变时,水的离子积常数不变,B不合题意;
C.![]() =
=![]() ,加水稀释,K(HF)不变,但c(F-)减小,所以
,加水稀释,K(HF)不变,但c(F-)减小,所以![]() 增大,C符合题意;
增大,C符合题意;
D.HF溶液加水稀释后,c(H+)减小,c(OH-)增大,则![]() 增大,D符合题意;
增大,D符合题意;
故选CD。答案为:CD;
(2)A.pH=3的HF溶液中水的电离受到抑制,pH=11的NaF溶液中,因F-而促进水的电离,所以由水电离出的c(H+)后者大于前者,A不正确;
B.①点时pH=6,HF、NaF混合溶液中以HF电离为主,此时溶液中c(F-)-c(Na+)= c(H+)- c(OH-)=10-6mol/L-10-8mol/L=9.9×10-7mol·L-1,B正确;
C.②点时,依据电荷守恒c(F-)+ c(OH-)=c(Na+)+ c(H+),pH=7,c(H+)=c(OH-),所以溶液中的c(F-)=c(Na+),C正确;
D.③点时V=20mL,溶液中只有NaF一种溶质,则F-水解而使溶液显碱性,此时溶液中c(F-)<c(Na+)=0.05mol·L-1,D不正确;
故选BC。答案为:BC;
(3)物质的量浓度均为0.1mol·L-1的下列四种溶液:①Na2CO3溶液;②NaHCO3溶液;③NaF溶液;④NaClO溶液。电离平衡常数的数据越小,盐的水解能力越强,c(OH-)越大,pH越大,由此确定盐的水解能力:Na2CO3溶液> NaClO溶液> NaHCO3溶液> NaF溶液,pH由大到小的是①④②③(或①>④>②>③)。答案为:①④②③(或①>④>②>③);
(4)Na2CO3溶液显碱性是因为![]() 水解的缘故,可通过减少
水解的缘故,可通过减少![]() 的浓度,观察溶液的颜色发生明显的改变,确定
的浓度,观察溶液的颜色发生明显的改变,确定![]() 水解使溶液显碱性,简单的实验事实为:在碳酸钠溶液中滴入酚酞溶液变红,再加入BaCl2溶液后产生沉淀且红色褪去或变浅。答案为:在碳酸钠溶液中滴入酚酞溶液变红,再加入BaCl2溶液后产生沉淀且红色褪去或变浅;
水解使溶液显碱性,简单的实验事实为:在碳酸钠溶液中滴入酚酞溶液变红,再加入BaCl2溶液后产生沉淀且红色褪去或变浅。答案为:在碳酸钠溶液中滴入酚酞溶液变红,再加入BaCl2溶液后产生沉淀且红色褪去或变浅;
(5)在HFO中,O元素显0价,HFO+H2


科目:高中化学 来源: 题型:
【题目】室温时,已知Ka(CH3COOH)=Kb(NH3H2O)。关于浓度均为0.1mol·L-1的醋酸和氨水的两种溶液的说法正确的是( )
①两溶液的pH之和为14
②两溶液中醋酸和NH3H2O的电离程度相同
③两溶液加水稀释,溶液中各离子浓度均降低
④两溶液等体积混合,pH=7,由水电离出c(H+)=1×10-7mol·L-1
A.①②B.②④C.①②④D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1 L某混合溶液中,溶质X、Y浓度都为0.1mol·L—1,向混合溶液中滴加0.1 mol·L—1某溶液Z,所得沉淀的物质的量如图所示,则X、Y、Z分别是 ( )
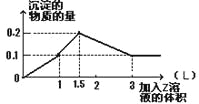
A.偏铝酸钠、氢氧化钡、硫酸
B.氯化铝、氯化镁、氢氧化钠
C.氯化铝、氯化铁、氢氧化钠
D.偏铝酸钠、氯化钡、硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释事实的化学用语不正确的是
A. 闪锌矿(ZnS)经CuSO4溶液作用后,转化为铜蓝(CuS):ZnS + Cu2+ === CuS + Zn2+
B. 0.1 mol/L 的醋酸溶液pH约为3:CH3COOH ![]() CH3COO- + H+
CH3COO- + H+
C. 电解NaCl溶液,阴极区溶液pH增大:2H2O + 2e- === H2↑+ 2OH-
D. 钢铁发生吸氧腐蚀,负极反应为:Fe-3e- === Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁和铝是两种重要的金属,它们的单质及化合物有着各自的性质。在一定温度下,氧化铁可以与一氧化碳发生下列反应:Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)
(1)该温度下,在2 L盛有Fe2O3粉末的密闭容器中通入CO气体,10 min后,生成了单质铁11.2 g。则10 min内CO的平均反应速率为_________。
(2)请用上述反应中某种气体的有关物理量来说明该反应已达到平衡状态:
①____________________________________________________;
②_____________________________________________________。
(3)某些金属氧化物粉末和铝粉在镁条的引燃下可以发生铝热反应。下列反应速率(v)和温度(T)的关系示意图中与铝热反应最接近的是___________________。
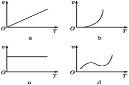
(4)写出氢氧化铝在水中发生碱式电离的电离方程式:___________________欲使上述体系中铝离子浓度增加,可加入的物质是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知: RX+Mg![]() RMgX (RX为卤代烃,X为卤族原子),生成的卤代烃基镁与具有羰基结构的化合物(醛、酮等)发生反应,再水解就能合成各种指定结构的醇:
RMgX (RX为卤代烃,X为卤族原子),生成的卤代烃基镁与具有羰基结构的化合物(醛、酮等)发生反应,再水解就能合成各种指定结构的醇:

现以2-丁烯和必要的无机物为原料合成F,进而合成一种分子式为C10H16O4的具有六元环的物质J,合成线路如下:(G的核磁共振氢谱有三组峰)
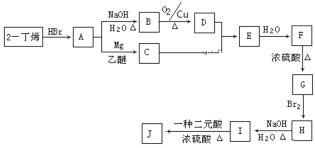
请按要求填空:
(1)F的系统命名:___________________________,E的结构简式是_________________________
(2)C→E的反应类型是______________,F→G的反应类型是___________________
(3)写出I→J化学反应方程式:___________________________________________
(4)A的同分异构体共有______种
(5)M为D的同分异构体且能发生银镜反应,写出所有M的结构简式_______________;其中核磁共振氢谱中出现3组峰的物质与新制氢氧化铜悬浊液在煮沸条件下发生反应的方程式为:______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一固定容积为2L的密闭容器内加入0.2mol的N2和0.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)2NH3(g)△H<0
(1)平衡常数的表达式K=__________,该反应450℃的平衡常数__________500℃时的平衡常数(填“>”、“<”或“=”);
(2)下列描述中能说明上述反应已达平衡的是__________
A.3υ正(H2)=2υ逆(NH3)
B.容器中气体的平均相对分子量不随时间而变化
C.容器中气体的密度不随时间而变化
D.容器中气体的分子总数不随时间而变化
(3)上述反应若第5分钟时达到平衡,测得NH3的物质的量为0.2mol计算从反应开始到平衡时,平均反应速率υ(N2)为__________mol/(L·min),NH3的体积分数__________
(4)保持其他条件不变,若初始投入量为amolN2、bmolH2、cmolNH3,也可得到与上述相同的平衡,则a、b、c需满足关系式:__________;
(5)第6分钟时,保持其它条件不变,若继续通入0.2mol的N2和0.6mol的H2,8分钟时达到平衡,N2的转化率__________(填“增大”、“减小”、“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,下列叙述不是可逆反应A(g)+3B(g)![]() 2C(g)达到平衡状态标志的是( )
2C(g)达到平衡状态标志的是( )
①C生成的速率与C分解的速率相等;②单位时间内生成a mol A,同时生成3a mol B;③A、B、C的浓度不再变化;④A、B、C的压强不再变化;⑤混合气体的总压强不再变化;⑥混合气体的物质的量不再变化;⑦单位时间内消耗a mol A,同时生成3a mol B;⑧A、B、C的分子数之比为1∶3∶2
A.②⑧B.①⑥C.②④D.③⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组用如图所示装置探究金属锌和稀硫酸的反应,实验过程中电流表的指针发生偏转。请回答下列问题:
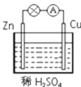
(1)锌片做电池的__________极(填“正或负”),发生的电极反应式:__________。
(2)铜片的现象是__________,发生的电极反应式:__________。
(3)若将稀H2SO4换成CuSO4,则正极反应式为:__________。
(4)若将电极换成铁片和铜片,则负极是__________(填“铁片或铜片”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com