
¢Ł14Cu2++5FeS2+12H2O £½ 7Cu2S + 5Fe2+ + 24H++3SO42-
¢ŚMn2+ + S2O82- + H2O”Ŗ MnO4- + SO42- H+
¶ŌÉĻŹöĮ½øö·“ӦŊ¶ĻÕżČ·µÄŹĒ£ŗ
| A£®¢Ł¢Ś·“Ó¦ÖŠSO42”Ŗ¶¼ŹĒŃõ»Æ²śĪļ |
| B£®Į½øö·“Ó¦ÖŠµē×Ó×ŖŅĘŹżÄ涼ŹĒ10mol |
| C£®¢Ł·“Ó¦ÖŠµÄĮņŌŖĖŲ¼Č±»Ńõ»ÆÓÖ±»»¹Ō |
| D£®Ńõ»ÆŠŌ£ŗMnO4”Ŗ> S2O82”Ŗ |
C
½āĪöŹŌĢā·ÖĪö£ŗA”¢S2O82-ÖŠSŌŖĖŲĪŖ+6¼Ū£¬×Ŗ»ÆĪŖSO42?S»ÆŗĻ¼Ū²»±ä£¬ĖłŅŌ·“Ó¦¢ŚÖŠSO42?²»ŹĒŃõ»Æ²śĪļ£¬“ķĪó£»B”¢·“Ó¦¢Ł»ÆŗĻ¼ŪÉżøߵďĒFeS2ÖŠµÄS×Ŗ»ÆĪŖSO42?£¬×ŖŅʵē×ÓĪŖ3”Į7mol=21mol£¬“ķĪó£»C”¢5FeS2ÖŠ3S×Ŗ»ÆĪŖSO42?£¬ĮņŌŖĖŲ»ÆŗĻ¼ŪÉżøߣ¬7S×Ŗ»ÆĪŖCu2S£¬ĮņŌŖĖŲ»ÆŗĻ¼Ū½µµĶ£¬ĖłŅŌ¢Ł·“Ó¦ÖŠµÄĮņŌŖĖŲ¼Č±»Ńõ»ÆÓÖ±»»¹Ō£¬ÕżČ·£»D”¢·“Ó¦¢ŚÖŠ£¬S2O82”ŖĪŖŃõ»Æ¼Į£¬MnO4”ŖĪŖŃõ»Æ²śĪļ£¬øł¾ŻŃõ»Æ¼ĮµÄŃõ»ÆŠŌ“óÓŚŃõ»Æ²śĪļ£¬ŌņŃõ»ÆŠŌ£ŗ S2O82”Ŗ>MnO4”Ŗ£¬“ķĪó”£
æ¼µć£ŗ±¾Ģāæ¼²éŃõ»Æ»¹Ō·“Ó¦ŌĄķ”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ÖųĆū»Æѧ¼ŅŠģ¹āĻÜ»ńµĆ¹ś¼Ņ×īøßæĘѧ¼¼Źõ½±£¬ŅŌ±ķÕĆĖūŌŚĻ”ĶĮŻĶČ”ĄķĀŪ·½Ćę×÷³öµÄ¹±Ļ×”£ŅŃÖŖ£ŗ½šŹōīę£ØĻ”ĶĮŌŖĖŲ£©ŌŚæÕĘųÖŠŅ×Ńõ»Æ±ä°µ£¬ŹÜČČŹ±Č¼ÉÕ£¬ÓöĖ®ŗÜæģ·“Ó¦”££Ø×¢£ŗīę³£¼ūµÄ»ÆŗĻ¼ŪĪŖ+3ŗĶ+4£¬Ńõ»ÆŠŌ£ŗCe4+>Fe3+>I2”££©ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®īęČÜÓŚĒāµāĖįµÄ»Æѧ·½³ĢŹ½æɱķŹ¾ĪŖ£ŗCe + 4HI  CeI4 + 2H2”ü CeI4 + 2H2”ü |
| B£®ÓĆCe(SO4)2ČÜŅŗµĪ¶ØĮņĖįŃĒĢśČÜŅŗ£¬ĘäĄė×Ó·½³ĢŹ½ĪŖ£ŗCe4+ + 2Fe2+=Ce3+ + 2Fe3+ |
| C£®ŌŚŅ»¶ØĢõ¼žĻĀ£¬µē½āČŪȌדĢ¬µÄCeO2ÖĘCe£¬ŌŚŅõ¼«»ńµĆīę |
D£®īęµÄĖÄÖÖŗĖĖŲ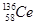 ”¢ ”¢ ”¢ ”¢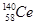 ”¢ ”¢ £¬ĖüĆĒ»„³ĘĪŖĶ¬ĖŲŅģŠĪĢå £¬ĖüĆĒ»„³ĘĪŖĶ¬ĖŲŅģŠĪĢå |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
¹ŲÓŚ·“Ó¦3Cl2 + 6KOH 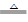 KClO3 + 5KCl + 3H2O£¬ŅŌĻĀĖµ·ØÕżČ·µÄŹĒ
KClO3 + 5KCl + 3H2O£¬ŅŌĻĀĖµ·ØÕżČ·µÄŹĒ
| A£®KOH¼Č²»ŹĒŃõ»Æ¼Į£¬ÓÖ²»ŹĒ»¹Ō¼Į |
| B£®Cl2ŹĒŃõ»Æ¼Į£¬KOHŹĒ»¹Ō¼Į |
| C£®3molĀČĘų²Ī¼Ó·“Ó¦×ŖŅĘ6 molµē×Ó |
| D£®±»Ńõ»ÆµÄĀČŌŖĖŲµÄÖŹĮæĪŖ±»»¹ŌµÄĀČŌŖĖŲÖŹĮæµÄ5±¶ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ĻĀĮŠ±ä»ÆÖŠ£¬ŹōÓŚ»¹Ō·“Ó¦µÄŹĒ
| A£®Cl£”śCl2 | B£®FeCl2”śFeCl3 | C£®C”śCO2 | D£®KMnO4”śMnO2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
½«“ÅŠŌŃõ»ÆĢś·ÅČėĻ”HNO3ÖŠæÉ·¢ÉśČēĻĀ·“Ó¦£ŗ
3Fe3O4+28HNO3= 9Fe(NO3)x+NO”ü+14H2O£¬ĻĀĮŠÅŠ¶ĻŗĻĄķµÄŹĒ
| A£®Fe(NO3)xÖŠµÄxĪŖ2 |
| B£®Ļ”HNO3ŌŚ·“Ó¦ÖŠÖ»±ķĻÖŃõ»ÆŠŌ |
| C£®“ÅŠŌŃõ»ÆĢśÖŠµÄĖłÓŠĢśŌŖĖŲČ«²æ±»Ńõ»Æ |
| D£®·“Ó¦ÖŠĆ滹Ō0.3molŃõ»Æ¼Į£¬¾ĶÓŠ0.9molµē×Ó×ŖŅĘ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ŅŃÖŖŌŚĖįŠŌČÜŅŗÖŠµÄ»¹ŌŠŌĒæČõĖ³ŠņĪŖ£ŗSO2 £¾IØC£¾H2O2£¾Fe2£«£¾ClØC£¬ĻĀĮŠ·“Ó¦²»æÉÄÜ·¢ÉśµÄŹĒ£ŗ
| A£®H2O2+ H2SO4£½SO2”ü+ O2”ü+2 H2O |
| B£®2IØC +2Fe3£«£½I2+2 Fe2£« |
| C£®2Fe3£«+ SO2 +2H2O£½2Fe2£«+SO42ØC +4H£« |
| D£®SO2 +2 H2O+ I2£½H2SO4+2HI |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
“ÓŃõ»Æ»¹Ō½Ē¶Č·ÖĪö£¬ĻĀĮŠ·“Ó¦ÖŠĖ®µÄ×÷ÓĆĻąĶ¬µÄŹĒ £Ø £©
¢Ł NaŗĶH2O ¢Ś NO2ŗĶH2O ¢Ū Cl2ŗĶH2O ¢Ü Na2O2ŗĶH2O
| A£®¢Ł¢Ś¢Ū | B£®¢Ł¢Ś¢Ü | C£®¢Ł¢Ū¢Ü | D£®¢Ś¢Ū¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
¶ŌÓŚ°×Į×ŅżĘšµÄÖŠ¶¾£¬ĮņĖįĶČÜŅŗŹĒŅ»ÖÖ½ā¶¾¼Į£¬ÓŠ¹Ų·“Ó¦ČēĻĀ£ŗ1lP£«15CuSO4£«24H2O£½5Cu3P£«6H3PO4£«15H2SO4£¬ĻĀĮŠ¹ŲÓŚøĆ·“Ó¦Ėµ·Ø“ķĪóµÄŹĒ£ŗ
| A£®Éś³É1 mol H3PO4Ź±£¬ÓŠ5 molµē×Ó×ŖŅĘ |
| B£®5molCuSO4²Ī¼Ó·“Ó¦Ź±£¬±»Ńõ»ÆµÄPĪŖ1mol |
| C£®Ńõ»Æ²śĪļŗĶ»¹Ō²śĪļµÄĪļÖŹµÄĮæÖ®±ČĪŖ6£ŗ5 |
| D£®6molH3PO4Éś³ÉŹ±£¬±»CuSO4Ńõ»ÆµÄPĪŖ3mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
Ēā»ÆŃĒĶ£ØCuH£©ŹĒŅ»ÖÖÄŃČÜĪļÖŹ£¬ÓĆCuSO4ČÜŅŗŗĶ”°ĮķŅ»ÖÖ·“Ó¦Īļ”±ŌŚ40”ę~50”ꏱ·“Ó¦æÉÉś³ÉĖü”£CuH²»ĪČ¶Ø£¬Ņ×·Ö½ā£»CuHŌŚĀČĘųÖŠÄÜČ¼ÉÕ£»øśŃĪĖį·“Ó¦ÄܲśÉśĘųĢ壬ŅŌĻĀÓŠ¹ŲµÄĶʶĻÖŠ“ķĪóµÄŹĒ
| A£®”°ĮķŅ»ÖÖ·“Ó¦Īļ”±Ņ»¶Ø¾ßÓŠ»¹ŌŠŌ |
| B£®CuH¼ČæÉ×öŃõ»Æ¼ĮŅ²æÉ×ö»¹Ō¼Į |
| C£®CuH+Cl2=CuCl+HCl£ØČ¼ÉÕ£© |
| D£®CuH+HCl=CuCl+H2”ü£Ø³£ĪĀ£© |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com