
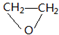 ��
��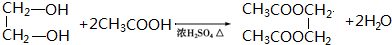 ��
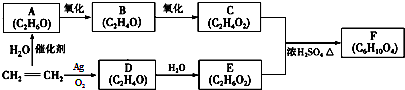
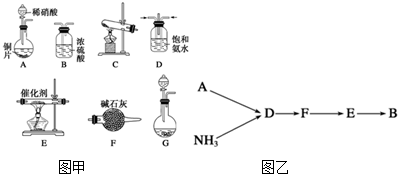
������ ��ϩ��ˮ�ӳ�����A��AΪ�Ҵ����Ҵ�����������B��BΪ��ȩ����ȩ����������CΪ���ᣬ��ϩ��������Ӧ����D��C2H4O����DΪ��������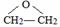 ����Ϊ����������Ҫ�����ᷢ��������Ӧ��1��2��Ӧ��D��E�ǿ����ӳɷ�Ӧ����EΪ�Ҷ������Ҷ��������ᷴӦ����F��C6H10O4����FΪ�������Ҷ���
����Ϊ����������Ҫ�����ᷢ��������Ӧ��1��2��Ӧ��D��E�ǿ����ӳɷ�Ӧ����EΪ�Ҷ������Ҷ��������ᷴӦ����F��C6H10O4����FΪ�������Ҷ���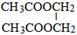 ���ݴ˽��
���ݴ˽��
��� �⣺��ϩ��ˮ�ӳ�����A��AΪ�Ҵ����Ҵ�����������B��BΪ��ȩ����ȩ����������CΪ���ᣬ��ϩ��������Ӧ����D��C2H4O����DΪ��������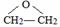 ����Ϊ����������Ҫ�����ᷢ��������Ӧ��1��2��Ӧ��D��E�ǿ����ӳɷ�Ӧ����EΪ�Ҷ������Ҷ��������ᷴӦ����F��C6H10O4����FΪ�������Ҷ���
����Ϊ����������Ҫ�����ᷢ��������Ӧ��1��2��Ӧ��D��E�ǿ����ӳɷ�Ӧ����EΪ�Ҷ������Ҷ��������ᷴӦ����F��C6H10O4����FΪ�������Ҷ���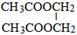 ��
��
��1�������Ϸ�����֪BΪ��ȩ������ȩ�����ʴ�Ϊ��ȩ����
��2�������Ϸ�����֪DΪ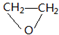 ���ʴ�Ϊ��
���ʴ�Ϊ��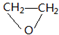 ��
��
��3���Ҷ��������ᷴӦ���ɶ������Ҷ���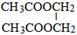 ������ʽΪ
������ʽΪ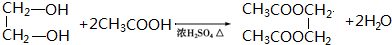 ��
��
�ʴ�Ϊ��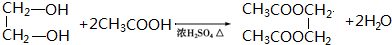 ��
��
��4���Ҵ���ͬ���칹��ΪCH3OCH3���ʴ�Ϊ��CH3OCH3��
��5���Ҵ������ǻ��������Ʒ�Ӧ�����������ɿ����Ƽ����Ҵ��Ͷ����ѣ��ʴ�Ϊ��A��
���� ���⿼���л��ƶϣ��漰ϩ��������ȩ������������Լ�ѧ�����������ȣ��Ƕ��л�������֪ʶ���ۺϿ��飬�ܽϺõĿ��鿼����˼ά������������ϩ��D�ķ���ʽ�����E�����ᷴӦ����F����������Cԭ����Ŀ���ж�D�Ľṹ�ǽ���Ĺؼ����Ѷ��еȣ��Ǹ߿��ȵ����ͣ�


 �������ϵ�д�
�������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ���� | B�� | �������� | C�� | ���� | D�� | ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����һ�ֺ��ط�����8O | |
| B�� | 1Hԭ�Ӻ�����1������ | |
| C�� | O2��O3��Ϊͬλ�� | |
| D�� | ͨ������£�He��N2��ѧ���ʶ����ȶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
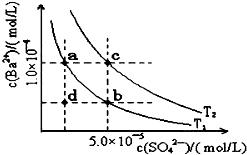 ��֪BaSO4��s��?Ba2+��aq��+SO4 2-��aq����25��ʱKsp=1.07��10-10����BaSO4�����¶����߶�������ͼ��ʾ����T1��T2��ͬ�¶�������BaSO4��ˮ�еij����ܽ�ƽ�����ߣ�������˵������ȷ���ǣ�������
��֪BaSO4��s��?Ba2+��aq��+SO4 2-��aq����25��ʱKsp=1.07��10-10����BaSO4�����¶����߶�������ͼ��ʾ����T1��T2��ͬ�¶�������BaSO4��ˮ�еij����ܽ�ƽ�����ߣ�������˵������ȷ���ǣ�������| A�� | �¶�ΪT1ʱ����T1�����Ϸ���������һ��ʱ������BaSO4�������� | |
| B�� | �����ܼ�����ʹ��Һ��d���ΪT1������a��b֮���ijһ�� | |
| C�� | ���¿�ʹ��Һ��b���Ϊd�� | |
| D�� | T2��25�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 73 | B�� | 74 | C�� | 75 | D�� | 76 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ˮ | B�� | ����ͭ | C�� | ���� | D�� | �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ۼ������Ȼ�����Һ�� Fe+Fe3+�T2Fe2+ | |
| B�� | Cl2��ˮ�ķ�ӦCl2+H2O�T2H++Cl-+ClO- | |
| C�� | ͭƬ������������Һ��Cu+Ag+�TCu2++Ag | |
| D�� | ����ʯ���ڴ���ķ�ӦCaCO3+2CH3COOH�TCa2++2CH3COO-+CO2��+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
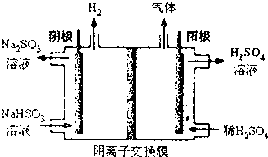 �����ѣ�CH3OCH4����һ����Ҫ�����ȼ�ϣ���ҵ������ˮú���ϳɶ����ѵ�������Ӧ���£�
�����ѣ�CH3OCH4����һ����Ҫ�����ȼ�ϣ���ҵ������ˮú���ϳɶ����ѵ�������Ӧ���£��鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com