
反应速率v和反应物浓度的关系是用实验方法测定的。化学反应H2+Cl2===2HCl的反应速率v可表示为v=k[H2]m[Cl2]n,式中k为常数,m、n值可用下表中数据确定。
| [H2]/mol·L-1 | [Cl2]/ mol·L-1 | v/mol·L-1·s-1 |
| 1.0 | 1.0 | 1.0 k |
| 2.0 | 1.0 | 2.0 k |
| 2.0 | 4.0 | 4.0 k |
由此可推得,m、n值正确的是( )
A.m=1、n=1 B.m=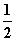 、n=
、n=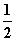
C.m=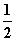 、n=1 D.m=1、n=
、n=1 D.m=1、n=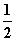
科目:高中化学 来源: 题型:
在以下性质的比较中,正确的是
A.微粒半径:O2-<F-<Na+<Li+ B.第一电离能:C < N < O
C.分子中的键角:CH4>H2O>CO2 D.共价键的键能:C-C < C=C < C≡C
查看答案和解析>>
科目:高中化学 来源: 题型:
某天然拒食素具有防御非洲大群蚯蚓的作用,其结构简式如图所示(未表示出原子或原子团的空间排列)。该拒食素与下列某试剂充分反应,所得有机物分子的官能团数目增加,则该试剂是( )。
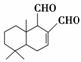
A.Br2的CCl4溶液 B.Ag(NH3)2OH溶液
C.HBr D.H2
查看答案和解析>>
科目:高中化学 来源: 题型:
目前钢铁是日常生活中使用最广泛的金属,下列关于铁的一些说法正确的是( )。
A.常温下浓硫酸与铁不反应,故常温下可用铁制容器贮藏贮运浓硫酸
B.铁是较活泼的金属,它与卤素(X2)反应的生成物均为FeX3
C.Fe(OH)2易被氧化成Fe(OH)3,说明稳定性:Fe(OH)2<Fe(OH)3
D.Fe3O4溶解于盐酸既有FeCl2又有FeCl3生成,故Fe3O4属于混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
由熔盐电解法获得的粗铝含一定量的金属钠和氢气,这些杂质可采用吹气精炼法除去,产生的尾气经处理后可用于钢材镀铝。工艺流程如下:
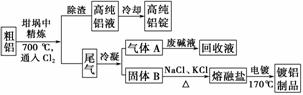
(注:NaCl熔点为801 ℃;AlCl3在181 ℃升华)
(1)精炼前,需清除坩埚表面的氧化铁和石英砂,防止精炼时它们分别与铝发生置换反应产生新的杂质,相关的化学方程式为①____________________________________________________________和
②____________________________________________________________。
(2)将Cl2连续通入坩埚中的粗铝熔体,杂质随气泡上浮除去。气泡的主要成分除Cl2外还含有________;固态杂质粘附于气泡上,在熔体表面形成浮渣,浮渣中肯定存在________。
(3)在用废碱液处理气体A的过程中,所发生反应的离子方程式为____________________________________________________________。
(4)镀铝电解池中,金属铝为________极,熔融盐电镀液中铝元素和氯元素主要以AlCl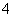 和Al2Cl
和Al2Cl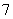 形式存在,铝电极的主要电极反应式为____________________________________________________________。
形式存在,铝电极的主要电极反应式为____________________________________________________________。
(5)钢材镀铝后,表面形成的致密氧化铝膜能防止钢材腐蚀,其原因是____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
设C(s)+CO2(g)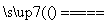 2CO(g)(ΔH=Q1 kJ·mol-1)反应速率为v1,N2(g)+3H2(g)
2CO(g)(ΔH=Q1 kJ·mol-1)反应速率为v1,N2(g)+3H2(g)
 2NH3(g)(ΔH=-Q2 kJ·mol-1)反应速率为v2,对于上述两个反应,当温度升高时,v1和v2的变化情况为( )
2NH3(g)(ΔH=-Q2 kJ·mol-1)反应速率为v2,对于上述两个反应,当温度升高时,v1和v2的变化情况为( )
A.同时增大 B.同时减小
C.v1增大,v2减小 D.v1减小,v2增大
查看答案和解析>>
科目:高中化学 来源: 题型:
在容积不变的密闭容器中存在如下反应:2SO2(g)+O2(g) 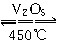 2SO3(g) ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是( )
2SO3(g) ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是( )

A.图Ⅰ表示的是t1时刻增大O2的浓度对反应速率的影响
B.图Ⅱ表示的是t1时刻加入催化剂后对反应速率的影响
C.图Ⅲ表示的是催化剂对平衡的影响,且甲的催化效率比乙高
D.图Ⅲ表示的是压强对化学平衡的影响,且乙的压强较高
查看答案和解析>>
科目:高中化学 来源: 题型:
关于工业合成氨的叙述中,错误的是( )
A.在动力、设备、材料允许的情况下,反应尽可能在高压下进行
B.温度越高越有利于工业合成氨
C.在工业合成氨中N2、H2的循环利用可提高其利用率,降低成本
D.及时从反应体系中分离出氨气有利于平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法或表述正确的是________(填序号)。
①(四川理综,4D)将FeCl3溶液加入Mg(OH)2悬浊液中,振荡,可观察到沉淀由白色变为红褐色
②(天津理综,3B)NH4F水溶液中含有HF,因此NH4F溶液不能存放于玻璃试剂瓶中
③(重庆理综,3D)25 ℃时Cu(OH)2在水中的溶解度大于其在Cu(NO3)2溶液中的溶解度
④(安徽理综,12D)溶解度小的沉淀易向溶解度更小的沉淀转化,ZnS沉淀中滴加CuSO4溶液可以得到CuS沉淀
⑤(江苏,11C)加热0.1 mol·L-1 Na2CO3溶液,CO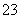 的水解程度和溶液的pH均增大
的水解程度和溶液的pH均增大
⑥(北京理综,9A)测0.1 mol·L-1氨水的pH为11:NH3·H2ONH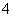 +OH-
+OH-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com