
能正确表示下列反应的离子方程式的是
A、NH4HSO3溶于过量的NaOH溶液中:HSO3-+OH-=SO32-+H2O
B、向NaAlO2溶液中通入过量CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-
C、Fe3O4与稀硝酸反应:Fe3O4+8H+=2Fe3++Fe2++4H2O
D、酸性KMnO4溶液与双氧水溶液反应:2MnO4- +5H2O2+6H+=2Mn2++5O2 ↑+8H2O
科目:高中化学 来源: 题型:
已知反应A2(g)+2B2(g)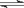 2AB2(g)△H <0,下列说法正确的
2AB2(g)△H <0,下列说法正确的
A.升高温度,正向反应速率增加,逆向反应速率减小
B.升高温度有利于反应速率增加,从而缩短达到平衡的时间
C.达到平衡后,升高温度或增大压强都有利于该反应平衡正向移动
D.达到平衡后,降低温度或减小压强都有利于该反应平衡正向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
如图锥形瓶中盛有气体X,滴管内盛有液体Y。若挤压滴管头,使Y滴入瓶中,振荡,过一会儿可见小气球a鼓起。气体X和液体Y不可能是( )
A.X是NH3、Y是水 B.X是NO2、Y是NaOH溶液
C.X是CO2、Y是稀硫酸 D.X是HCl、Y是NaNO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
有一混合溶液,其中只含有Fe2+、Cl-、Br-、I-(忽略水的电离),其中Cl-、Br-、I-的个数比为2∶3∶4,向该溶液中通入氯气,使溶液中Cl-和Br-的个数比为3∶1,则通入氯气的物质的量与溶液中剩余的Fe2+的物质的量之比为(还原性I->Fe2+>Br->Cl-)( )
A.7∶1 B.7∶2 C.7∶3 D.7∶4
查看答案和解析>>
科目:高中化学 来源: 题型:
研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2-CaO作电解质,利用如图所示装置获得金属钙,并以钙为还原剂,还原二氧化钛制备金属钛。下列正确的是:
A、由TiO2制得1mol 金属Ti ,理论上外电路转移2NA电子
B、阳极的电极反应式为:C + 2O2- - 4e- == CO2↑
C、若用铅蓄电池作该装置的供电电源,“ +”接线柱应连接Pb电极
D、在制备金属钛前后,整套装置中CaO的总量减少
查看答案和解析>>
科目:高中化学 来源: 题型:
环氧乙烷的化学式为C2H4O,关于环氧乙烷的下列说法正确的是
A、它是氧化物 B、它是含有3种元素的混合物
C、它的摩尔质量是44g D常温下,1 mol环氧乙烷含有2NA个碳原子
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于金属钠的叙述中,正确的是
A.钠暗灰色固体
B.将金属钠在空气中加热则生成白色固体
C.钠投入到Fe2(SO4)3溶液中,钠先与H2O反应,钠投入到稀H2SO4中,钠也是先与H2O反应
D.钠钾合金在室温下呈液态,可用做原子反应堆的导热剂
查看答案和解析>>
科目:高中化学 来源: 题型:
有100 mL 3 mol/L的氢氧化钠溶液和100 mL 1 mol/L的氯化铝溶液。按如下两种方法进行实验:①将氢氧化钠溶液分多次加入到氯化铝溶液中;②将氯化铝溶液分多次加入到氢氧化钠溶液中。比较两次实验的结果是( )
A.现象相同,最终沉淀量相等
B.现象不同,最终沉淀量不相等
C.现象相同,最终沉淀量不相等
D.现象不同,最终沉淀量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
某强酸性溶液X中可能含有Fe2+、A13+、NH4+、CO32—、SO32—、SO42—、C1—中的若干种,现取X溶液进行连续实验,实验过程及产物如下:
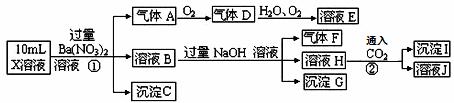
下列说法正确的是( )
A.X中肯定存在Fe2+、NH4+、SO42— B.溶液E和气体F不能发生化学反应
C.X中肯定不存在CO32—、SO32—、C1— D.沉淀I是A1(OH)3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com