
【题目】如表为长式周期表的一部分,其中的编号代表对应的元素. 
请回答下列问题:
(1)科学家发现,②、④、⑨三种元素的原子形成的晶体具有超导性,其晶胞的结构特点如图所示(图中②、④、⑨分别位于晶胞的体心、顶点、面心),则该化合物的化学式为(用对应的元素符号表示).
(2)某元素的价电子排布式为nsnnpn+1 , 该元素与元素①形成的18电子的X分子的结构式为;该元素还可与元素①形成10电子的气体分子Y,将过量的Y气体通入盛有含⑩元素的硫酸盐溶液中,反应过程中的实验现象为 .
(3)比较③,⑤,⑥,⑦,⑧五种元素的电负性大小,由大到小排列的顺序为(用 元素符号表示).
(4)⑩元素单质晶体采取堆积方式 , 空间利用率为 . 
【答案】
(1)MgNi3C
(2)![]() ;先产生蓝色沉淀,然后沉淀溶解,变成深蓝色溶液
;先产生蓝色沉淀,然后沉淀溶解,变成深蓝色溶液
(3)Ca<Al<S<Cl<O
(4)面心立方最密堆积;74%
【解析】解:由元素周期表可以得出元素①为H,②为C,③为O,④为Mg,⑤为Mn,⑥为S,⑦为Cl,⑧为Ca,⑨为Ni,⑩为Cu;
(1.)②、④、⑨分别位于晶胞的体心、顶点、面心,C原子个数为1,Mg原子个数为8× ![]() =1,Ni原子个数为6×
=1,Ni原子个数为6× ![]() =3,化学式为MgNi3C,所以答案是:MgNi3C;
=3,化学式为MgNi3C,所以答案是:MgNi3C;
(2.)元素的特征电子排布式为nsnnpn+1 , 则n=2,故该元素的特征电子排布式为2s22p3 , 为N原子,元素与元素①形成的18电子的X分子为N2H4 , 其结构式为 ![]() ;元素①为H元素,与X形成的物质为NH3 , 与硫酸铜溶液先生成蓝色沉淀,后形成络合物,则观察到的现象为先产生蓝色沉淀,然后沉淀溶解,变成深蓝色溶液,所以答案是:
;元素①为H元素,与X形成的物质为NH3 , 与硫酸铜溶液先生成蓝色沉淀,后形成络合物,则观察到的现象为先产生蓝色沉淀,然后沉淀溶解,变成深蓝色溶液,所以答案是: ![]() ;先产生蓝色沉淀,然后沉淀溶解,变成深蓝色溶液;
;先产生蓝色沉淀,然后沉淀溶解,变成深蓝色溶液;
(3.)非金属性越强,电负性越大,则电负性从小到大顺序是Ca<Al<S<Cl<O,所以答案是:Ca<Al<S<Cl<O;
(4.)Cu单质的晶体堆积方式为面心立方密堆积,晶胞中Cu原子数目为8× ![]() +6×
+6× ![]() =4,设Cu原子半径为r,则晶胞中Cu原子总体积为4×
=4,设Cu原子半径为r,则晶胞中Cu原子总体积为4× ![]() πr3 , 设Cu原子半径为r,则晶胞棱长为4r×
πr3 , 设Cu原子半径为r,则晶胞棱长为4r× ![]() =2
=2 ![]() r,晶胞体积为(2
r,晶胞体积为(2 ![]() r)3=16
r)3=16 ![]() r3 , 空间利用率=
r3 , 空间利用率= ![]() ×100%=74%,所以答案是:面心立方最密堆积;74%.
×100%=74%,所以答案是:面心立方最密堆积;74%.


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
【题目】某溶液含有Fe3+、Al3+、Ba2+、Ag+、K+五种阳离子,现用过量的H2SO4、NaOH、NH3·H2O、NaCl四种溶液,按图所示步骤分开五种离子。下列判断正确的是

A.沉淀乙是氢氧化铝和氢氧化银的混合物
B.溶液3中含有Al3+
C.试剂①是NaCl,试剂④是H2SO4
D.溶液4含有三种阳离子,分别是H+、Na+、K+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含氟的卤素互化物通常作氟化剂,使金属氧化物转化为氟化物,如2Co3O4+6C1F3= 6CoF3+3C12+4X。下列有关该反应的说法,正确的是
A. X与O3互为同位素 B. ClF3中氯元素为-3价
C. Co3O4在反应中作氧化剂 D. lmol Co3O4参加反应转移9 mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“稀土之父“徐光宪在《化学分子共和国》中介绍了许多物质,下列有关说法不正确的是
A. 固态CO2 俗称干冰,大量排放易造成温室效应
B. 碘单质“望酸碱而逃”指:碘单质遇碱歧化为I-和IO3-,再遇酸归中成碘单质
C. CO会引起煤气中毒,冬天用煤进行取暖时,在屋内放置一盆水,就可以有效防止中毒
D. NO自述“诞生在闪电的弧光中,强大的能量造就了我”指:高压放电情况下,N2和O2生成NO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据已学知识,请你回答下列问题:
(1)写出原子序数最小的第Ⅷ族元素原子的原子结构示意图 .
(2)写出3p轨道上有2个未成对电子的元素的符号: .
(3)该元素被科学家称之为人体微量元素中的“防癌之王”,其原子的外围电子排布式为4s24p4 , 该元素的名称是 .
(4)已知下列化学键的键能:Si﹣O:460kJ/mol,Si﹣Si:175kJ/mol,O=O:498kJ/mol,则反应:Si+O2=SiO2的反应热△H= .
(5)写出二氧化硫和水合氢离子中S原子,O原子分别采用和杂化形式,其空间构型分别为和 .
(6)用氢键表示法表示HF水溶液中的所有氢键、、、 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】摩尔浓度相同的三种盐NaX、NaY和NaZ的溶液,其中pH值依次为8、9、10,则HX、HY、HZ的酸性由强到弱的顺序是( )
A.HX、HZ、HY
B.HZ、HY、HX
C.HX、HY、HZ
D.HY、HZ、HX
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以氯乙烷为原料制备1,2﹣二溴乙烷,下列方案中合理的是( )
A.CH3CH2Cl ![]() CH3CH2OH
CH3CH2OH ![]() CH2=CH2
CH2=CH2 ![]() CH2BrCH2Br
CH2BrCH2Br
B.CH3CH2Cl ![]() CH2BrCH2Br
CH2BrCH2Br
C.CH3CH2Cl ![]() CH2=CH2
CH2=CH2 ![]() CH3CH2Br
CH3CH2Br ![]() CH2BrCH2Br
CH2BrCH2Br
D.CH3CH2Cl ![]() CH2=CH2
CH2=CH2 ![]() CH2BrCH2Br
CH2BrCH2Br
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂-液态多硫电池具有能量密度高、储能成本低等优点,以熔融金属银、熔融硫和多硫化锂分别作两个电极的反应物,固体Al2O3陶瓷(可传导Li+)为电解质,其反应原理如图所示。下列关于其说法错误的是
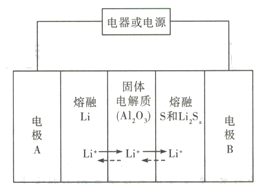
A. 放电时,电极B为正极
B. 充电时内电路中Li+的移动方向为从B到A
C. 该电池的适宜工作温度应该在Al2O3的熔点和沸点之间
D. 充电时,阳极反应为Sx2--2e-=xS
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳、 氮、磷、砷和硼的相关化合物在化工、医药、农药、材料等领域有着广泛的应用。锂、钠、铝、铁等金属在日常生活、工业生产中也占有举足轻重的地位,请回答下列问题:
(1)基态As原子的电子排布式为[Ar]______________________;
(2)氮化硼(BN)有多种晶型,其中立方氮化硼与金刚石的构型类似,则其晶胞中B—N—B之间的夹角是___________________(填角度)。
(3)砷化硼(BAs)是ⅢA一VA族半导体材料的重要成员之一,其晶体结构与金刚石相似。
①BAs晶体中,每个As与____________个B相连,As的杂化形式为_______________;
②已知B原子的电负性比As原子的电负性大,则As与B之间存在的化学键有____________(填字母)。
A.离子键 B.金属键 C.极性键 D.氢键 E.配位键 F.σ键 G.π键
(4)铁的另一种配合物Fe(CO)5熔点为-20.5℃,沸点为103℃,易溶于CCl4,据此可以判断Fe(CO)5晶体属于________________________________(填晶体类型)。
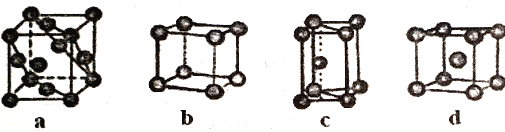
(5)金属晶体的四种堆积如下图,金属钠的晶体堆积模型为___________(填字母)。
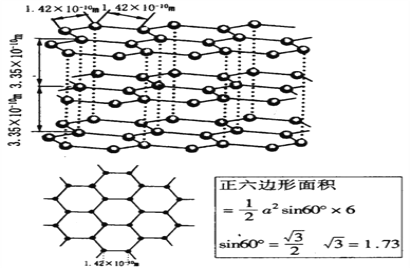
(6)石墨晶体的结构如下图,石墨的密度为________________________________(只列式不化简不计算)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com