
 M、N、O、P、Q是元素周期表中原子序数依次递增的前四周期元素.M原子最外层电子数为内层电子数的3倍;N的焰色反应呈黄色;O的氢化物是一种强酸,其浓溶液可与M、Q的化合物反应生成O的单质;P是一种金属元素,其基态原子中有6个未成对电子.请回答下列问题:
M、N、O、P、Q是元素周期表中原子序数依次递增的前四周期元素.M原子最外层电子数为内层电子数的3倍;N的焰色反应呈黄色;O的氢化物是一种强酸,其浓溶液可与M、Q的化合物反应生成O的单质;P是一种金属元素,其基态原子中有6个未成对电子.请回答下列问题:分析 M、N、O、P、Q是元素周期表中原子序数依次递增的前四周期元素.M原子最外层电子数为内层电子数的3倍,原子只能有2个电子层,最外层电子数为6,则M为氧元素;N的焰色反应呈黄色,则N为Na;O的氢化物是一种强酸,其浓溶液可与M、Q的化合物反应生成O的单质,可推知O为Cl、Q为Mn;P是一种金属元素,其基态原子中有6个未成对电子,核外电子排布为1s22s22p63s23p63d54s1,则P为Cr,据此解答.
解答 解:M、N、O、P、Q是元素周期表中原子序数依次递增的前四周期元素.M原子最外层电子数为内层电子数的3倍,原子只能有2个电子层,最外层电子数为6,则M为氧元素;N的焰色反应呈黄色,则N为Na;O的氢化物是一种强酸,其浓溶液可与M、Q的化合物反应生成O的单质,可推知O为Cl、Q为Mn;P是一种金属元素,其基态原子中有6个未成对电子,核外电子排布为1s22s22p63s23p63d54s1,则P为Cr,
(1)由上述分析可知,元素Q为锰,P是一种金属元素,其基态原子中有6个未成对电子,处于第四周期,核外电子排布为1s22s22p63s23p63d54s1,价层电子排布式为3d54s1,
故答案为:锰;3d54s1;
(2)HF分子间存在氢键,而HCl分子间无氢键,故HCl的沸点比HF的低
故答案为:HF分子间存在氢键,而HCl分子间无氢键;
(3)O、Cl元素形成的氧化物中Cl元素表现正化合价,故O原子对键合电子的吸引力更强,故电负性O>Cl,Cl的最高价含氧酸根为ClO4-,Cl原子孤电子对=$\frac{7+1-2×4}{2}$=0,价层电子对数为4,故其空间构型为 正四面体,其中心原子的杂化类型为sp3,
故答案为:O>Cl;正四面体;sp3;
(4)晶胞中Na为晶胞内部,晶胞中含有8个Na原子,O原子位于顶点与面心,晶胞中含有O原子数目为8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,故该晶胞的化学式为Na2O,以晶胞中上面心M离子为研究对象,晶胞中每个M周围最近的N离子有8个,M离子配位数为8,该晶体类型为离子晶体,
故答案为:Na2O;8;离子晶体;
(5)N离子与周围4个M离子形成正四面体结构,N、M连续处于晶胞体对角线上,NM距离为体对角线长度的$\frac{1}{4}$,晶胞的边长为a×10-10cm,则晶胞体对角线长度为$\sqrt{3}$a×10-10cm,则距离最近的M、N离子间的距离为$\frac{\sqrt{3}}{4}$×a×10-10cm,
故答案为:$\frac{\sqrt{3}}{4}$×a×10-10cm.
点评 本题是对物质结构的考查,涉及核外电子排布、电负性、分子结构、杂化轨道、晶胞结构与计算等,(3)中注意根据氧化物中化合价判断O与Cl的电负性,(5)为易错点、难点,需要学生具有一定空间想象及数学计算能力,难点中等.


科目:高中化学 来源: 题型:解答题
| 编号 | 电极材料 | 电解质溶液 | 电流计指针偏转方向 |
| 1 | Al、Mg | 稀盐酸 | 偏向Al |
| 2 | Al、Cu | 稀盐酸 | 偏向Cu |
| 3 | Al、石墨 | 稀盐酸 | 偏向石墨 |
| 4 | Al、Mg | 氢氧化钠 | 偏向Mg |
| 5 | Al、Zn | 浓硝酸 | 偏向Al |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化铝熔点高达2045℃,可用于制成坩埚熔化氢氧化钠固体 | |
| B. | HF可以用于刻蚀玻璃 | |
| C. | 镁铝合金可用作制造飞机的材料 | |
| D. | 过氧化钠可用作供氧剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化合物 | 相对分子质量 | 密度/g•cm-3 | 沸点/℃ | 溶解度/(g/100g水) |
| 正丁醇 | 74 | 0.80 | 118.0 | 9 |
| 冰醋酸 | 60 | 1.045 | 118.1 | 互溶 |
| 乙酸正丁酯 | 116 | 0.882 | 126.1 | 0.7 |
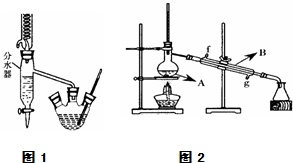
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该样品中一定含有NH4HC03和NH4Cl | |
| B. | 该样品中含N元素的质量分数为17.57% | |
| C. | 该样品若和足量烧碱反应,将消耗0.4mol NaOH | |
| D. | 根据上述数据可以确定原样品中含有5.3g NH4N03 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
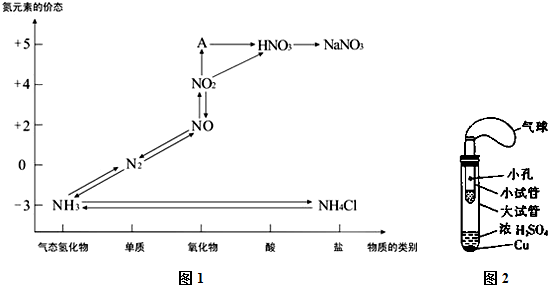
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、Fe2+、Cl-、NO${\;}_{3}^{-}$ | B. | Na+、Ba2+、Cl-、SO${\;}_{4}^{2-}$ | ||
| C. | NH${\;}_{4}^{+}$、Fe3+、Cl-、SCN- | D. | K+、Mg2+、SO${\;}_{4}^{2-}$、NO${\;}_{3}^{-}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该合金中铜与镁的物质的量之比是1:2 | |
| B. | 该浓硝酸中HNO3的物质的量浓度是14.0 mol•L-1 | |
| C. | NO2和N2O4的混合气体中,NO2的体积分数是80% | |
| D. | 得到2.54 g沉淀时,加入NaOH溶液的体积是640 mL |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com