
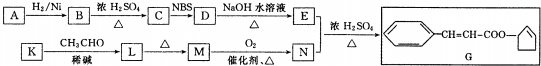
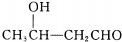
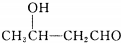 $\stackrel{△}{→}$CH3CH=CHCHO+H2O
$\stackrel{△}{→}$CH3CH=CHCHO+H2O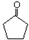 ,G中官能团的名称为碳碳双键、酯基.
,G中官能团的名称为碳碳双键、酯基.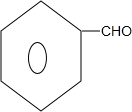 +CH3CH2OH$\stackrel{稀碱}{→}$
+CH3CH2OH$\stackrel{稀碱}{→}$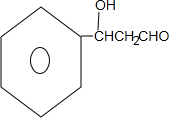 ,反应类型加成反应.
,反应类型加成反应.分析 本题采用逆推法并结合反应条件分析,G为酯,说明E与N发生酯化反应生成G,据反应条件可知,E为醇,N为酸,则E为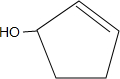 ,N为
,N为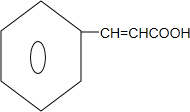 ,结合已知反应,D→E为卤代烃的水解,D为
,结合已知反应,D→E为卤代烃的水解,D为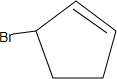 ,C→D为发生类型CH3CH2CH=CH2$\stackrel{NBS}{→}$CH3CHBrCH=CH2的反应,则C为
,C→D为发生类型CH3CH2CH=CH2$\stackrel{NBS}{→}$CH3CHBrCH=CH2的反应,则C为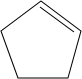 ,B→C为消去反应,B为
,B→C为消去反应,B为 ,A→B为催化加氢,A为
,A→B为催化加氢,A为 ;
;
M→N为醛基催化氧化,所以M为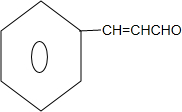 ,结合已知反应分析,L为
,结合已知反应分析,L为 ,K→L发生的是羟醛缩合反应,K为
,K→L发生的是羟醛缩合反应,K为 ,据此分析解答.
,据此分析解答.
解答 解:G为酯,说明E与N发生酯化反应生成G,据反应条件可知,E为醇,N为酸,则E为 ,N为
,N为 ,结合已知反应,D→E为卤代烃的水解,D为
,结合已知反应,D→E为卤代烃的水解,D为 ,C→D发生类似CH3CH2CH=CH2$\stackrel{NBS}{→}$CH3CHBrCH=CH2的反应,则C为
,C→D发生类似CH3CH2CH=CH2$\stackrel{NBS}{→}$CH3CHBrCH=CH2的反应,则C为 ,B→C为消去反应,B为
,B→C为消去反应,B为 ,A→B为催化加氢,A为
,A→B为催化加氢,A为 ;
;
(1)A为 ,G中含有碳碳双键、酯基,故答案为:
,G中含有碳碳双键、酯基,故答案为: ; 碳碳双键、酯基;
; 碳碳双键、酯基;
(2)M→N为醛基催化氧化生成羧基的反应,检验M已完全转化为N的实验就是检验有没有醛基,取少量M于试管中,滴加稀NaOH至溶液呈碱性,再加新制的Cu(OH)2加热,若没有砖红色沉淀产生,说明M已完全转化为N,
故答案为:取少量M于试管中,滴加稀NaOH至溶液呈碱性,再加新制的Cu(OH)2加热,若没有砖红色沉淀产生,说明M已完全转化为N(其他合理操作均可);
(3)碳碳双键遇高锰酸钾能够被氧化,常温下不能被氧气氧气,故答案为:KMnO4(H+)在氧化醛基的同时,还可以氧化碳碳双键;
(4)L为 ,K→L发生的是羟醛缩合反应,属于加成反应,K为
,K→L发生的是羟醛缩合反应,属于加成反应,K为 ,反应方程式为:
,反应方程式为: +CH3CH2OH$\stackrel{稀碱}{→}$
+CH3CH2OH$\stackrel{稀碱}{→}$ ,
,
故答案为: +CH3CH2OH$\stackrel{稀碱}{→}$
+CH3CH2OH$\stackrel{稀碱}{→}$ ;加成反应;
;加成反应;
(5)M为 ,F是M的同系物,比M多一个碳原子.①能发生银镜反应,说明含有醛基,
,F是M的同系物,比M多一个碳原子.①能发生银镜反应,说明含有醛基,
②能与溴的四氯化碳溶液加成,说明含有碳碳双键;
③苯环上有2个对位取代基,
符合上述条件的同分异构体有:甲基在一侧的CH3-C6H5-CH=CHCHO,CH3-C6H5-C(CHO)=CH2两种,醛基在一侧的OHC-C6H5-CH=CHCH3,
OHC-C6H5-CH2CH=CH2,OHC-C6H5-C(CH3)=CH2三种,碳碳双键在一侧的有:OHCCH2-C6H5-CH=CH2一种,共6种,故答案为:6;
(6)以丙烯和NBS试剂为原料制各甘油(丙三醇),流程为:CH2=CHCH3$\stackrel{NBS}{→}$CH2=CHCH2Br$\stackrel{溴水}{→}$CH2BrCHBrCH2Br$→_{加热}^{NaOH溶液}$CH2(OH)CH(OH)CH2OH,
故答案为:CH2=CHCH3$\stackrel{NBS}{→}$CH2=CHCH2Br$\stackrel{溴水}{→}$CH2BrCHBrCH2Br$→_{加热}^{NaOH溶液}$CH2(OH)CH(OH)CH2OH.
点评 本题考查了有机推断的解题思路和方法,注意反应条件的应用和已知反应的原理,题目难度较大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 原固体混合物中NaHCO3的物质的量为0.2mol | |
| B. | 固体残渣的成分为NaOH和Na2CO3的混合物 | |
| C. | 原固体混合物中NaOH和NaHCO3的物质的量之比为2﹕5 | |
| D. | 原固体混合物中加入过量盐酸会放出5.6L气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向溶液中加入石蕊试液后,呈蓝色 | |
| B. | 向溶液中加入酚酞试液后,呈红色 | |
| C. | 将溶液在试管中加热至沸腾,试管口放置的红色石蕊试纸变蓝色 | |
| D. | 将溶液中加入过量烧碱溶液加热至沸腾,试管口放置的红色石蕊试纸变蓝色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 为了减慢反应速率可用饱和食盐水代替水反应 | |
| B. | 此反应是放热反应 | |
| C. | 为了除去杂质气体,可用硫酸铜溶液 | |
| D. | 反应中需加碎瓷片作沸石 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
 在2L的恒容密闭容器中充入A(g)和B(g),发生反应:
在2L的恒容密闭容器中充入A(g)和B(g),发生反应:| 实验 序号 | 温度 | 起始物质的量 | 热量 变化 | |
| A | B | |||
| Ⅰ | 600℃ | 1 mol | 3 mol | 96 kJ |
| Ⅱ | 800℃ | 1.5 mol | 0.5 mol | -- |
| A. | 实验Ⅰ中,10 min内平均速率v(B)=0.06 mol•L-1•min-1 | |
| B. | 上述方程式中a=-160 | |
| C. | 600℃时,该反应的平衡常数是0.45 | |
| D. | 向实验Ⅱ的平衡体系中再充入0.5 mol A和1.5 mol B,A的转化率增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯与水反应生成乙醇,乙炔与氢气反应 | |
| B. | 光照下,丙烷与氯气的反应;丙炔与溴的四氯化碳溶液反应 | |
| C. | 丙烯与酸性高锰酸钾溶液反应;丁烷燃烧 | |
| D. | 乙烯生成聚乙烯,乙炔生成聚乙炔 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 如果大量苯溶入水中渗入土壤,会对周边农田、水源造成严重污染 | |
| B. | 可以采取抽吸水渠中上层液体的办法,达到部分清除泄漏物的目的 | |
| C. | 由于苯是一种易挥发、易燃的物质,周围地区如果有一个火星就可能引起爆炸 | |
| D. | 事故发生地周围比较空旷,有人提议用点火焚烧的办法来清除泄漏物,会产生大量浓烟,所以该方法未被采纳 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com