
【题目】如表为元素周期表中的一部分,表中列出10种元素在周期表中的位置,按要求回答下列各题![]() 请用对应的元素符号作答,填序号无效
请用对应的元素符号作答,填序号无效![]()
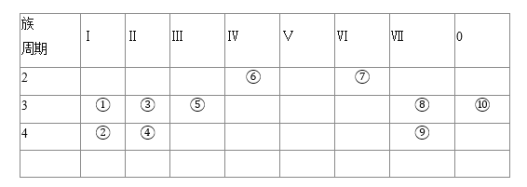
(1)化学性质最不活泼的元素符号是______,金属性最强的单质与水反应的化学方程式是______.
(2)①③⑤三种元素最高价氧化物的水化物中碱性最强的物质的化学式是______.
(3)元素①形成的稳定的氧化物在呼吸面具中供氧时的化学方程式是______,该化合物的焰色反应为______色.
(4)②③⑤三种元素形成的离子,离子半径由大到小的顺序是______.
(5)元素⑧的单质和石灰乳作用可制成有漂白和消毒作用的漂白粉,用化学方程式表示漂白粉在潮湿空气中起漂白作用的原理______.
(6)如何证明⑧和⑨元素的非金属性强弱______.
【答案】Ar ![]() NaOH
NaOH ![]() 、
、![]() 黄 ②>③>⑤
黄 ②>③>⑤ ![]() 将氯气通入NaBr溶液中,如果溶液由无色变为橙色,就说明氯气的氧化性大于溴,则非金属性
将氯气通入NaBr溶液中,如果溶液由无色变为橙色,就说明氯气的氧化性大于溴,则非金属性![]()
【解析】
根据元素在周期表中的位置知,![]() 分别是Na、K、Mg、Ca、Al、C、O、Cl、Br、Ar元素,
分别是Na、K、Mg、Ca、Al、C、O、Cl、Br、Ar元素,
(1)稀有气体化学性质最不活泼;金属性最强的金属位于周期表左下角;
(2)同一周期,金属元素的金属性随着原子序数增大而减弱,元素的金属性越强,其最高价氧化物的水化物碱性越强;
(3)作为呼吸面具中供氧剂的物质是![]() ,
,![]() 和
和![]() 、
、![]() 反应生成
反应生成![]() ;Na元素的焰色反应呈黄色;
;Na元素的焰色反应呈黄色;
(4)电子层数越多其离子半径越大,电子层结构相同的离子,离子半径随着原子序数增大而减小;
(5)元素⑧的单质是氯气,氯气和石灰乳反应是生成![]() 、
、![]() 而制取漂白粉,次氯酸钙不稳定,易和空气中
而制取漂白粉,次氯酸钙不稳定,易和空气中![]() 、
、![]() 反应生成HClO;
反应生成HClO;
(6)元素的非金属性越强,其单质的氧化性越强,根据单质之间的置换反应确定Cl、Br元素的非金属性强弱。
根据元素在周期表中的位置知,![]() 分别是Na、K、Mg、Ca、Al、C、O、Cl、Br、Ar元素,
分别是Na、K、Mg、Ca、Al、C、O、Cl、Br、Ar元素,
(1)稀有气体化学性质最不活泼,这几种元素中最不活泼的是Ar;金属性最强的金属位于周期表左下角,为K元素,K和水反应方程式为![]() ,
,
故答案为:Ar;![]() ;
;
(2)同一周期,金属元素的金属性随着原子序数增大而减弱,元素的金属性越强,其最高价氧化物的水化物碱性越强,所以这三种元素金属性最强的是Na,其最高价氧化物的水化物为NaOH,
故答案为:NaOH;
(3)作为呼吸面具中供氧剂的物质是![]() ,
,![]() 和
和![]() 、
、![]() 反应生成
反应生成![]() ,反应方程式为
,反应方程式为![]() 、
、![]() ,Na元素的焰色反应呈黄色,
,Na元素的焰色反应呈黄色,
故答案为:![]() 、
、![]() ;黄;
;黄;
(4)电子层数越多其离子半径越大,电子层结构相同的离子,离子半径随着原子序数增大而减小,所以这三种元素简单离子半径大小顺序是![]() ,
,
故答案为:②>③>⑤;
(5)元素⑧的单质是氯气,氯气和石灰乳反应是生成![]() 、
、![]() 而制取漂白粉,次氯酸钙不稳定,易和空气中
而制取漂白粉,次氯酸钙不稳定,易和空气中![]() 、
、![]() 反应生成HClO,起漂白作用的是HClO,反应方程式为:
反应生成HClO,起漂白作用的是HClO,反应方程式为:![]() ,
,
故答案为:![]() ;
;
(6)元素的非金属性越强,其单质的氧化性越强,根据单质之间的置换反应确定Cl、Br元素的非金属性强弱,其检验方法为:将氯气通入NaBr溶液中,如果溶液由无色变为橙色,就说明氯气的氧化性大于溴,则非金属性![]() ,
,
故答案为:将氯气通入NaBr溶液中,如果溶液由无色变为橙色,就说明氯气的氧化性大于溴,则非金属性![]() 。
。


 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案科目:高中化学 来源: 题型:
【题目】磷和砷的相关化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题:
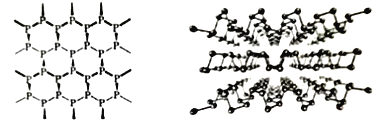
(1)黑磷是新型材料,具有类似石墨一样的片层结构(如图),层与层之间以_____结合。从结构上可以看出单层磷烯并非平面结构,但其导电性却优于石墨烯的原因是________________。
(2)四(三苯基膦)钯分子结构如下图:
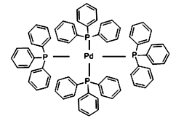
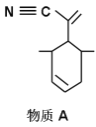
该物质可用于上图所示物质A的合成:物质A中碳原子杂化轨道类型为__________;
(3)PCl5是一种白色晶体,熔融时形成一种能导电的液体,测得其中含有一种正四面体形阳离子和一种正八面体形阴离子.(该晶体的晶胞如图所示).熔体中P-Cl的键长只有198 nm和206 nm两种,写这两种离子的化学式为______________________;正四面体形阳离子中键角_____ PCl3的键角(填> 或<或=),原因是______________________________________.
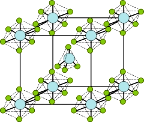
(4)PBr5气态分子的结构与PCl5相似,它的熔体也能导电,经测定知其中只存在一种P-Br键长,试用电离方程式解释PBr5熔体能导电的原因___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实,不能用勒夏特列原理解释的是
A.氯水中有下列平衡Cl2+H2 OHCl + HClO,当加入AgNO3溶液后,溶液颜色变浅
B.对2HI(g)H2(g)+I2 (g),平衡体系增大压强可使颜色变深
C.反应CO+NO2CO2+NO ΔH <0,升高温度可使平衡向逆反应方向移动
D.合成NH3反应,为提高NH3的产率,理论上应采取降低温度的措施
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用Al-PMOF可快速将芥子气降解为无毒物质,其结构如图。其中X、Y、Z为短周期元素且原子序数依次增大,X、Y同主族。下列说法正确的是

A.原子半径:Z>Y>X
B.YXZ2中Y的化合价为+5
C.含氧酸酸性:Z>Y
D.同浓度氢化物水溶液酸性:Z>Y>X
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是:

A. 图1表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化
B. 图2表示压强对可逆反应2A(g)+2B(g) ![]() 3C(g)+D(s)的影响,乙的压强大
3C(g)+D(s)的影响,乙的压强大
C. 图3表示H2与O2发生反应过程中的能量变化,则氢气的燃烧热为241.8kJ·mo1ˉ1
D. 图4表示用水稀释等体积且pH相同的盐酸和醋酸,溶液导电性:a>b>c
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧气、二氧化碳是最常见的气体。回答下列问题:
(1)宇航员呼吸产生的CO2用下列反应处理,实现空间站中的O2循环利用。镍催化剂反应:CO2(g)+4H2(g)![]() CH4(g)+2H2O(g)
CH4(g)+2H2O(g)
①已知H2(g)+![]() O2(g)
O2(g)![]() H2O(g)ΔH=-akJ·mol-1,
H2O(g)ΔH=-akJ·mol-1,
CH4(g)+2O2(g)![]() CO2(g)+2H2O(g)ΔH=-bkJ·mol-1。则镍催化剂反应的ΔH=____kJ·mol-1
CO2(g)+2H2O(g)ΔH=-bkJ·mol-1。则镍催化剂反应的ΔH=____kJ·mol-1
②空间站中所涉及的反应有:
a.镍催化剂反应:CO2(g)+4H2(g)![]() CH4(g)+2H2O(g)
CH4(g)+2H2O(g)
b.电解水反应:2H2O(l)=2H2(g)+O2(g)
c.模拟呼吸反应:C(s)+O2(g)=CO2(g)
则实现空间站O2循环总反应为____
(2)可用O2将HCl转化为Cl2,实现循环利用:O2(g)+4HCl(g)![]() 2Cl2(g)+2H2O(g)。将1molO2和4molHCl充入某恒容密闭容器中,分别在T1和T2的温度下进行实验,测得容器内总压强(p)与反应时间(t)的变化关系如图所示。
2Cl2(g)+2H2O(g)。将1molO2和4molHCl充入某恒容密闭容器中,分别在T1和T2的温度下进行实验,测得容器内总压强(p)与反应时间(t)的变化关系如图所示。

③该反应的速率v=kca(O2)·cb(HCl),k为速率常数),下列说法正确的是____(填标号)。
A.温度升高,k增大
B.使用催化剂,k不变
C.在容器中充入不反应的He,总压增大,k增大
D.平衡后再充入1molO2和4molHCl,k增大
④T1____T2(填“>”或“<”);T1时的转化率____T2时的转化率(填“>”“=”或“<”)。
⑤T1时,HCl的平衡转化率=____;T2反应的Kx=____(Kx为以物质的量分数表示的平衡常数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验事实得出的相应结论不正确的是
选项 | 事实 | 结论 |
A | 其他条件相同,Na2S2O3溶液和H2SO4溶液反应,升高溶液的温度,析出硫沉淀所需时间缩短 | 当其他条件不变时,升高反应温度,化学反应速率加快 |
B | 向2.0 mL浓度均为0.1 mol·L-1的KCl、KI混合溶液中滴加1~2滴0.01 mol·L-1AgNO3溶液,振荡,沉淀呈黄色 | Ksp:AgCl>AgI |
C | 2NO2(g) | 加压平衡向着气体颜色加深的方向移动 |
D | 将MgCl2溶液蒸干后灼烧,得到MgO固体 | 蒸干的过程中水解生成的HCl挥发,水解进一步促进生成Mg(OH)2,灼烧后产生MgO |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数,下列叙述中正确的是( )
A.常温常压下,11.2LCO2所含的原子数为1.5NA
B.常温下,46gNO2和N2O4的混合物中含有的氮原子数为NA
C.1L0.5mol·L-lFeCl3溶液完全转化可制得0.5NA个Fe(OH)3胶粒
D.1molNa被完全氧化生成Na2O2,失去2NA个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一种矿石,经测定含有镁、硅、氧三种元素且它们的质量比为12∶7∶16。
(1)用盐的组成表示其化学式: ___________。
(2)用氧化物的组成表示其化学式: _______。
(3)该矿石的成分属于________(填物质的分类)。
(4)写出该矿石(氧化物形式)与盐酸反应的化学方程式: ______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com