
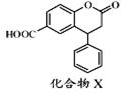
| A. | 可以与饱和Na2CO3溶液反应 | |
| B. | 分子中两个苯环一定处于同一平面 | |
| C. | 在酸性条件下水解,水解产物只有一种 | |
| D. | 1 mol化合物X最多能与3 mol NaOH反应 |
分析 分子中含-COOH、碳碳双键、-COOC-,结合羧酸、烯烃、酯的性质来解答.
解答 解:A.含有羧基,具有酸性,可与饱和Na2CO3溶液反应,故A正确;
B.苯环为平面结构,2个苯环直接的亚甲基、次甲基均为四面体构型,则两个苯环不一定处于同一平面,故B错误;
C.为环酯,水解产物只有一种,故C正确;
D.含-COOH、-COOC-及水解生成的酚-OH均与NaOH反应,则加热条件下1 mol X最多能与3molNaOH反应,故D正确.
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、有机反应为解答的关键,侧重分析与应用能力的考查,注意羧酸、烯烃、酯的性质及应用,题目难度不大.


 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol•L-1的NaCl溶液是指由1 mol NaCl和1 000 mL水配制成的溶液 | |
| B. | 从1 L 0.5 mol•L-1的NaCl溶液中取出100 mL,剩余溶液物质的量浓度为0.45 mol•L-1 | |
| C. | 0℃时,2 mol Cl2的体积可能为22.4 L | |
| D. | CaCl2的摩尔质量是111 g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 反应时间/min | n(CO)/mol | n(H2O)/mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.20 | |
| t2 | 0.80 |
| A. | 反应在 t1min 内的平均反应速率为υ(CO2)=0.40/t1mol/(L•min) | |
| B. | 到 t1min 时,反应未达到平衡状态 | |
| C. | 温度升至 800℃时,上述反应的平衡常数为 0.64,则正反应为放热反应 | |
| D. | 保持 700℃不变,向平衡体系中再通入 0.60 mol CO 和 0.30 mol H2O,达到新的平衡,与原平衡相比,CO的转化率增大,H2的体积分数增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入NH4HS固体 | B. | 压强、温度不变,充入少量氩气 | ||
| C. | 容积、温度一定,充入氦气 | D. | 温度、容积一定,充入H2S气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用浓盐酸与铁屑反应制取H2:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2═2Mn2++5O2↑+8H2O | |
| C. | 用醋酸除去水垢:CaCO3+2CH3COOH═Ca2++2CH3COO-+H2O+CO2↑ | |
| D. | 将氯气溶于水制备次氯酸:Cl2+H2O═2H++Cl-+ClO- |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | a克CH4在氧气中完全燃烧,将其产物全部跟足量的过氧化钠完全反应,反应后固体质量恰好也增加a克 | |
| B. | 将等物质的量的Na2O和Na2O2分别投入到足量且等质量的水中,得到溶质质量分数相等 | |
| C. | 1mol Na2O2与2mol NaHCO3固体混合后,在密闭容器中加热充分反应,排出气体物质后冷却,残留的固体物质是Na2CO3 | |
| D. | 向某溶液中加入氯水,然后再加入KSCN溶液变红色,说明原溶液中含有Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3 | B. | 5 | C. | 4 | D. | 7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com