
分析 (1)钠与水反应生成氢氧化钠和氢气;
(2)氯气与氢氧化钠反应生成氯化钠、次氯酸钠和水;
(3)加热碳酸氢钠固体生成碳酸钠、水和二氧化碳;
(4)过氧化钠和二氧化碳的反应生成碳酸钠和氧气;
(5)碳酸氢钠和氢氧化钠水溶液的反应生成碳酸钠和水.
解答 解:(1)钠与水反应生成氢氧化钠和氢气,离子方程式:2Na+2H2O=2OH-+2Na++H2↑,
故答案为:2Na+2H2O=2OH-+2Na++H2↑;
(2)氯气与氢氧化钠反应生成氯化钠、次氯酸钠和水,反应的离子方程式:Cl2+2OH-=Cl-+ClO-+H2O;
故答案为:Cl2+2OH-=Cl-+ClO-+H2O;
(3)加热碳酸氢钠固体生成碳酸钠、水和二氧化碳,反应的离子方程式:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑;
故答案为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑;
(4)过氧化钠和二氧化碳的反应生成碳酸钠和氧气,反应的离子方程式:2Na2O2+2CO2═2Na2CO3+O2;
故答案为:2Na2O2+2CO2═2Na2CO3+O2;
(5)碳酸氢钠和氢氧化钠水溶液的反应生成碳酸钠和水,反应的离子方程式:HCO3-+OH-=H2O+CO32-;
故答案为:HCO3-+OH-=H2O+CO32-.
点评 本题考查了化学方程式、离子方程式的书写,明确反应原理及产物是解题关键,注意原子个数、电荷数守恒.


 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:选择题
| A. | ②③④⑥ | B. | ②③④⑤ | C. | ①②③④⑤ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 正反应速率加快 | B. | 正反应速率减慢 | C. | 逆反应速率加快 | D. | 无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CuO→CuCl2 | B. | K2SO4→KCl | C. | CaCO3→CaCl2 | D. | Mg(OH)2→MgCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 18 g水中所含电子的物质的量为10 mol | |
| B. | N2和CO的摩尔质量相等,都是28 | |
| C. | 1 mol CO2的质量为44 g•mol-1 | |
| D. | 硫酸和磷酸的摩尔质量均为98 g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
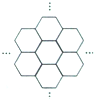 据报道,科学家己经研制出世界上最薄的材料一-碳膜片,其厚度只有一根头发的二十万分之一.如图所示,这种碳膜片状如蜂巢,是由碳原子构成的六边形单元向外延展而成,下列有关碳膜片的说法中,正确的是( )
据报道,科学家己经研制出世界上最薄的材料一-碳膜片,其厚度只有一根头发的二十万分之一.如图所示,这种碳膜片状如蜂巢,是由碳原子构成的六边形单元向外延展而成,下列有关碳膜片的说法中,正确的是( )| A. | 碳膜片属于碳元素的同素异形体 | |
| B. | 碳膜片与C60是同一种物质 | |
| C. | 碳膜片属于人工合成的有机高分子材料 | |
| D. | 碳膜片在氧气中完全燃烧的产物和碳在氧气中完全燃烧的产物不同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com