
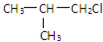 ��G�Ĺ������������Ȼ�
��G�Ĺ������������Ȼ�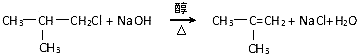 ��E������Cu��OH��2��Ӧ��
��E������Cu��OH��2��Ӧ��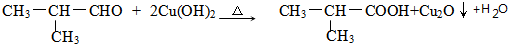 ��
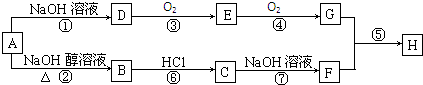
�� ���� A�ķ���ʽΪC4H9Cl�����������ƴ���Һ�����������·�����ȥ��Ӧ����B��B��HCl�����ӳɷ�Ӧ����C��C����±������ˮ�ⷴӦ����F����FΪ�������ΪC4H9OH��F���ܷ�����������Ӧ����FΪ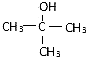 ����CΪ
����CΪ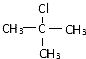 ��BΪ
��BΪ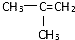 ����A����ˮ�ⷴӦ����D��D����������Ӧ����E��E����������Ӧ����G��ת��������̼�Ǽܲ��䣬��AΪ
����A����ˮ�ⷴӦ����D��D����������Ӧ����E��E����������Ӧ����G��ת��������̼�Ǽܲ��䣬��AΪ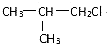 ����DΪ
����DΪ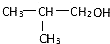 ��EΪ
��EΪ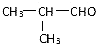 ��GΪ
��GΪ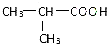 ��G��F����ת����Ӧ����HΪ
��G��F����ת����Ӧ����HΪ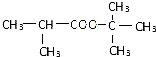 ���ݴ˽��
���ݴ˽��
��� �⣺A�ķ���ʽΪC4H9Cl�����������ƴ���Һ�����������·�����ȥ��Ӧ����B��B��HCl�����ӳɷ�Ӧ����C��C����±������ˮ�ⷴӦ����F����FΪ�������ΪC4H9OH��F���ܷ�����������Ӧ����FΪ ����CΪ
����CΪ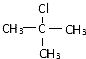 ��BΪ
��BΪ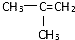 ����A����ˮ�ⷴӦ����D��D����������Ӧ����E��E����������Ӧ����G��ת��������̼�Ǽܲ��䣬��AΪ
����A����ˮ�ⷴӦ����D��D����������Ӧ����E��E����������Ӧ����G��ת��������̼�Ǽܲ��䣬��AΪ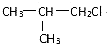 ����DΪ
����DΪ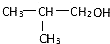 ��EΪ
��EΪ ��GΪ
��GΪ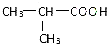 ��G��F����ת����Ӧ����HΪ
��G��F����ת����Ӧ����HΪ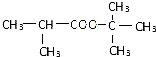 ��
��
��1��ͨ�����Ϸ���֪��A�ṹ��ʽΪ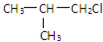 ��GΪ
��GΪ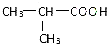 ����������������Ȼ���
����������������Ȼ���
�ʴ�Ϊ��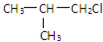 ���Ȼ���
���Ȼ���
��2����Ӧ�٢�����ȡ����Ӧ����Ӧ�ۢ�����������Ӧ����Ӧ��������ȥ��Ӧ����Ӧ�����ڼӳɷ�Ӧ����Ӧ������ȡ����Ӧ���뷴Ӧ�٢�������ͬ���Ǣݣ���A�л���C��������ȥ��Ӧ������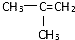 ��������ɵ�B�Ĵ�����Ӱ�죬
��������ɵ�B�Ĵ�����Ӱ�죬
�ʴ�Ϊ���ݣ��ޣ�
��3��A��B�Ļ�ѧ��Ӧ����ʽΪ�� ��E������Cu��OH��2��Ӧ��ѧ����ʽΪ
��E������Cu��OH��2��Ӧ��ѧ����ʽΪ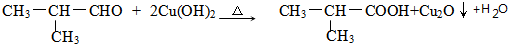 ��
��
�ʴ�Ϊ�� ��
��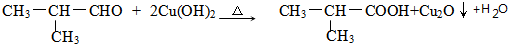 ��
��
���� ���⿼���л����ƶϣ�Ϊ��Ƶ���㣬���ؿ���ѧ�������ƶ�������֪ʶ�ۺ�Ӧ����������ȷ�����ż������ʹ�ϵ�ǽⱾ��ؼ���ע�⣺���������еĴ����ܱ���������Ϊ�״��㣮


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Һ̬���ж����ӷ���Ӧ������ĥ�ڵ�ϸ��ƿ�У���ˮ�⣬�Ӹ��������������������� | |
| B�� | ���ͻ�ú�ʹ���ڴ���������ɫ����ƿ�� | |
| C�� | ̼������Һ������������Һ���������ĥ��������ɫ����ƿ�� | |
| D�� | ��ˮ����������Һ���������ĥ��������ɫ����ƿ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | C2H2 | B�� | KOH | C�� | NaF | D�� | C60 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
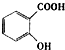 ���ɵ��»��߳���ͷʹ�����ĵ�֢״���農��ע��С�մ�NaHCO3����Һ������С�մ���ˮ��������е��Ȼ���Ӧ����ˮ�����ƣ�ʹ֢״���⣮д��ˮ������С�մ�Ӧ�Ļ�ѧ����ʽ��
���ɵ��»��߳���ͷʹ�����ĵ�֢״���農��ע��С�մ�NaHCO3����Һ������С�մ���ˮ��������е��Ȼ���Ӧ����ˮ�����ƣ�ʹ֢״���⣮д��ˮ������С�մ�Ӧ�Ļ�ѧ����ʽ��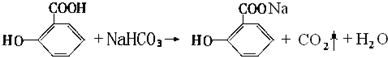 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ȼ����백ˮ��Ӧ��Al3++3OH-�TAl��OH��3�� | |
| B�� | ����ϡ���ᷴӦ��2Fe+6H+�T2Fe3++3H2�� | |
| C�� | ������ˮ��Ӧ��Cl2+H2O?2H++Cl-+ClO- | |
| D�� | ���մ���Һ�м��������Ĵ��CO32-+2CH3COOH�TCO2��+H2O+2CH3COO- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na2O | B�� | Na2O2 | C�� | Na2O��Na2O2 | D�� | ����ȷ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
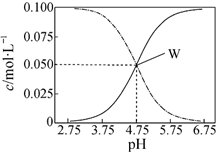
| A�� | pH=5.5��Һ�У�c��CH3COOH����c��CH3COO-����c��H+����c��OH-�� | |
| B�� | W���ʾ��Һ�У�c��Na+��=c��CH3COO-��+c��CH3COOH�� | |
| C�� | ��W������ʾ��1.0L��Һ��ͨ��0.05molHCl���壨��Һ����仯�ɺ��ԣ���c��H+��=c��CH3COOH��+c��OH-�� | |
| D�� | pH=3.5��Һ�У�c��Na+��+c��H+��-c��OH-��+c��CH3COOH��=0.1mol•L-1 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com