

���� ��1��ʵ����������������Ӧ��ȡ�Ȼ�������������Ҫ��ȡ������һ�㳣��Ũ����Ͷ������̷�Ӧ��ȡ������
��2��D��������Fe��Ӧ�����Ȼ��������Ȼ����׳��⣬�Ʊ��������к���ˮ��������Ҫ���и��
��3�����������£�����������Ӧ�����Ȼ�����
��� �⣺��1��ʵ����������������Ӧ��ȡ�Ȼ������������ȱ�����ȡ������ʵ���ҳ���Ũ����Ͷ������̼�����ȡ���������������£�Ũ����Ͷ������̷�Ӧ�����Ȼ��̡�������ˮ������B�з����Ļ�ѧ��Ӧ��4HCl��Ũ��+MnO2 $\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+Cl2��+2H2O��
�ʴ�Ϊ��4HCl��Ũ��+MnO2 $\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+Cl2��+2H2O��
��2��D��������Fe��Ӧ�����Ȼ��������Ȼ����׳��⣬�Ʊ��������к���ˮ��������Ҫ���и����C��Ũ����������ǣ�����������
�ʴ�Ϊ������������
��3�����������£�����������Ӧ�����Ȼ�������Ӧ����ʽΪ��2Fe+3Cl2 $\frac{\underline{\;\;��\;\;}}{\;}$ 2FeCl3��
�ʴ�Ϊ��2Fe+3Cl2 $\frac{\underline{\;\;��\;\;}}{\;}$2FeCl3��
���� ���⿼���������Ʊ�ʵ�鷽���е��й�֪ʶ����Ŀ�Ѷ��еȣ�ע�����ʱ���������Ƿ����������������Ӧ�������Ȼ��������Ȼ�������Ϊ�״��㣮


 Сѧ���AB��ϵ�д�
Сѧ���AB��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1�� | B�� | 2�� | C�� | 3�� | D�� | 4�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� | CH3OH | CH3OCH3 | H2O |
| Ũ��/��mol•L-1�� | 0.44 | 0.6 | 0.6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
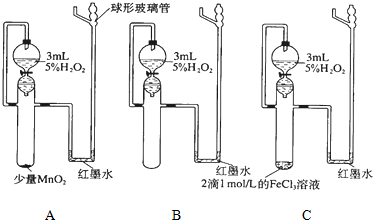
| ʵ��Ŀ�� | �����Թ�������ֽ⻯ѧ��Ӧ����Ӱ�� | ||
| ʵ�鲽�� | ��������ͬ�Ĵ�������©���зֱ����2��3mLԼ5%��H2O2��Ȼ����һ֧�Թ��еμ�2��1mol/L��FeCl3��Һ����һ֧�Թ��м�������MnO2���壮ͬʱ����֧�Թ��з���©���е�ȫ����Һ���۲��īˮ��������� | ||
| ��Ӧ���� | A����MnO2 | B���� | C 2��FeCl3��Һ |
| ʵ������ | |||
| ��Ӧ�� �ʴ�С | ����v ��A����v ��B����v ��C����ʾ�� | ||
| ���� | |||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
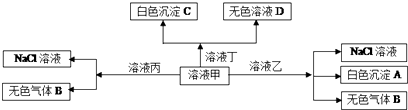
| A�� | ��ΪAlCl3����ΪNaHCO3 | |
| B�� | �ڼ��еμӶ���ʼ��Ӧ�����ӷ���ʽ��2HCO3-+Ba2++2OH-B�TaCO3��+2H2O+CO32- | |
| C�� | ��ɫ����A�����ܽ�����Һ���� | |
| D�� | �ڱ��п��Դ���������У�Fe2+��SO42-��NO3- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ij��ȤС����С����ý������ᷴӦ����ʵ�飬��5.4g����ƬͶ��500mL 0.5mol•L-1��������Һ�У�ͼΪ��Ӧ�������������뷴Ӧʱ��Ĺ�ϵͼ��
ij��ȤС����С����ý������ᷴӦ����ʵ�飬��5.4g����ƬͶ��500mL 0.5mol•L-1��������Һ�У�ͼΪ��Ӧ�������������뷴Ӧʱ��Ĺ�ϵͼ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
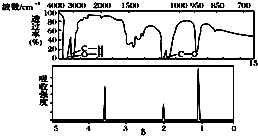
| A�� | �ɺ˴Ź�������֪�����л��������������ֲ�ͬ�Ļ�ѧ�� | |
| B�� | �ɺ������֪�����л�������������ֲ�ͬ����ԭ�� | |
| C�� | ��A�Ļ�ѧʽΪC2H6O������ṹ��ʽΪCH3-O-CH3 | |
| D�� | ������˴Ź�����������֪������е���ԭ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
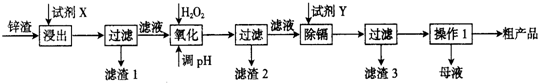
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ���� | NaCl | KCl | AlCl3 | SiCl4 | ����B |
| �۵�/�� | 810 | 776 | 190 | -68 | 2300 |
| �е�/�� | 1465 | 1418 | 180 | 57 | 2500 |
| A�� | SiCl4�Ƿ��Ӿ��� | B�� | ����B������ԭ�Ӿ��� | ||
| C�� | AlCl3���������� | D�� | NaCl�л�ѧ����ǿ�ȱ�KCl�е�С |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com