
[���ʽṹ������]��ϩͪ (CH2=C=O)��һ����Ҫ���л��м��壬����C2H2��O2�Ļ������ͨ��п���ơ��������ֽ�����������(����)��Ӧ�õ���Ҳ����CH3COOH�ں���(C2H5O)3P=O�����¼�����H2O�õ���
��1��Zn2+��̬��������Ų�ʽΪ ��
��2����H2O��Ϊ�ȵ������һ��������Ϊ ����ϩͪ������̼ԭ���ӻ���������� ��
��3��CH3COOH�ķе��HCOOCH3�ĸߣ�����Ҫԭ���� ��
��4��lmol(C2H5O)3P=O�����к��е�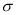 ������ĿΪ ��
������ĿΪ ��
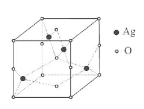
��5��Ag��������ľ����ṹ��ͼ��ʾ��
��������Ļ�ѧʽΪ .
��1��[Ar]3d10��1s22s22p63s23p63d10��
��2��sp2��sp��
��3��������Ӽ���������
��4��25NA��
��5��AgO��
��������
�����������1��ZnΪ30��Ԫ�أ����ݹ�������֪��Zn2+��̬��������Ų�ʽΪ[Ar]3d10��1s22s22p63s23p63d10�� ��2����H2O��Ϊ�ȵ������һ��������ΪNH2����������ϩͪ���ӵĽṹ��ʽ֪����ϩͪ��CH2�е�CΪsp2�ӻ����ʻ��е�CΪsp�ӻ���̼ԭ���ӻ����������sp2��sp����3��CH3COOH�ķе��HCOOCH3�ĸߣ�����Ҫԭ����������Ӽ��������� ��4�� (C2H5O)3P=O ��̼�����̼̼������̼������������������Ϊ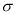 ��������˫������1��
��������˫������1��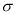 ����lmol(C2H5O)3P=O�����к��е�
����lmol(C2H5O)3P=O�����к��е�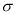 ������ĿΪ25NA����5������Ag��������ľ����ṹ�����и������Agλ�ھ����ڲ���1�������к�Ag�ĸ���Ϊ4��λ�ڶ����ϵ�OΪ8����λ�����ϵ�OΪ4����λ�����ϵ�OΪ2����λ���ڲ���OΪ1����1�������к�O����Ϊ��8��1/8+4��1/4+2��1/2+1=4����������Ļ�ѧʽΪAgO��
������ĿΪ25NA����5������Ag��������ľ����ṹ�����и������Agλ�ھ����ڲ���1�������к�Ag�ĸ���Ϊ4��λ�ڶ����ϵ�OΪ8����λ�����ϵ�OΪ4����λ�����ϵ�OΪ2����λ���ڲ���OΪ1����1�������к�O����Ϊ��8��1/8+4��1/4+2��1/2+1=4����������Ļ�ѧʽΪAgO��
���㣺�������ʽṹ�����ʣ��漰ԭ�ӽṹ����ѧ�����͡����ӽṹ�;������㡣



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015�ӱ�ʡ��һ��ѧ�ڵڶ����¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��ͼ���������߷ֱ��ʾ1 g C3H6��1 g M��������ͬ�����������ѹǿ���¶ȵĹ�ϵ���Ծ�ͼ���ж�M���������

A��SO2 B��CO C��C3H8 D��Cl2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����������и�����ѧ����ĩ���ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
Һ��ȼ�ϵ�����������ȼ�ϵ�ؾ������С,��������洢װ�õ��ŵ�.һ������(N2H4)Ϊȼ�ϵĵ��װ����ͼ��ʾ.�õ���ÿ����е�������Ϊ������,KOH��Ϊ�����.���й��ڸ�ȼ�ϵ�ص���������ȷ����
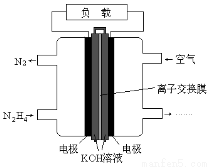
A���������Ҳ�缫�������غ��������缫
B�����������ĵ缫��ӦʽΪN2H4+4OH--4e-=N2+4H2O
C����ȼ�ϵ�صĵ缫����Ӧ���ö�������,����ߵ缫��Ӧ�����ڵ缫 �����������,��ʹ������������Һ��ֽӴ�
D����ȼ�ϵ�س����ŵ�ʱ,K+�Ӹ���������Ǩ��,������ӽ���Ĥ��ѡ�������ӽ���Ĥ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�꽭��ʡ����������⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
�����й�˵����ȷ����
A�������ĸ�ʴ�����У����ⸯʴ��������ʴ������ͬʱ����
B����ӦNH4Cl(s)��NH3(g)+HCl(g)�������²����Է����У���÷�Ӧ�Ħ�H��0
C������Ksp(BaSO4)��Ksp(BaCO3)�����BaSO4����������ת��ΪBaCO3 ����
D��25��ʱ��0.1 mol��L��1CH3COOH��Һ��ˮϡ�ͺ�c(OH��)/c(CH3COOH)����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�꽭��ʡ����������⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
�����й��������ʵ�Ӧ�ô������
A���������費��ǿ�ᷴӦ������ʯӢ��������ʢ�������
B��̼�����ƾ��������ԣ�������ʳƷ����
C���������ƾ���ǿ�����ԣ���������������Һ
D��������ˮ������Al(OH)3���壬��������ˮ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�꽭��ʡ�Ͼ��С��γ��и���һģ��ѧ�Ծ��������棩 ���ͣ������
(12��)����п����Ҫ�Ļ�������ԭ�ϣ��Ӻ�п��ˮ(��Zn2+��������Mn2+��Fe2+��Pb2+��)Ϊԭ����ȡZnO��ʵ���������£�
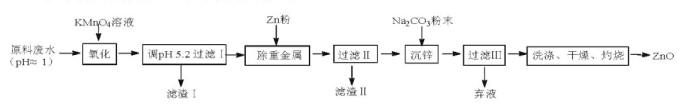
��֪���������������������PH��Χ
�������� | Fe(OH)3 | Fe(OH)2 | Zn(OH)2 | Pb(OH)2 |
pH | 2.2��3.2 | 5.8��7.9 | 5.5��13.5 | 7.0��13.0 |
��1��KMnO4������ˮ��Mn2+����MnO2�����ӷ���ʽΪ ������I����Ҫ�ɷֳ�MnO2�⣬��һ��
�� (д��ѧʽ)��
��2������II����Ҫ�ɷֳ�������Zn�ۡ�MnO2�⣬���� (д��ѧʽ)������II�к��ж������̣������ԭ���� ��
��3���������ɵļ�ʽ̼��п[ZnCO3��2Zn(OH)2]�Ļ�ѧ����ʽΪ ������ʱ���õ��Ĺ��������������ƾ�����õ���2���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�꽭��ʡ�Ͼ��С��γ��и���һģ��ѧ�Ծ��������棩 ���ͣ�ѡ����
�ڵ�ұ���ĵ����д��ڵ����W2[X2Y2Z4]����֪����Ԫ�صļ����ӵĵ��Ӳ�ṹ����ͬ��Yԭ������������Ϊ������3����Xԭ������������ΪYԭ��������������һ�룬����˵����ȷ����
A��ԭ��������W>X>Y>Z
B��ԭ�Ӱ뾶��r(w)>r(X)>r(Y)>r(Z)
C��W������������ˮ������Ա�X����
D��Y�ļ��⻯����ȶ��Ա�Z��ǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�꽭��ʡ���Ƹ۵����и���һģ��ѧ�Ծ��������棩 ���ͣ�ѡ����
25��ʱ������ˮ���Ȼ����Һ��ϵõ� c(NH3��H2O)��c(NH4��) = 0.1 mol��L��1�Ļ����Һ����Һ��c(NH3��H2O)��c(NH4��)��pH�Ĺ�ϵ��ͼ��ʾ�������й�����Ũ�ȹ�ϵ����һ����ȷ����
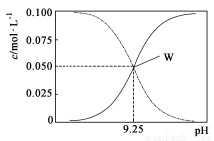
A��W���ʾ��Һ�У�c(NH4��) ��c(H��) �� c(Cl��)��c(OH��)
B��pH��10.5��Һ�У�c(Cl��)��c(OH��)��c(NH3��H2O)��0.1 mol��L��1
C��pH��9.5��Һ�У�c(NH3��H2O)��c(NH4��)��c(OH��)��c(H��)
D����W������ʾ1L��Һ�м���0.05molNaOH���壨������Һ����仯����c(Cl��)��c(Na��)��c(OH��) ��c(NH4��) ��c(H��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��㶫ʡ�����и�����һѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����£����б�����ȷ����
A��pH=3��CH3COOH��Һ��Ũ��С��pH=2�������Ũ��
B����NaHCO3��Һ�м�������NaOH���壬������HCO3-��ˮ�⣬ʹc��HCO3-������
C������������CH3COOH��Һ��NaOH��Һ��ϣ�������Һ�����ڣ�c(Na+)+c(H+)=c(CH3COO-)+c(OH-)
D��Na2CO3��Һ�У�c(Na+)>c(CO32-)>c(OH-)=c(HCO3-)>c(H+)
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com