
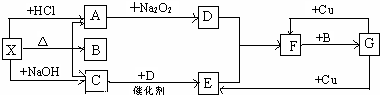
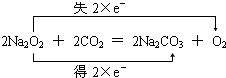 ,
,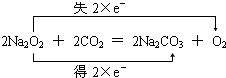 ;
;
| ||
| ||
| 1mol×[5-(-3)] |
| 4 |


科目:高中化学 来源:不详 题型:问答题
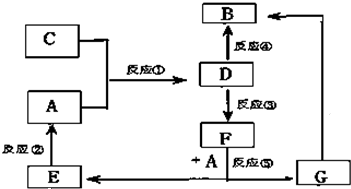
| 实验步骤 | 实验现象 | 用化学用语解释 |
| 将少量气体通入淀粉KI溶液 | 溶液最初变成______色 | ______ (用离子方程式表示) |
| 继续通入气体 | 溶液逐渐变成无色 | ______ (用化学方程式表示) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
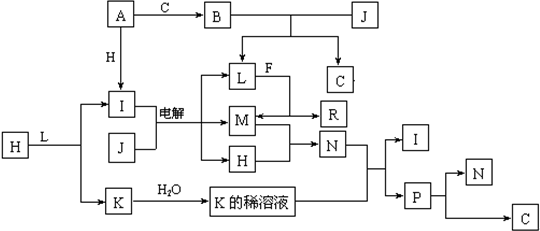
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题

查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
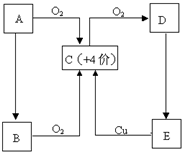
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 点燃 |
| 溶于水 |
| 惰性电极电解 |
| A.①② | B.②④ | C.①③ | D.③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| O2 |
| O2 |
| H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
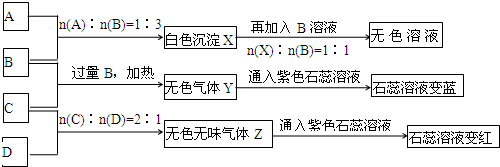
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com