
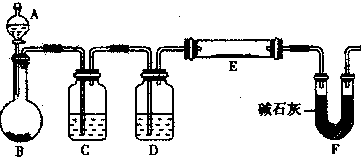
下图为某学生利用氯酸钾分解制氧气的反应装置,以此来测定氧气的摩尔质量.实验步骤如下:

①把适量的氯酸钾粉末和少量二氧化锰粉末混合均匀,放入干燥的试管中,准确称量,质量为α g.
②装好实验装置.
③检查装置气密性.
④加热,开始反应,直到产生一定量的气体.
⑤停止加热(如图,导管出口高于液面).
⑥测量收集到的气体体积.
⑦准确称量试管和残留物的质量为bg.
⑧测量实验室的温度.
⑨把残留物倒人指定的容器中,洗净仪器,放回原处,把实验桌面收拾干净.
⑩处理实验数据,求出氧气的摩尔质量.
回答下列问题:
(1)如何检查装置的气密性?
_________________________________________________________________________________________________________________________________________________________.
(2)以下是测量收集到气体体积必须包括的几个步骤:①调整量筒内外液面高度使之相同②使试管和量筒内的气体都冷却至室温 ③读取量筒内气体的体积.这三步操作的正确顺序是_________(请填写步骤代号).
(3)测量收集到的气体体积时,如何使量筒内外液面的高度相同?
_______________________________________________________________________________
(4)如果实验中得到的氧气体积是cL(25℃、1.01×105Pa),水蒸气的影响忽略不计,氧气的摩尔质量的计算式为(含口a、b、c,不必化简):
M(O2)=__________________________________.
(1)将导管的出口浸入水槽的水中,手握住试管,有气泡从导管口逸出,放开手后,有少量水进入导管,表明装置不漏气 (2)②①③ (3)慢慢将量筒下移
(4)
|
第(1)小题是考生熟悉的常用的“查漏”的方法,用手握住试管,体温使导管在浸入水槽中的出口处冒出气泡,放开手后,有少量水吸入导管,表明不漏气. 第(2)小题,因为排出的气体是需要用排出的水的体积衡量的,而反应前后的量筒温度是不同的,因此,反应终止应该先停止加热,待体系恢复到室温时,才取出导管.这一步操作跟通常的实验不同,所以停止加热时导管的出口要高于量筒内的液面,此时即使不取出导管而停止加热,也不会造成水的倒吸. 停止加热、回到室温后,将量筒下移以调节量筒内的液面与水槽一致,此时量筒内气体压强也为大气压,读数才是正确的.所以本小题的正确顺序是②①③. 第(3)小题是指出量筒应慢慢下移. 第(4)小题是利用恒压下的气体公式求得气体的摩尔数和分子量.
|


科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:058

①把适量的氯酸钾粉末和少量二氧化锰粉末混合均匀,放入干燥的试管中,准确称量,质量为α g.
②装好实验装置.
③检查装置气密性.
④加热,开始反应,直到产生一定量的气体.
⑤停止加热(如图,导管出口高于液面).
⑥测量收集到的气体体积.
⑦准确称量试管和残留物的质量为bg.
⑧测量实验室的温度.
⑨把残留物倒人指定的容器中,洗净仪器,放回原处,把实验桌面收拾干净.
⑩处理实验数据,求出氧气的摩尔质量.
回答下列问题:
(1)如何检查装置的气密性?
_________________________________________________________________________________________________________________________________________________________.
(2)以下是测量收集到气体体积必须包括的几个步骤:①调整量筒内外液面高度使之相同②使试管和量筒内的气体都冷却至室温 ③读取量筒内气体的体积.这三步操作的正确顺序是_________(请填写步骤代号).
(3)测量收集到的气体体积时,如何使量筒内外液面的高度相同?
_______________________________________________________________________________
(4)如果实验中得到的氧气体积是cL(25℃、1.01×105Pa),水蒸气的影响忽略不计,氧气的摩尔质量的计算式为(含口a、b、c,不必化简):
M(O2)=__________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
①把适量的氯酸钾粉末和少量二氧化锰粉末混合均匀,放入干燥的试管中,准确称量,质量为ag;
②装好实验装置;
③检查装置气密性;
④加热,开始反应,直到产生一定量的气体;
⑤停止加热(如下图,导管口高于液面);

⑥测量收集到气体的体积;
⑦准确称量试管和残留物的质量为bg;
⑧测量实验室的温度;
⑨把残留物倒入指定的容器中,洗净仪器,放回原处,把实验桌面收拾干净;
⑩处理实验数据,求出氧气的相对分子质量。
回答下列问题:
(1)如何检查装置的气密性:__________。
(2)以下是测量收集到气体体积必须包括的几个步骤:①调整量筒内外液面高度使之相同;②使试管和量筒内的气体都冷却至室温;③读取量筒内气体的体积。这三步操作的正确顺序是:__________(请填写步骤代号)。
(3)测量收集到气体体积时,如何使量筒内外液面的高度相同?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com