
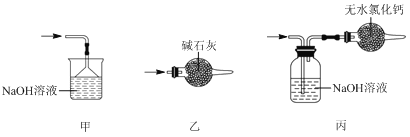
����Ŀ��ʵ���ҿ��������������Ʊ���ˮ���Ȼ�����SnCl4����SnCl4�ӷ���������ˮ�⣬Cl2��������SnCl4���Ʊ�ԭ����ʵ��װ��ͼ���£�
Sn(s)+2Cl2(g)=SnCl4(l) ��H = �C511kJmol��1

�����õ����й��������£�
���� | Sn | SnCl4 | CuCl2 |
�۵�/�� | 232 | -33 | 620 |
�е�/�� | 2260 | 114 | 993 |
�Ʊ������У����������ģ�������������ʱ��Ӧ���в�����������SnCl4Һ��������ڸ߶�ʱ��Һ̬���ᆳ����������ƿ���ش��������⣺
��1��a�ܵ�������________��
��2��A�з�Ӧ�����ӷ���ʽ��________��
��3��D��������________��
��4��E����ȴˮ��������________��
��5��β������ʱ����ѡ�õ�װ����________������ţ���
��6�������к�ͭ������E�в���CuCl2������Ӱ��F�в�Ʒ�Ĵ��ȣ�ԭ����________��
��7��SnCl4��Ʒ�к���Cl2������ʱ����������м������ɵô�����SnCl4����������в���Ҫ�õ���������________������ţ���
A��������ƿ B���¶ȼ� C�������� D�������� E������ƿ
���𰸡�ƽ��ѹǿ��ʹŨ�����ܹ�˳������ 2MnO4��+10Cl��+16H+=2Mn2++5Cl2��+8H2O ʹ������ָ��� �������Ȼ�����������ʧ�����²����½� �� CuCl2�۵�ϸߣ����������Ȼ���Һ����� E
��������
��1��a�ܽ���Һ©��Һ��������ͨ����ƽ��ѹǿ��ʹŨ�����ܹ�˳�����µ����ã�
��2��A�еķ�ӦΪ������غ�Ũ��������������Ӧ�����Ȼ��̡��Ȼ��ء�������ˮ�������غ��ϵ��ƽ��д�����ӷ���ʽ��
��3��DΪʢ��Ũ�����ϴ��ƿ������������������������Ϣ��֪��SnCl4������ˮ�⣬��D��������ʹ������ָ��
��4������Ϣ��֪��SnCl4�ӷ�����E����ȴˮ�������DZ������Ȼ�����������ʧ�����²����½���
��5��β������ʱ��ѡ�õ�װ���в���ʹ��ˮ��Һ����Ϊˮ��������E��ʹSnCl4����ˮ�⣻
��6���ɱ������ݿ�֪��CuCl2�۵�ϸߣ����������Ȼ���Һ����������������к�ͭ������E�в���CuCl2������Ӱ��F�в�Ʒ�Ĵ��ȣ�
��7�������������Ҫ�õ���������������ƿ���¶ȼơ������ܺͽ��������Դ˷�����
��1��a�ܽ���Һ©��Һ��������ͨ����ƽ��ѹǿ��ʹŨ�����ܹ�˳�����µ����ã�
�ʴ�Ϊ��ƽ��ѹǿ��ʹŨ�����ܹ�˳�����£�
��2��A�еķ�ӦΪ������غ�Ũ��������������Ӧ�����Ȼ��̡��Ȼ��ء�������ˮ�����ӷ���ʽΪ2MnO4��+10Cl��+16H+=2Mn2++5Cl2��+8H2O��
�ʴ�Ϊ��2MnO4��+10Cl��+16H+=2Mn2++5Cl2��+8H2O��
��3��DΪʢ��Ũ�����ϴ��ƿ������������������������Ϣ��֪��SnCl4������ˮ�⣬��D��������ʹ������ָ��
�ʴ�Ϊ��ʹ������ָ��
��4������Ϣ��֪��SnCl4�ӷ�����E����ȴˮ�������DZ������Ȼ�����������ʧ�����²����½���
�ʴ�Ϊ���������Ȼ�����������ʧ�����²����½���
��5��β������ʱ��ѡ�õ�װ���в���ʹ��ˮ��Һ����Ϊˮ��������E��ʹSnCl4����ˮ�⣬�ʲ�ѡ�ס�����Ӧѡ�ң�
�ʴ�Ϊ���ң�
��6���ɱ������ݿ�֪��CuCl2�۵�ϸߣ����������Ȼ���Һ����������������к�ͭ������E�в���CuCl2������Ӱ��F�в�Ʒ�Ĵ��ȣ�
�ʴ�Ϊ��CuCl2�۵�ϸߣ����������Ȼ���Һ�������
��7�������������Ҫ�õ���������������ƿ���¶ȼơ������ܺͽ���������������ƿ���ʲ�ѡE��
�ʴ�Ϊ��E��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
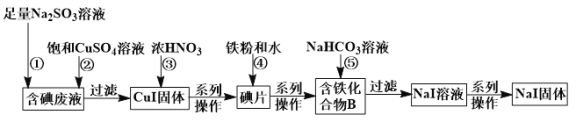
����Ŀ��ij��ѧ��ȤС������NaI��Һ��ͨ������Cl2�õ������Һ�������ú����Һ��ȡNaI���壬ʵ���������£�
��֪��Ӧ����2I��+2Cu2++![]() +H2O
+H2O![]() 2CuI��+
2CuI��+![]() +2H+��
+2H+��
�ش��������⣺
��1������ʵ������Ҫ�IJ�����������ͨ©�����ձ���_____________��
��2����Ӧ����CuI����������ԭ����ֻ��NO2���÷�Ӧ�Ļ�ѧ����ʽΪ_________________������95.5 g CuI���뷴Ӧ������Ҫ�����______________L��O2���ܽ����ɵ�NO2��ˮ����ȫת��Ϊ���ᡣ
��3��������B�к�����Ԫ�أ���ԭ������һ��Ԫ��ԭ�ӵ����ʵ���֮��Ϊ3��8������B�Ļ�ѧʽΪ_____________��
��4����Ӧ�������ɺ�ɫ�������ɫ���壬��ɫ������׳�Ϊ��������������Ӧ���Ļ�ѧ����ʽΪ______��
��5����������Cl2ͨ�뺬12 g NaI����Һ�У�һ��ʱ������Һ���ɵõ����������Ϊ_________g��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������Ⱦ��������Ҫ����֮һ������������Ĺ�ҵβ���������·������������Ƶ��й㷺��;��ʯ�ࡣ
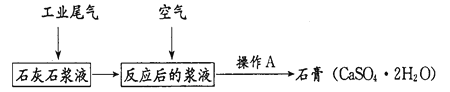
(1)SO2��ɵ�һ�ֳ���������ȾΪ___���оٶ��������һ����;___��
(2)SO2ʹ��ɫKMnO4��Һ��ɫ�����ӷ���ʽΪ___��(��ʾ��KMnO4 ����ԭΪMn2+)
(3)ͨ����ʱ��Ӧ�Ļ�ѧ����ʽΪ___������ʵ���ҽ��У�����A��_____��
(4)��������麟�������ֽ��ҵ������ij����ˮ��Һ�����ù�ҵβ���õ���������泥��������Ϊ_______��
(5)���������ȼú�м�����������ʯ�ң��ɼ��������ж���������ŷţ�����Ϊ�Ƿ����?_______(����������������������)��������______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ܽ�����п�̻���ȡ�ߴ�п�Ĺ���������ͼ��ʾ���ܽ�������п�̻���п��ͭ���ӡ���Ԫ�طֱ���Zn(NH3)42+��Cu(NH3)42+��Cd(NH3)42+��AsCl52������ʽ���ڡ�

�ش��������⣺
��1��Zn(NH3)42+��Zn�Ļ��ϼ�Ϊ________�����ܽ�����ZnO������Ӧ�����ӷ���ʽΪ________��
��2��п���������¶ȵĹ�ϵ��ͼ��ʾ������30 ��ʱп��������ߵ�ԭ��Ϊ________��

��3�����������ӡ��У�AsCl52��ת��ΪAs2O5���������۳���ȥ����Һʼ�սӽ����ԡ��÷�Ӧ�����ӷ���ʽΪ________��
��4��������3������Ҫ�ɷ�Ϊ________��
��5������⡱ʱZn(NH3)42+�������ŵ�ĵ缫��ӦʽΪ_______���������ų�һ����ɫ��ζ�����壬����ͨ�����KSCN��FeCl2��Һ�У�����������������________��д��ѧʽ��������ĵ��Һ������________��дһ�����ʵĻ�ѧʽ����ɷ��ء��ܽ����������ʹ�á�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��FeSe ��MgB2�ȳ������Ͼ��й�����Ӧ��ǰ����
��1����̬Feԭ�Ӽ۲���ӵĵ����Ų�ͼ���������ʽ��Ϊ________����̬Seԭ�ӵĵ���ռ������ܼ��ĵ���������ͼΪ________�Ρ�
��2����FeSe��Ƕ����ण�![]() ���ܵõ������������ܵij������ϡ�����е�ԭ�ӵ��ӻ�����Ϊ________���÷����ڴ���________�����ţ���
���ܵõ������������ܵij������ϡ�����е�ԭ�ӵ��ӻ�����Ϊ________���÷����ڴ���________�����ţ���
A���Ҽ� B���м� C����λ�� D�����
��3���������ֱ������Һ�����õ����кܸ߷�Ӧ���ԵĽ���������Һ����ͨ��ϵ�з�Ӧ���Ƶ�FeSe����������Li0.6(NH2)0.2(NH3)0.8Fe2Se2��
��NH2���Ŀռ乹��Ϊ________��
��Һ���ǰ���Һ���IJ���,������Һ����ԭ����________��
�۽��������Һ��ʱ������Ӧ��Li + (m+n)NH3=X+e��(NH3)n��X�Ļ�ѧʽΪ________��
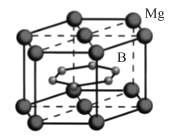
��4��MgB2����ṹ��ͼ��ʾ��Bԭ�Ӷ���Ϊһ�㣬����������ʯī�Ľṹ��ÿ��Bԭ����Χ����________����֮�Ⱦ����������Bԭ�ӣ��������ױ߱߳�Ϊa cm����Ϊc cm�������ӵ�������ֵΪNA ���þ�����ܶ�Ϊ________ g��cm��3���г�����ʽ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NA�ǰ���٤��������ֵ���������˵����ȷ���ǣ� ��
A.2.24LN2��O2�Ļ�������з�����Ϊ0.1NA
B.2.4gþ�ڿ�������ȫȼ������MgO��Mg3N2��ת�Ƶĵ�����Ϊ0.2NA
C.��״���£�22.4LCCl4�к��з��ӵ���ĿΪNA
D.0.1molFeCl3��ȫˮ�����ɵ�Fe(OH)3����������Ϊ0.1NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ѡ���У�����ָ����Ŀ����Ŀǰ����ȵ��� �� ��
A.��������17gOH����1mol��OH
B.˫����Ŀ��1mol![]() ��4mol C2H4
��4mol C2H4
C.�����������³�ѹ��16g������4g����
D.������������72gCaO2��62g Na2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��![]() ��
��![]() ��
��![]() ��
��![]() ��ԭ��������������
��ԭ��������������![]() ��
��![]() ��
��![]() ��
��![]() �ֱ�λ��ͬһ���壬
�ֱ�λ��ͬһ���壬![]() ��
��![]() ���γɹ��ۻ�����
���γɹ��ۻ�����![]() ��
��![]() ԭ�ӵ��ڲ������������������������2.5����������������ȷ���ǣ� ��
ԭ�ӵ��ڲ������������������������2.5����������������ȷ���ǣ� ��
A.![]() �����е�����ԭ������㶼Ϊ8���ӽṹ
�����е�����ԭ������㶼Ϊ8���ӽṹ
B.![]() ��
��![]() �Ļ�ѧ��������ͬ
�Ļ�ѧ��������ͬ
C.![]() �ǹ��ۻ�����
�ǹ��ۻ�����
D.ԭ�Ӱ뾶��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������˵����Ϊ1 ~ 18��Ԫ��ԭ�ӵĺ�����Ӳ������������������ش��������⣺
(1)�˵����Ϊ6��14��Ԫ��ԭ�ӣ����ǵ�____________��ͬ��____________����ͬ���˵����Ϊ15��16��Ԫ��ԭ�ӣ����ǵ�____________��ͬ��____________����ͬ���˵����Ϊ10��18��Ԫ��ԭ�ӣ����ǵ�������������Ϊ____________�����ǵ�Ԫ�ط��ŷֱ���____________��____________��
(2)ijԪ�ص�ԭ�Ӻ������������Ӳ㣬�����������Ǻ������������![]() ����Ԫ�ص�Ԫ�ط�����____________��ԭ�ӽṹʾ��ͼ��____________��
����Ԫ�ص�Ԫ�ط�����____________��ԭ�ӽṹʾ��ͼ��____________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com