
| A£® |  | B£® | C2H2 | C£® |  | D£® | 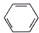 |
·ÖĪö ŗ¬ÓŠ²»±„ŗĶ¼üµÄÓŠ»śĪļŅŌ¼°ŅŅ“¼µČæÉÓėĖįŠŌøßĆĢĖį¼Ų·¢ÉśŃõ»Æ»¹Ō·“Ó¦£¬ŅŌ“Ė½ā“š£®
½ā“š ½ā£ŗA”¢ ĪŖ2-¼×»ł-1-±ūĻ©£¬ŗ¬ÓŠ²»±„ŗĶ¼ü£¬ÄÜÓėĖįŠŌøßĆĢĖį¼Ų·¢ÉśŃõ»Æ»¹Ō·“Ó¦£¬ÄÜŹ¹ĖįŠŌKMnO4ČÜŅŗĶŹÉ«£¬¹ŹA²»Ń”£»
ĪŖ2-¼×»ł-1-±ūĻ©£¬ŗ¬ÓŠ²»±„ŗĶ¼ü£¬ÄÜÓėĖįŠŌøßĆĢĖį¼Ų·¢ÉśŃõ»Æ»¹Ō·“Ó¦£¬ÄÜŹ¹ĖįŠŌKMnO4ČÜŅŗĶŹÉ«£¬¹ŹA²»Ń”£»
B”¢C2H2ĪŖŅŅČ²£¬ŗ¬ÓŠ²»±„ŗĶ¼ü£¬ÄÜÓėĖįŠŌøßĆĢĖį¼Ų·¢ÉśŃõ»Æ»¹Ō·“Ó¦£¬ÄÜŹ¹ĖįŠŌKMnO4ČÜŅŗĶŹÉ«£¬¹ŹB²»Ń”£»
C”¢±½µÄĶ¬ĻµĪļæÉŅŌŹ¹øßĆĢĖį¼ŲČÜŅŗĶŹÉ«£¬¹ŹC²»Ń”£»
D”¢±½ÓėĖįŠŌøßĆĢĖį¼Ų²»·“Ó¦£¬Ōņ²»ÄÜŹ¹ĖįŠŌKMnO4ČÜŅŗĶŹÉ«µÄŹĒ±½£¬¹ŹDŃ”£»¹ŹŃ”D£®
µćĘĄ ±¾Ģā×ŪŗĻæ¼²éÓŠ»śĪļµÄŠŌÖŹ£¬×¢Ņā°ŃĪÕÓŠ»śĪļµÄ½į¹¹ŗĶ¹ŁÄÜĶŵĊŌÖŹ£¬ĪŖ½ā“šøĆĢāµÄ¹Ų¼ü£¬ÄŃ¶Č²»“ó£®


 ³å“Ģ100·Ö1ŗžķĻµĮŠ“š°ø
³å“Ģ100·Ö1ŗžķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CH4ŗĶCH3CH2CH3 | B£® | ${\;}_{17}^{35}$ClŗĶ${\;}_{17}^{37}$Cl | ||
| C£® | 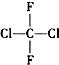 ŗĶ ŗĶ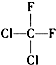 | D£® |  ŗĶCH3-CH2-CH2-CH3 ŗĶCH3-CH2-CH2-CH3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | øĆ·“Ó¦Éę¼°µ½Ąė×Ó¼üŗĶ¹²¼Ū¼üµÄ¶ĻĮŃÓėŠĪ³É | |
| B£® | øĆ·“Ó¦ÖŠ£¬»ÆѧÄÜÖ»×Ŗ±äĪŖČČÄÜ | |
| C£® | ¶ĻæŖ1molH-H¼üŗĶ1molCl-Cl¼üĖłĪüŹÕµÄ×ÜÄÜĮ棬Š”ÓŚŠĪ³É1molH-Cl¼üĖł·Å³öµÄÄÜĮæ | |
| D£® | ·“Ó¦ĪļĖł¾ßÓŠµÄ×ÜÄÜĮæøßÓŚ²śĪļĖł¾ßÓŠµÄ×ÜÄÜĮæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŅŅ“¼”¢“ĪĀČĖįÄĘČÜŅŗµÄĻū¶¾ŌĄķĻąĶ¬ | |
| B£® | Ė«ŃõĖ®ŗĶ“ĪĀČĖįÄĘ¾ßÓŠ½ĻĒæµÄøÆŹ“ŠŌ£¬²»ÄÜÓĆӌʤ·ōµÄĻū¶¾ | |
| C£® | øßĆĢĖį¼ŲČÜŅŗŗĶĖ«ŃõĖ®¾łæÉŅŌ½«²”¶¾Ńõ»Æ¶ų“ļµ½Ļū¶¾µÄÄæµÄ | |
| D£® | ŌŚ“ĪĀČĖįÄĘČÜŅŗÖŠĶØČėÉŁĮ涞Ńõ»ÆĮņæÉ·¢Éś·“Ó¦£ŗ2NaClO+SO2+H2OØTNa2SO3+HClO |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
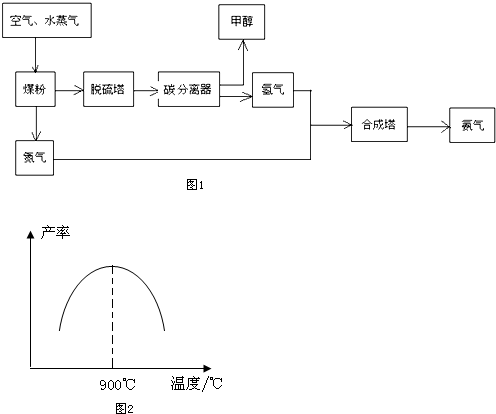
| ĪļÖŹ | H2 | CO | C H3OH |
| ÅضČ/£Ømol•L-1£© | 0.20 | o.10 | o.40 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
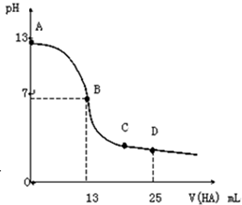 ³£ĪĀĻĀ£¬Ļņ25mL0.1mol•L-1MOHČÜŅŗÖŠÖšµĪ¼ÓČė0.2mol•L-1HAČÜŅŗ£¬ĒśĻßČēĶ¼ĖłŹ¾£ØĢå»ż±ä»ÆŗöĀŌ²»¼Ę£©£®»Ų“šĻĀĮŠĪŹĢā£ŗ
³£ĪĀĻĀ£¬Ļņ25mL0.1mol•L-1MOHČÜŅŗÖŠÖšµĪ¼ÓČė0.2mol•L-1HAČÜŅŗ£¬ĒśĻßČēĶ¼ĖłŹ¾£ØĢå»ż±ä»ÆŗöĀŌ²»¼Ę£©£®»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com