
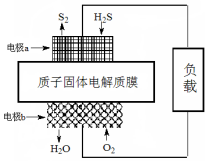
 已知:2H2S(g)+O2(g)═S2(s)+2H2O(l)△H=-632kJ•mol-1.下图为H2S燃料电池的示意图.下列说法正确的是( )
已知:2H2S(g)+O2(g)═S2(s)+2H2O(l)△H=-632kJ•mol-1.下图为H2S燃料电池的示意图.下列说法正确的是( )| A. | 电极a为电池的负极 | |
| B. | 电极b上发生的电极反应为:O2+2H2O+4e-═4OH- | |
| C. | 电路中每通过4 mol电子,电池内部释放632 kJ热能 | |
| D. | 每34 g H2S参与反应,有2 mol H+经质子膜进入正极区 |
分析 根据2H2S(g)+O2(g)═S2(s)+2H2O反应,得出负极H2S失电子发生氧化反应,正极O2得电子发生还原反应,据此分析解答.
解答 解:A、由2H2S(g)+O2(g)═S2(s)+2H2O反应,得出负极H2S失电子发生氧化反应,则a为电池的负极,故A正确;
B、正极O2得电子发生还原反应,所以电极b上发生的电极反应为:O2+4H++4e-=2H2O,故B错误;
C、电路中每流过4mol电子,则消耗1mol氧气,但该装置将化学能转化为电能,所以电池内部几乎不放出能量,故C错误;
D、每34g即$\frac{34g}{34g/mol}$=1molH2S参与反应,则消耗0.5mol氧气,则根据O2+4H++4e-=2H2O,所以有2mol H+经质子膜进入正极区,故D正确;
故选:AD.
点评 本题侧重考查原电池原理,明确电解质溶液酸碱性是解本题关键,难点是电极反应式的书写,题目难度不大.


科目:高中化学 来源: 题型:多选题
| A. | 原混合气体的体积为1.2V | B. | 原混合气体的体积为1.1V | ||
| C. | 反应达平衡时气体B消耗掉0.05V | D. | 反应达到平衡时气体A消耗掉0.05V |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能使红色石蕊试纸变蓝的溶液中:Na+、K+、NO3-、AlO2- | |
| B. | 在含有大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN- | |
| C. | 在加入铝粉能产生氢气的溶液中:NH4+、Fe2+、SO42-、NO3- | |
| D. | 能使湿润的淀粉碘化钾试纸变蓝的溶液中:Na+、NH4+、S2-、Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 降低N2的浓度能加快反应速率 | |
| B. | 降低体系温度能加快反应速率 | |
| C. | 达平衡时各组分含量之比一定等于 1:3:2 | |
| D. | 达到平衡时N2的浓度不再变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用丁达尔效应区分氢氧化铁胶体与氯化铜溶液 | |
| B. | 用澄清石灰水鉴别NaHCO3和Na2CO3 | |
| C. | 用分液法分离植物油和水的混合物 | |
| D. | 用淀粉溶液检验食盐溶液中是否存在I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | KOH是氧化剂 | B. | Cl2发生还原反应 | ||
| C. | KFeO4是氧化产物 | D. | 生成lmol K2Fe04转移6mol的电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇、乙酸都能与金属钠反应 | |
| B. | 乙醇、乙酸都能与NaOH溶液反应 | |
| C. | 乙醇、乙酸都能使紫色石蕊试液变红色 | |
| D. | 乙醇、乙酸互为同分异构体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com