
【题目】已知:Fe2O3(s)+3C(石墨)![]() 2Fe(s)+3CO(g) ΔH=+489.0 kJ·mol1①
2Fe(s)+3CO(g) ΔH=+489.0 kJ·mol1①
CO(g)+![]() O2(g)
O2(g)![]() CO2(g) ΔH=283.0 kJ·mol1②
CO2(g) ΔH=283.0 kJ·mol1②
C(石墨)+O2(g)![]() CO2(g) ΔH=393.5 kJ·mol1③
CO2(g) ΔH=393.5 kJ·mol1③
则4Fe(s)+3O2(g)![]() 2Fe2O3(s)的ΔH为
2Fe2O3(s)的ΔH为
A.+1 164.1 kJ·mol1 B.1 641.0 kJ·mol1
C.259.7 kJ·mol1 D.519.4 kJ·mol1
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案 全优冲刺100分系列答案
全优冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】一定温度下,向一个容积为2L的真空密闭容器中(事先装入催化剂)通入1 mol N2和3 mol H2,发生下列反应:N2+3H2![]() 2NH3,3 min后测得密闭容器内的压强是起始时的0.9倍,在此时间内v(H2)是( )
2NH3,3 min后测得密闭容器内的压强是起始时的0.9倍,在此时间内v(H2)是( )
A.0.2 mol·L-1·min-1 B.0.6 mol·L-1·min-1
C.0.1 mol·L-1·min-1 D.0.3 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知HCO3﹣+AlO2﹣+H2O═CO32﹣+Al(OH)3↓;将足量的KHCO3溶液不断滴入含等物质的量的KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀的物质的量与滴入的KHCO3溶液体积的关系可表示为( )
A.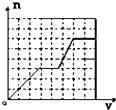
B.
C.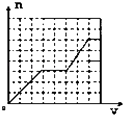
D.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫及其化合物对人类的生产和生活有着重要的作用.
2SO2(g)+O2(g)2SO3(g)△H=﹣198kJmol﹣1是制备硫酸的重要反应.
(1)在容积为V L的密闭容器中起始充入2mol SO2和1mol O2 , 反应在不同条件下进行,反应体系总压强随时间的变化如下图所示.与实验a相比,实验b改变的条件是 , 判断的依据 . 
(2)二氧化硫在一定条件下还可以发生如下反应:
SO2(g)+NO2(g)SO3(g)+NO(g)△H=﹣42kJmol﹣1 .
在1L恒容密闭容器中充入SO2(g)和NO2(g),所得实验数据如下:
实验编号 | 温度 | 起始时物质的量/mol | 平衡时物质的量/mol | |
N(SO2) | N(NO2) | N(NO) | ||
甲 | T1 | 0.80 | 0.20 | 0.18 |
乙 | T2 | 0.20 | 0.80 | 0.16 |
丙 | T3 | 0.20 | 0.30 | a |
①实验甲中,若2min时测得放出的热量是4.2kJ,则0~2min时间内,用SO2(g)表示的平均反应速率v(SO2)= , 该温度下的平衡常数 .
②实验丙中,达到平衡时,NO2的转化率为 .
③由表中数据可推知,TlT2(填“>”“<’’或“=”),判断的理由是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程.反应过程的示意图如下: 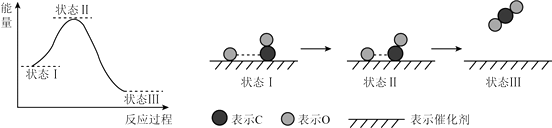
下列说法正确的是( )
A.CO和O生成CO2是吸热反应
B.在该过程中,CO断键形成C和O
C.CO和O生成了具有极性共价键的CO2
D.状态Ⅰ→状态Ⅲ表示CO与O2反应的过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己烯雌酚是一种激素类药物,结构如图所示,下列有关叙述中正确的是( ) 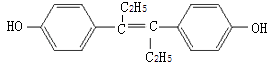
A.该有机物属于芳香烃
B.该物质不能使酸性高锰酸钾溶液褪色
C.该分子对称性好,所以没有顺反异构
D.该有机物分子中,最多可能有18个碳原子共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图所示装置除去含有CN﹣、Cl﹣ 废水中的CN﹣时,控制溶液pH为9~10,阳极产生的ClO﹣将CN﹣氧化为两种无污染的气体,下列说法不正确的是( ) 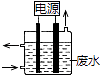
A.用石墨作阳极,铁作阴极
B.阳极的电极反应式:Cl﹣+2OH﹣﹣2e﹣═ClO﹣+H2O
C.阴极的电极反应式:2H2O+2e﹣═H2↑+2OH﹣
D.除去CN﹣的反应:2CN﹣+5ClO﹣+2H+═N2↑+2CO2↑+5Cl﹣+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】车辆排放的氮氧化物、煤燃烧产生的二氧化硫是导致雾霾天气的“罪魁祸首”.活性炭可处理大气污染物NO.在5L密闭容器中加入NO和活性炭(假设无杂质),一定条件下生成气体E和F.当温度分别在T1和T2时,测得各物质平衡时物质的量(n/mol)如表:
物质 | 活性炭 | NO | E | F |
初始 | 3.000 | 0.10 | 0 | 0 |
T1 | 2.960 | 0.020 | 0.040 | 0.040 |
T2 | 2.975 | 0.050 | 0.025 | 0.025 |
(1)写出NO与活性炭反应的化学方程式;
(2)计算上述反应T1℃时的平衡常数K1=;
(3)上述反应T1℃时达到化学平衡后再通入0.1molNO气体,则达到新化学平衡时NO的转化率为;
(4)如图为在T1℃达到平衡后在t2、t3、t4、t5时改变某一个反应条件,平衡体系中反应速率随时间变化的情况,且所改变的条件均不同.已知t3﹣t4阶段为使用催化剂.请判断该反应△H0(填“>”或“<”). 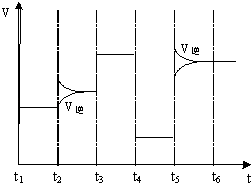
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com